El agua de mar, esa vasta extensión azul que cubre la mayor parte de nuestro planeta, es mucho más que simple H2O. Constituye una compleja disolución, una mezcla de sustancias que le confieren sus características únicas. La pregunta de si el agua de mar filtrada se considera homogénea o heterogénea es fundamental para comprender su naturaleza y sus aplicaciones. Para desentrañar esta cuestión, debemos examinar en profundidad su composición, las teorías sobre su origen y las propiedades fisicoquímicas que la definen.

Orígenes y Composición del Agua de Mar: Un Legado Geológico
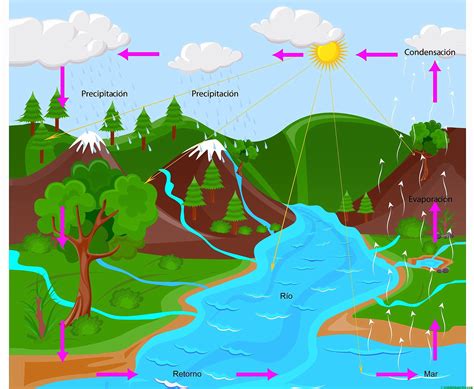
Las teorías científicas sobre los orígenes del agua marina se remontan a 1715, con la propuesta de Edmond Halley. Halley postuló que la sal y otros minerales eran arrastrados al mar por los ríos desde los continentes, como resultado del lavado continuo de los minerales terrestres por la lluvia. Una vez en el océano, estas sales se habrían concentrado progresivamente a través del ciclo hidrológico. Halley también observó que los lagos sin salida al mar, como el Mar Muerto o el Mar Caspio, presentaban altas concentraciones salinas, lo que apoyaba su teoría.
Si bien la teoría de Halley era parcialmente correcta, la composición actual del agua de mar es el resultado de procesos más complejos. A la aportación de sales por los ríos se suma la presencia de sodio en el fondo oceánico desde su formación. El cloro, otro ion salino predominante, parece provenir de escapes gaseosos del interior de la Tierra, liberados a través de fuentes hidrotermales y erupciones volcánicas. La teoría comúnmente aceptada es que la salinidad del agua de mar se ha mantenido relativamente estable durante miles de millones de años, con un ciclo continuo de iones que entran y salen del interior terrestre. La salinidad no ha crecido significativamente en eones, en parte debido a la acumulación de sal en los sedimentos.
El agua de mar es, en esencia, una disolución acuosa (H2O) de una gran variedad de sustancias. Se estima que hasta dos tercios de los elementos químicos naturales están presentes en el agua de mar, aunque la mayoría se encuentra en concentraciones muy bajas, como trazas. Un aspecto crucial que simplifica su estudio es que las proporciones relativas de los componentes principales son notablemente constantes, a pesar de que la concentración total de todas las sustancias disueltas, conocida como salinidad, puede variar considerablemente.
La salinidad se expresa comúnmente en tanto por mil (‰). Esta medida varía significativamente entre diferentes cuencas oceánicas, latitudes y profundidades. El Mar Rojo, rodeado por regiones áridas, presenta la mayor salinidad entre los mares abiertos, alcanzando hasta 40 ‰. En contraste, el Mar Báltico muestra la salinidad más baja (alrededor de 6 ‰ en las aguas superficiales del Golfo de Botnia). Esta baja salinidad se debe a su escasa profundidad, un clima frío y la gran cantidad de cuencas fluviales que vierten sus aguas en él, además de una topografía casi cerrada que limita el intercambio con el océano. En lagos y mares cerrados, la salinidad puede ser aún más variable, desde un 12 ‰ en el Mar Caspio hasta un asombroso 330 ‰ en las capas superficiales del Mar Muerto. La existencia de drenaje, con uno o más emisarios, o la predominancia de la evaporación como único mecanismo de compensación de aportes, son factores clave que determinan la salinidad de mares interiores.
Propiedades Fisicoquímicas del Agua de Mar
La salinidad es un factor determinante en varias propiedades del agua de mar. Las sales disueltas en el agua se disocian en iones, que son átomos con carga eléctrica positiva o negativa. Estos iones tienen la capacidad de intercambiar electrones con partículas vecinas.
Una de las propiedades más importantes del agua de mar es su densidad. Esta se determina mediante la ecuación internacional de estado del agua de mar a presión atmosférica, formulada por la UNESCO. Esta ecuación se basa en extensos trabajos para establecer las relaciones entre las variables termodinámicas del agua de mar: densidad, presión, salinidad y temperatura. La densidad media en superficie del agua de mar es de aproximadamente 1.025 g/ml, lo que la hace más densa que el agua dulce o el agua pura.
La temperatura también influye significativamente. A mayor contenido de sal, el punto de congelación del agua de mar desciende. Por ello, el agua marina se solidifica (se convierte en hielo) a temperaturas inferiores a los -2 °C. Se ha registrado una corriente en la Antártida que se mantiene a -2.6 °C, lo que demuestra la influencia de la salinidad en el punto de congelación. El fenómeno del descenso crioscópico es la reducción del punto de congelación de un disolvente puro por la presencia de solutos. Este efecto es directamente proporcional a la molalidad de la disolución y es más pronunciado para solutos iónicos, como los predominantes en el agua de mar. En las regiones polares, este descenso crioscópico provoca que, al enfriarse intensamente el agua del océano, se produzca la separación de una fase sólida flotante de agua pura.
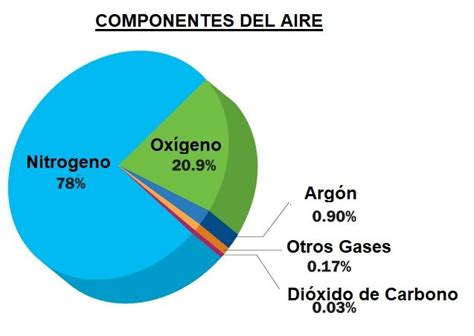
Los gases disueltos en el agua de mar son los mismos que componen el aire atmosférico, pero en proporciones distintas. Factores como la temperatura y la salinidad influyen en la solubilidad de estos gases: a mayor temperatura o salinidad, menor es la solubilidad. La actividad metabólica de los organismos marinos y los equilibrios químicos con solutos como el ion bicarbonato (HCO3-) también juegan un papel crucial. En las aguas oceánicas superficiales bien mezcladas, la composición típica de gases disueltos incluye aproximadamente un 64% de nitrógeno (N2), un 34% de oxígeno (O2) y un 1.8% de dióxido de carbono (CO2). Curiosamente, la concentración de CO2 en el agua de mar es considerablemente mayor que en el aire libre (0.04%). El oxígeno abunda en la superficie, donde la fotosíntesis supera a la respiración, y tiende a disminuir a profundidades de unos 400 metros. A esta profundidad, los efectos de la difusión desde la superficie y la fotosíntesis ya no son tan significativos, pero la alta densidad de organismos consumidores agota el oxígeno disponible.
¿Homogénea o Heterogénea? La Naturaleza de las Mezclas
Para abordar la cuestión de si el agua de mar filtrada es homogénea o heterogénea, debemos definir estos términos en el contexto de las mezclas. Las mezclas constituyen la mayor parte de la materia en la naturaleza y se forman por la unión de dos o más sustancias en proporciones variables, donde cada componente mantiene sus propiedades físicas y químicas.
Las mezclas homogéneas, también conocidas como sistemas homogéneos o disoluciones químicas, se caracterizan por presentar una única fase observable. Aunque el agua potable, por ejemplo, es una mezcla de agua y sales, a simple vista solo se percibe la fase líquida. En estas mezclas, cada sustancia constituyente aporta sus propiedades específicas al sistema. El agua de mar filtrada, donde las sales están completamente disueltas, es un ejemplo clásico de mezcla homogénea. La sal más abundante en el agua de mar es el cloruro de sodio (NaCl), la sal común de mesa.
En una mezcla homogénea, la fase dispersa (las sustancias en menor proporción) se disuelve completamente en la fase dispersante (la sustancia en mayor proporción). Las partículas de la fase dispersa no se depositan en el fondo del recipiente y mantienen la homogeneidad con la fase dispersante. Además, las mezclas homogéneas suelen ser translúcidas, permitiendo el paso de la luz. En un sistema homogéneo, las propiedades de sus componentes se conservan; por ejemplo, el azúcar mantiene su sabor dulce al disolverse en té.
Por otro lado, las mezclas heterogéneas son aquellas en las que se pueden distinguir dos o más fases o componentes. Un ejemplo común es el agua con piedras, donde tanto el agua como las piedras son claramente visibles. La sangre, aunque a simple vista pueda parecer homogénea, es en realidad una mezcla heterogénea compleja, fundamental para la vida humana. En el contexto del agua de mar, si estuviera contaminada con partículas sólidas no disueltas, como arena o algas, o si existieran capas de diferente salinidad no completamente mezcladas, podría presentar características heterogéneas. Sin embargo, el agua de mar "filtrada" implica la eliminación de partículas sólidas, y si el proceso de filtración es efectivo y la disolución de sales es completa, el resultado es una mezcla homogénea.
Métodos de Desalinización: Transformando el Agua Marina
La necesidad de obtener agua dulce a partir del agua de mar ha impulsado el desarrollo de diversas tecnologías de desalinización. La unidad de destilación solar utilizada por los 4083 habitantes de Symi, una isla griega, produce 15.000 litros diarios de agua dulce. En Wrightsville Beach, Carolina del Norte, una planta de congelación genera 750.000 litros de agua destilada diariamente.
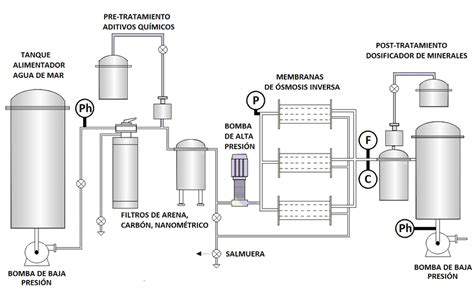
La ósmosis inversa es un método moderno y eficiente que desala el agua forzándola a través de una membrana sintética semipermeable. Otro método es la hidratación, que implica la mezcla de propano con el agua salada. Para aguas con salinidad moderada, como el agua salobre encontrada en Webster, Dakota del Sur (con una salinidad casi el doble de lo considerado aceptable por el gobierno, pero mucho menor que el agua de mar), se puede emplear la electrodiálisis. Sin embargo, este proceso resulta costoso cuando la concentración de sales es alta.
En resumen, el agua de mar es una disolución compleja cuya naturaleza, tras un proceso de filtración adecuado, se clasifica como una mezcla homogénea. Su salinidad y composición son el resultado de miles de millones de años de procesos geológicos y químicos, y sus propiedades fisicoquímicas, como la densidad y el punto de congelación, son determinantes para los ecosistemas marinos y para las aplicaciones humanas, incluida la obtención de agua dulce a través de tecnologías de desalinización. La comprensión de estas características es esencial para apreciar la magnitud y la importancia del agua de mar en nuestro planeta.