El cloruro de berilio, con la fórmula química BeCl₂, es un compuesto inorgánico de notable interés en la química. Se presenta como un sólido incoloro y posee una marcada higroscopicidad, lo que significa que tiende a absorber la humedad del ambiente. Esta característica influye en su manejo y almacenamiento, requiriendo condiciones controladas para preservar su pureza. Su solubilidad es considerable en una variedad de disolventes polares, facilitando su uso en diversas reacciones y procesos químicos.
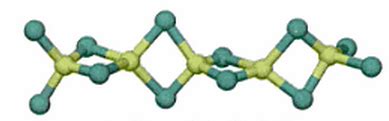
Estructuras Cristalinas del Cloruro de Berilio
La investigación ha revelado la existencia de dos polimorfos del cloruro de berilio, cada uno con una disposición atómica distintiva. Ambas estructuras comparten la característica de presentar centros de berilio en estado de oxidación +2 (Be²⁺) que se encuentran interconectados por ligandos de cloruro que actúan como puentes dobles.
Una de estas formas cristalinas se compone de politetraedros que comparten bordes. Esta disposición tridimensional crea una red sólida con propiedades específicas. La otra forma, por su parte, exhibe una estructura que se asemeja al yoduro de zinc. En esta configuración, se observan jaulas interconectadas que recuerdan a la estructura del adamantano, una molécula orgánica cíclica conocida por su rigidez y simetría.
Comportamiento del Cloruro de Berilio en Fase Gaseosa
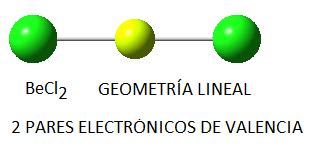
En estado gaseoso, el cloruro de berilio adopta formas moleculares diferentes a las de su estado sólido. Este compuesto puede existir como un monómero lineal, donde los átomos de berilio y cloro se disponen en una línea recta. Esta geometría lineal es precisamente la predicha por la teoría TRePEV (Teoría de Repulsión de Pares de Electrones de la Capa de Valencia), que explica la geometría molecular basándose en la repulsión entre los pares de electrones de la capa de valencia.
Además de la forma monomérica lineal, en fase gaseosa también se ha identificado la existencia de un dímero puenteado. En esta estructura dimérica, dos átomos de cloro actúan como puentes entre dos átomos de berilio. En el dímero, el átomo de berilio se encuentra en un estado de coordinación de tres, lo que difiere de la coordinación tetraédrica observada en algunas de sus formas sólidas.
Reacción del Cloruro de Berilio con Agua
Cuando el cloruro de berilio se introduce en agua, ocurre una reacción de hidratación que da lugar a la formación de un tetrahidrato, cuya fórmula química es BeCl₂•4H₂O. La especie predominante en esta disolución acuosa es el ion tetrahidroxoberilato ([Be(H₂O)₄]²⁺), asociado con dos aniones cloruro (Cl⁻). La presencia de las moléculas de agua coordinadas alrededor del ion berilio es fundamental para la estabilidad de este complejo acuoso. Las investigaciones sobre la hidratación del berilio(II) en soluciones acuosas, utilizando técnicas espectroscópicas vibracionales y estudios ab initio de orbitales moleculares, han proporcionado una comprensión detallada de estas interacciones.
Además de su solubilidad en agua, el BeCl₂ también muestra afinidad por ciertos éteres, lo que amplía su versatilidad como reactivo en síntesis orgánica e inorgánica.
El Ion Hipoclorito: Un Agente Oxidante Potente
El ion hipoclorito, también conocido por las nomenclaturas sistemáticas de la IUPAC y de Stock como monoxoclorato(I) o monoxoclorato(1-), es un oxoanión con la fórmula química ClO⁻. En este ion, el átomo de cloro se encuentra en un estado de oxidación de +1. Los hipocloritos son sales que derivan del ácido hipocloroso (HClO).
Ejemplos comunes y de gran relevancia en la vida cotidiana y la industria incluyen el hipoclorito de sodio (NaClO), ampliamente conocido como lejía, lavandina o agente blanqueante, y el hipoclorito de calcio (Ca(ClO)₂), presente en la lejía en polvo.
Inestabilidad y Reactividad de los Hipocloritos
Los hipocloritos son, en general, compuestos bastante inestables. Un ejemplo ilustrativo es el hipoclorito de sodio, que no se comercializa en forma sólida pura. Al intentar eliminar el agua de una disolución de NaClO, este compuesto tiende a sufrir una reacción de dismutación. Esta reacción resulta en la formación de una mezcla de cloruro de sodio (NaCl) y clorato de sodio (NaClO₃). El calentamiento de una disolución de hipoclorito de sodio también induce esta misma reacción de dismutación.
Debido a su inherente inestabilidad, los hipocloritos actúan como agentes oxidantes muy potentes. Las reacciones que involucran hipocloritos y compuestos orgánicos son frecuentemente exotérmicas, liberando una cantidad significativa de calor. En algunos casos, estas reacciones pueden ser lo suficientemente vigorosas como para provocar combustiones. Por esta razón, es crucial manejar los hipocloritos con la máxima precaución.
Aplicaciones Domésticas e Industriales de los Hipocloritos
La capacidad de los hipocloritos para actuar como agentes oxidantes los convierte en herramientas valiosas en diversas aplicaciones. Se utilizan de manera generalizada en el hogar y en la industria como agentes blanqueantes. Su función principal es la de eliminar o degradar los colorantes, permitiendo blanquear la ropa, aclarar el color del cabello y eliminar manchas difíciles de diversas superficies.
Más allá de sus propiedades blanqueantes, los hipocloritos son ampliamente empleados como desinfectantes y desodorantes de amplio espectro. Su poder oxidante les permite destruir microorganismos patógenos, como bacterias y virus, y neutralizar compuestos orgánicos volátiles responsables de malos olores.
Hipocloritos como Agentes Oxidantes Fuertes
Dentro de la familia de los oxoaniones del cloro, los hipocloritos se destacan por ser los agentes oxidantes más potentes. Su elevada capacidad oxidante les permite reaccionar y oxidar a casi cualquier sustancia que actúe como agente reductor. Esta propiedad subraya su eficacia en aplicaciones de limpieza, desinfección y en procesos químicos donde se requiere una fuerte oxidación.
Precauciones en el Uso de Hipocloritos
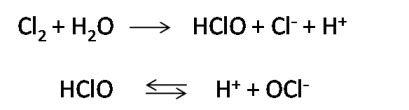
Es fundamental destacar la importancia de manejar los hipocloritos con precaución, especialmente en el contexto doméstico. Una de las advertencias más cruciales es evitar la mezcla de lejía (hipoclorito de sodio) con ácidos fuertes, como el ácido clorhídrico (HCl). La reacción entre un hipoclorito y un ácido genera cloro gaseoso (Cl₂), un gas tóxico y peligroso para la salud. Esta advertencia es particularmente relevante al considerar la combinación de productos de limpieza de uso común.
Manejo del hipoclorito
Nomenclatura y Estados de Oxidación
En las nomenclaturas sistemáticas de la IUPAC y de Stock, cuando se utiliza un número romano entre paréntesis, este indica el estado de oxidación del átomo de cloro dentro del ion o compuesto en cuestión. Siguiendo esta convención, el término "clorato" se refiere a cualquier oxoanión de cloro, independientemente de su estado de oxidación específico, aunque el hipoclorito se caracteriza por el estado de oxidación +1 del cloro.
El Berilio y la Química de Coordinación
El berilio, a pesar de ser un metal alcalinotérreo, presenta una química de coordinación particular. El cloruro de berilio, al ser un compuesto iónico-covalente, participa en la formación de complejos de coordinación. En disolución acuosa, el ion Be²⁺ tiende a formar complejos octaédricos o tetraédricos con moléculas de agua, como se observa en el tetrahidrato. La fuerte polaridad del enlace Be-Cl y la alta densidad de carga del ion Be²⁺ contribuyen a su tendencia a formar complejos estables con ligandos donadores de electrones.
Comparación entre Cloruro de Berilio e Hipoclorito
Aunque ambos compuestos contienen cloro y berilio respectivamente, sus propiedades y aplicaciones son radicalmente diferentes. El cloruro de berilio es un compuesto con una estructura cristalina compleja y un comportamiento particular en fase gaseosa, con aplicaciones más centradas en la química inorgánica y la síntesis. Por otro lado, el ion hipoclorito es un anión reactivo y un potente agente oxidante, cuyas aplicaciones principales se encuentran en la desinfección, el blanqueo y la oxidación. La confusión entre ellos es improbable dada la disparidad de sus roles químicos.
Perspectivas Futuras y Aplicaciones Potenciales
La investigación continua sobre el cloruro de berilio y sus derivados podría abrir nuevas vías para su aplicación en catálisis, ciencia de materiales o como precursor en la síntesis de otros compuestos de berilio. La comprensión detallada de sus estructuras polimórficas y su comportamiento en diferentes fases podría ser clave para diseñar materiales con propiedades específicas. En cuanto a los hipocloritos, si bien sus usos están bien establecidos, la optimización de su estabilidad y la búsqueda de formulaciones más seguras y eficientes siguen siendo áreas de interés.
El estudio de la química del berilio, incluyendo compuestos como el cloruro de berilio, es un campo que, a pesar de los desafíos inherentes a la toxicidad del elemento, sigue proporcionando información valiosa sobre los principios fundamentales de la química inorgánica y la formación de enlaces. La capacidad del berilio para formar estructuras poliméricas y complejos de coordinación únicas lo convierte en un objeto de estudio fascinante para químicos teóricos y experimentales.
La interacción entre el cloruro de berilio y disolventes, como se observa con los éteres, sugiere posibilidades para su uso en reacciones de transferencia de fase o como reactivo en medios no acuosos. La exploración de estas interacciones podría expandir el repertorio de reacciones en las que el cloruro de berilio puede participar.
En el ámbito de los hipocloritos, la búsqueda de alternativas más sostenibles o de métodos de generación in situ para reducir el transporte y almacenamiento de estos compuestos reactivos es un área de investigación activa, impulsada por consideraciones de seguridad y medioambientales.