El hipoclorito de sodio (NaCIO) es un compuesto químico de vital importancia en la desinfección del agua, especialmente en el ámbito del agua de consumo. Su eficacia bactericida, bajo costo y la presencia de un cloro residual que mantiene su acción desinfectante en la red de distribución lo convierten en una herramienta fundamental para garantizar la salud pública. Este artículo se adentra en los aspectos clave de la determinación de hipoclorito de sodio en el agua, abarcando desde su naturaleza química y mecanismos de acción hasta las normativas que rigen su uso y los métodos analíticos para su cuantificación.
Naturaleza Química y Mecanismo de Acción del Hipoclorito de Sodio
El hipoclorito de sodio es una sustancia altamente alcalina, con un pH que típicamente oscila entre 11 y 13. Esta alcalinidad no solo contribuye a su estabilidad y eficacia como desinfectante, sino que también explica su baja tensión superficial, inferior a la del agua, lo que facilita su penetración en diversas superficies. La acción desinfectante del hipoclorito de sodio se fundamenta en su capacidad para desnaturalizar y solubilizar las proteínas presentes en la envoltura de los microorganismos, incluyendo virus, bacterias, hongos y esporas, conduciendo a su desintegración. En medio alcalino, el equilibrio químico de las soluciones de hipoclorito de sodio favorece la forma iónica disociada, el hipoclorito de sodio, que es más estable y menos reactiva que el ácido hipocloroso. Las soluciones de hipoclorito de sodio exhiben un equilibrio dinámico representado por la siguiente ecuación:
Cl₂ (g) + 2NaOH (ac) → NaCl (ac) + NaCIO (ac) + H₂O (l)
Este equilibrio es sensible al pH. En medios ácidos, el equilibrio se desplaza hacia la formación de ácido hipocloroso (HClO) y cloro gaseoso (Cl₂), ambos altamente tóxicos y reactivos. Por esta razón, la vida útil de las soluciones de hipoclorito de sodio es más prolongada en soluciones con pH elevado.
El hipoclorito de sodio ha sido utilizado como desinfectante durante más de siete décadas y ha demostrado ser efectivo contra un amplio espectro de patógenos, incluyendo bacterias grampositivas y gramnegativas, hongos, esporas y virus, incluso los coronavirus. Es el ingrediente activo del blanqueador doméstico y se emplea extensamente para purificar agua y desinfectar piscinas.
Usos y Aplicaciones del Hipoclorito de Sodio
La versatilidad del hipoclorito de sodio se refleja en su amplia gama de aplicaciones en diversos sectores industriales y de consumo. Históricamente, su descubrimiento a finales del siglo XVIII marcó un hito en la industria textil, donde se utilizó por primera vez para blanquear algodón, demostrando su capacidad para eliminar manchas a temperatura ambiente.
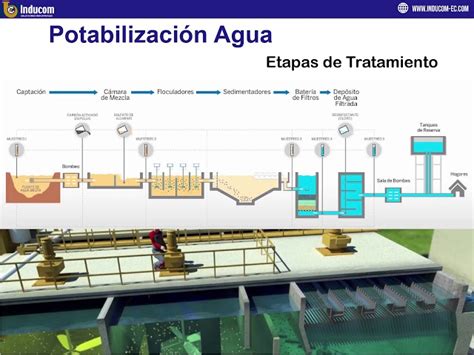
Tratamiento de Agua de Consumo
En el tratamiento de aguas, el hipoclorito de sodio es un agente desinfectante primordial. Al final de la etapa de desinfección en las plantas de tratamiento, el agua contiene dos formas de cloro residual: el cloro libre y el cloro combinado. El cloro libre es el más efectivo desinfectante, mientras que el cloro combinado, formado por la reacción del cloro libre con aminas o amoniaco, es menos potente pero persiste por más tiempo en la red de distribución, asegurando la desinfección continua.
Otros Sectores Industriales
Además del tratamiento de agua, el hipoclorito de sodio encuentra aplicaciones significativas en:
- Agricultura: Utilizado para la desinfección de equipos e instalaciones.
- Industria Química: Como reactivo en diversas síntesis.
- Industria de Pintura y Cal: En procesos de blanqueo.
- Industria Alimentaria: Para la desinfección de superficies y equipos.
- Industria del Vidrio: En procesos de limpieza.
- Industria del Papel: Como agente blanqueador.
- Industria Farmacéutica: En la desinfección de áreas y equipos.
- Síntesis de Compuestos: Como precursor en la fabricación de otros químicos.
- Eliminación de Residuos: En el tratamiento de aguas residuales para reducir olores y desinfectar.
- Industria Textil: Para el blanqueo de fibras y tejidos.
En el ámbito doméstico y de oficinas, su uso es frecuente para fines de limpieza y desinfección general.
Normativa y Seguridad en el Uso del Hipoclorito de Sodio
El uso del hipoclorito de sodio está regulado por normativas específicas para garantizar la seguridad y la calidad del agua tratada. En España, el Real Decreto 3/2023 establece los límites máximos permitidos para los niveles de cloro libre y cloro combinado residual en el agua de consumo. Estos parámetros son cruciales para asegurar una desinfección efectiva sin comprometer la salud de los consumidores.
Riesgos y Precauciones
Dada su naturaleza altamente alcalina, el hipoclorito de sodio presenta riesgos de irritación en contacto con la piel, ojos y vías respiratorias. Su manejo inadecuado puede tener consecuencias graves. Es fundamental tener en cuenta las siguientes precauciones:
- Reacciones Violentas: Puede reaccionar de forma violenta con compuestos ácidos, liberando cloro gaseoso tóxico. Por ello, nunca debe mezclarse con ácidos como el clorhídrico, cítrico o acético.
- Mezclas Peligrosas: La combinación con amoniaco produce vapores de cloro o cloramina, gases irritantes. Tampoco debe mezclarse con alcohol o peróxido de hidrógeno, ya que pueden generarse cloroformo, cloratos y reacciones exotérmicas peligrosas.
- Uso de Agua Caliente: No debe utilizarse en combinación con agua caliente, ya que esto puede acelerar su descomposición y la liberación de gases.
El hipoclorito de sodio es una sustancia química inorgánica que, si bien es inflamable, su solución es una base débil. Un pH de 11 es irritante, mientras que un pH de 13 se considera corrosivo.
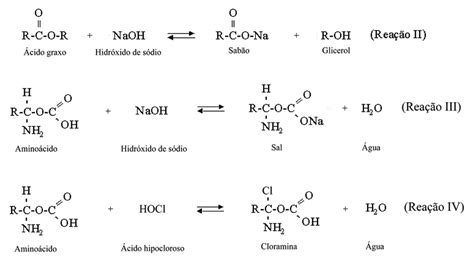
Formación de Nitrosaminas
Un aspecto de seguridad relevante, especialmente en el caso de la cloraminación, es la potencial formación de nitrosaminas, como la N-nitrosodimetilamina (NDMA, CAS: 62-75-9). Las NDMA pueden formarse como un subproducto de la cloraminación del agua, particularmente en pequeños abastecimientos. Si se supera el valor paramétrico de cloro combinado residual en la red de distribución, se recomienda la aplicación rápida de medidas correctoras para mitigar este riesgo. La relación entre el cloro combinado residual y la formación de nitrosaminas subraya la importancia de un control riguroso de los procesos de desinfección.
Métodos de Determinación de Hipoclorito de Sodio
La medición precisa de la concentración de hipoclorito de sodio es fundamental para garantizar su calidad, eficacia y seguridad. Permite determinar la concentración de cloro activo, esencial para su capacidad desinfectante.
Titulación como Método Analítico
Uno de los métodos más fiables y utilizados para determinar la concentración de hipoclorito de sodio es la titulación. Este método analítico proporciona resultados precisos y confiables, siendo accesible debido a la utilización de reactivos comunes como tiosulfato de sodio, yoduro de potasio y ácido acético glacial. Es un método estandarizado y aceptado internacionalmente por organismos como ASTM, AOAC e ISO, lo que facilita su implementación en laboratorios de control de calidad.
El principio básico de la titulación para determinar hipoclorito de sodio implica la reacción del hipoclorito con yoduro de potasio en medio ácido (generalmente ácido acético), liberando yodo (I₂). El yodo liberado se valora posteriormente con una solución de tiosulfato de sodio, utilizando almidón como indicador.
La reacción general puede esquematizarse de la siguiente manera:
Oxidación del yoduro:CIO⁻ + 2I⁻ + 2H⁺ → I₂ + Cl⁻ + H₂O
Valoración del yodo:I₂ + 2S₂O₃²⁻ → 2I⁻ + S₄O₆²⁻
El conocimiento de la concentración del hipoclorito en gramos por litro (gr./l.) de una solución concentrada comercialmente (aproximadamente 13% de cloro disponible) permite calcular la cantidad de cloro activo. Por ejemplo, si la concentración es del 13% y el peso específico de la solución es 1.24, la cantidad de cloro activo en gramos por litro se puede estimar como:
1.240 gr./l. (solución) x 0.13 (concentración) = 161 gr. aprox. de cloro activo por litro.
Otros Factores que Influyen en la Desinfección
El efecto desinfectante del cloro en el agua no solo depende de la cantidad de cloro activo, sino también de otros factores cruciales:
- pH del agua: Como se mencionó, el pH influye significativamente en la forma química del cloro y, por ende, en su poder desinfectante. Un pH más alto reduce la eficacia del cloro.
- Temperatura del agua: A temperaturas elevadas, el cloro se degrada más rápidamente, disminuyendo su efectividad. Si la temperatura es mayor de 30 ºC, la degradación se acelera.
- Tiempo de contacto: El tiempo que el desinfectante permanece en contacto con el agua y los microorganismos es esencial para una desinfección completa.
- Tipo de microorganismo: La resistencia de los diferentes microorganismos al cloro varía.
Degradación del Hipoclorito de Sodio y Formación de Cloratos
El hipoclorito de sodio es un compuesto que se degrada con el tiempo, un proceso que se ve acelerado por la exposición a la luz, el calor y un pH elevado. Esta degradación conduce a la formación de clorato (ClO₃⁻) en la solución. El aumento de la concentración de clorato en el hipoclorito sódico con el tiempo es un fenómeno conocido desde hace bastantes años.
Esta degradación puede generar problemas en los sistemas de distribución de agua, especialmente en puntos donde se realizan reencloraciones con hipoclorito degradado. Concentraciones elevadas de clorato pueden ser indeseables.
Para abordar esta problemática, se proponen medidas como la instalación de equipos para analizar muestras de hipoclorito sometido a distintas condiciones de almacenamiento (temperatura, tiempo) con el fin de elaborar recomendaciones para su almacenamiento y uso desde la recepción en las Estaciones de Tratamiento de Agua Potable (ETAP). Asimismo, se considera la ampliación de este control a los depósitos de red donde se realizan reencloraciones.
Consideraciones sobre el Clorato
El hipoclorito de sodio, al descomponerse, puede transformar impurezas, como el bromuro, en bromato. La formación de bromato a partir de clorato es una preocupación en el tratamiento de agua, especialmente en condiciones de pH elevado, como las que presenta el hipoclorito de sodio.
Equipos y Reactivos para el Análisis
La determinación de hipoclorito de sodio y la monitorización de sus parámetros en el agua de consumo pueden requerir el uso de diversos equipos y reactivos. Estos pueden incluir:
- Equipos de dosificación: Válvulas, rotámetros, etc., para la correcta adición del hipoclorito en el tratamiento.
- Reactivos de titulación: Tiosulfato de sodio, yoduro de potasio, ácido acético glacial, almidón como indicador.
- Equipos de medición de pH: Para controlar la alcalinidad de las soluciones y del agua tratada.
- Equipos analíticos: Fotómetros o espectrofotómetros para análisis más precisos y automatizados de cloro residual.
- Kits de análisis: Para mediciones rápidas en campo de cloro libre y total.
La elección de los equipos y métodos analíticos dependerá de la precisión requerida, la frecuencia de los análisis y los recursos disponibles.
El Hipoclorito de Sodio como Antiséptico Histórico
El hipoclorito de sodio no es un descubrimiento reciente. Sus propiedades antisépticas fueron reconocidas y utilizadas desde hace bastante tiempo. De hecho, ya era usado como antiséptico en hospitales, y su poder desinfectante fue crucial en momentos históricos. Un ejemplo significativo fue la epidemia de fiebre tifoidea en Inglaterra en 1897, donde su aplicación demostró ser un avance importante en el control de enfermedades transmitidas por el agua.
Consideraciones Adicionales
El hipoclorito de sodio se descompone con facilidad, por lo que su almacenamiento y manipulación deben realizarse con cuidado. Las soluciones comerciales fuertes, que contienen entre el 12% y el 15% de cloro disponible, requieren precauciones especiales.
La electrólisis de cloruro de sodio es un método para la producción de hipoclorito de sodio. En este proceso, el cloruro de sodio reacciona y forma NaCIO, liberando hidrógeno en el cátodo. Este método permite la preparación de soluciones de hipoclorito in situ, lo que puede ser ventajoso para ciertos abastecimientos.
En el contexto de la determinación de hipoclorito de sodio, es importante considerar que la concentración puede variar. Por ejemplo, se pueden encontrar diluciones con cantidades específicas de hipoclorito, como 20 gr., 40 gr. en volúmenes determinados de agua, o la preparación de soluciones con proporciones como 5 ml. de hipoclorito concentrado en 50 ml. de agua, o 2.5 ml. en 25 ml., 15 ml. en 10 ml. Estas diluciones son ejemplos de cómo se puede ajustar la concentración para diferentes aplicaciones.
La sustancia química inorgánica hipoclorito de sodio está sujeta a la regulación (CE) No. 1907/2006, referente al registro, evaluación, autorización y restricción de sustancias y preparados químicos.
18. ¿Por qué debemos clorar el agua que consumimos?
tags: #determinacion #de #hipoclorito #de #sodio #en