La gestión del fósforo en las aguas residuales es un componente esencial del tratamiento moderno, fundamental para salvaguardar nuestros cuerpos de agua de la contaminación por nutrientes. Al eliminar eficazmente el fósforo, las plantas de tratamiento de aguas residuales (EDAR) juegan un papel crucial en la prevención de floraciones algales masivas y la eutrofización, promoviendo así ecosistemas acuáticos más saludables, garantizando la seguridad del agua potable y mejorando la calidad del agua para actividades recreativas.
El fósforo es un nutriente vital para el crecimiento de las plantas, pero su exceso en el medio ambiente desencadena un enriquecimiento de nutrientes que puede llevar a una grave degradación ambiental de los ecosistemas acuáticos. En muchos sistemas de agua dulce, el fósforo es el nutriente limitante para el crecimiento de las algas. Cuando las algas consumen todo el fósforo disponible, mueren y su descomposición consume el oxígeno disuelto en el agua. Esta caída drástica en los niveles de oxígeno puede resultar en mortandades masivas de peces y otros organismos acuáticos que no pueden sobrevivir en condiciones hipóxicas.

Las floraciones algales no solo dañan la vida acuática y la calidad del agua, sino que también pueden afectar las fuentes de agua potable, generando problemas de sabor y olor. Las toxinas producidas por algunas algas representan riesgos significativos para la salud humana y animal. En 2021, los Centros para el Control y la Prevención de Enfermedades de EE. UU. informaron sobre los impactos negativos de estas floraciones. Además, las condiciones eutróficas hacen que las aguas recreativas sean inseguras para nadar y pescar, con posibles implicaciones socioeconómicas. Se estima que las floraciones de algas conllevan costos considerables para Estados Unidos, afectando tanto al medio ambiente como a la economía.
Fuentes y Formas del Fósforo en las Aguas Residuales
El fósforo (P) es un elemento químico de número atómico 15. Debido a su alta reactividad, no se encuentra de forma libre en la naturaleza, sino principalmente en forma de fosfato en minerales. Los organismos complejos, incluyendo plantas y animales, utilizan el fósforo, ya que los fosfatos son componentes esenciales del ADN, ARN, ATP y fosfolípidos. El ortofosfato, una de las formas más comunes, consiste en un átomo de fósforo unido a cuatro átomos de oxígeno, y a menudo se le denomina "fósforo reactivo" por su tendencia a unirse con otros compuestos. Los fosfatos condensados son varias moléculas de ortofosfato unidas, y el fósforo total abarca todas estas formas, incluyendo el fósforo orgánico.
Las aguas residuales urbanas son una fuente significativa de fósforo. Provienen principalmente del uso de detergentes sintéticos y de las excreciones humanas. Las heces humanas contienen entre un 3.0% y un 5.4% de fósforo (en forma de P2O5), y la orina entre un 2.5% y un 5.0%. Las concentraciones típicas de fósforo total en aguas residuales domésticas oscilan entre 6 y 20 mg/L. A nivel mundial, se estima que las aguas residuales urbanas (UWWW) son responsables de aproximadamente el 85% del fósforo descargado al medio ambiente.
Las aguas residuales de actividades acuícolas también contribuyen a la carga de fósforo, principalmente a través de alimento no consumido y excretas de los animales. En sistemas de recirculación acuícola (SRA), donde el agua se reutiliza extensivamente, los lodos producidos pueden presentar concentraciones de fósforo total superiores a las de los lodos domésticos, con un promedio del 1.3% de fósforo total en la masa sólida seca.
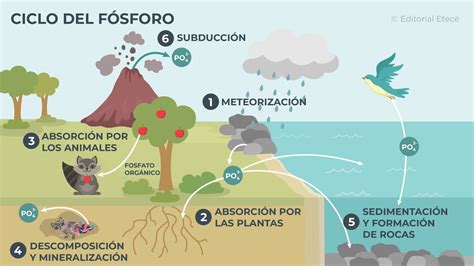
El Problema de la Eutrofización
Aunque los fosfatos no generan problemas de sabor y olor en el agua potable, sus altos niveles en los vertidos de aguas residuales tienen un impacto devastador en los ecosistemas acuáticos. Los altos niveles de fosfato aceleran el crecimiento de algas y plantas, provocando la eutrofización. Este fenómeno conduce a la creación de "zonas muertas" costeras, desprovistas de vida acuática debido a la falta de oxígeno. La proliferación de algas, como el sargazo observado en las costas de Florida, causa problemas ambientales severos, incluyendo la degradación de hábitats y la muerte de peces.
El fósforo es un nutriente esencial para las plantas y, particularmente, para el crecimiento de las algas. El vertido de fósforo, junto con otros nutrientes, en los cuerpos de agua receptores fomenta el crecimiento algal. Estas floraciones no solo son estéticamente desagradables, sino que también consumen grandes cantidades de oxígeno al morir y descomponerse, lo que resulta tóxico para la vida acuática. La contaminación por fósforo es una causa principal de pérdida de biodiversidad y contribuye a la degradación de ecosistemas de los que depende la humanidad. A escala mundial, las pérdidas de fósforo de la tierra a las aguas dulces se han duplicado en el último siglo, superando la capacidad del planeta para asimilarlo.
Métodos para la Eliminación de Fósforo de las Aguas Residuales
Las plantas de tratamiento de aguas residuales emplean diversas tecnologías para eliminar el fósforo antes de la descarga de los efluentes. Estos métodos se pueden clasificar principalmente en químicos y biológicos, con algunas tecnologías avanzadas que combinan ambos enfoques.
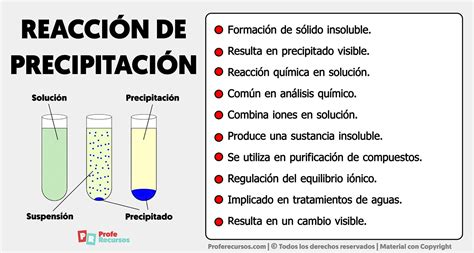
1. Precipitación Química
Este método consiste en la adición de productos químicos, conocidos como coagulantes, que reaccionan con el fósforo disuelto para formar compuestos insolubles. Estos compuestos se sedimentan y se eliminan como lodo, o se separan mediante filtración.
- Cal (Hidróxido de Calcio, Ca(OH)2): Se añade en forma de caliza. Reacciona con la alcalinidad del agua residual para formar carbonato de calcio, y a pH elevados (alrededor de 10), los iones de calcio reaccionan con el fosfato para precipitar como hidroxiapatito. La cantidad de cal requerida depende principalmente de la alcalinidad del agua residual, siendo aproximadamente 1.5 veces la alcalinidad expresada como CaCO3. Se requiere neutralización posterior para reducir el pH.
- Aluminio (Sulfato de Aluminio, Al2(SO4)3): El sulfato de aluminio o la alúmina se utilizan frecuentemente para precipitar fosfatos de aluminio (AlPO4). La dosis requerida depende de la eficiencia de eliminación deseada, y la eficacia de la coagulación disminuye al bajar la concentración de fósforo. Dosis típicas para lograr un 80-90% de eliminación varían entre 50 y 200 mg/L. Altas dosis pueden afectar negativamente a la población bacteriana en sistemas de lodos activados.
- Hierro (Cloruro Férrico, FeCl3, o Sulfato Férrico, Fe2(SO4)3): Los iones de hierro se combinan para formar fosfato férrico (FePO4). Estos iones reaccionan lentamente con la alcalinidad, por lo que a menudo se añade un coagulante como la cal para elevar el pH y facilitar la coagulación.
La precipitación química puede lograr una alta eficiencia de eliminación de fósforo, a menudo superior al 90%, con concentraciones finales de P inferiores a 0.5 mg/L. Sin embargo, este método es costoso debido al consumo de productos químicos y aumenta el volumen de lodo generado hasta en un 40%.
Estrategias de Precipitación Química:
- Tratamiento Primario: La precipitación química se realiza antes de la decantación primaria, eliminando el fósforo eficazmente.
- Postprecipitación: Es un tratamiento estándar de efluentes secundarios, utilizando principalmente reactivos metálicos. Proporciona altas eficiencias de eliminación (hasta 95%) y mejora la eliminación de sólidos suspendidos. Las desventajas incluyen altos costos de planta y el riesgo de coloración residual por hierro.
- Coprecipitación: Los agentes químicos se añaden directamente en el tanque de aireación de plantas de lodos activados. Los costos de planta son más bajos, pero la eficiencia de eliminación es menor (por debajo del 85%), resultando en concentraciones de fósforo de aproximadamente 1 mg/L en el efluente final. Los lodos biológicos y químicos se mezclan, requiriendo mayor capacidad de sedimentación.
2. Eliminación Biológica Mejorada de Fósforo (EBPR)
Esta tecnología avanzada utiliza microorganismos específicos, conocidos como organismos acumuladores de fosfato (PAO, por sus siglas en inglés), que absorben y almacenan fósforo dentro de sus células. El proceso EBPR se basa en la alternancia de condiciones anaeróbicas y aeróbicas.
- Etapa Anaeróbica: En ausencia de oxígeno y nitratos, los PAO asimilan ácidos grasos volátiles (AGV) del agua residual, que actúan como fuente de carbono. Para realizar esta asimilación, los PAO hidrolizan sus reservas internas de polifosfatos, liberando ortofosfato al medio. La energía necesaria se obtiene de esta hidrólisis.
- Etapa Aeróbica: En presencia de oxígeno, los PAO degradan los compuestos orgánicos acumulados (como el polihidroxibutirato, PHB) para obtener energía para su crecimiento y mantenimiento celular. Parte de esta energía se utiliza para captar y almacenar el ortofosfato del medio en forma de polifosfatos.
Una vez que los PAO han acumulado una cantidad significativa de fósforo, la biomasa que los contiene se separa del agua tratada mediante la eliminación del lodo. La ventaja principal de EBPR es que no requiere productos químicos adicionales y puede integrarse en procesos de tratamiento biológico existentes, como los sistemas de lodos activados. Además, produce significativamente menos lodo que la precipitación química y evita la formación de precipitados que requieran filtración. La eficiencia de EBPR depende de la disponibilidad de materia orgánica fácilmente biodegradable (bsCOD) en el afluente y de condiciones operativas adecuadas, como el tiempo de retención y la temperatura. Los nitratos presentes en la etapa anaeróbica pueden ser perjudiciales para el proceso.

3. Tecnologías de Filtración por Membrana
La filtración por membrana emplea membranas semipermeables para separar físicamente el fósforo y otros contaminantes del agua.
- Microfiltración y Ultrafiltración: Eliminan sólidos suspendidos y algunas moléculas orgánicas disueltas más grandes.
- Nanofiltración y Ósmosis Inversa: Con tamaños de poro mucho más pequeños, estas membranas pueden eliminar sales disueltas, moléculas orgánicas e incluso iones monovalentes.
La filtración por membrana es un método eficaz para la eliminación de fósforo disuelto, ofreciendo alta eficiencia y calidad de efluente constante. Sin embargo, requiere una gestión cuidadosa del ensuciamiento de las membranas, un consumo de energía considerable y una inversión inicial elevada.
4. Reactores Aerobios de Lecho Fluidizado con Circulación Interna (RALFCI)
La investigación ha explorado el uso de reactores compactos y eficientes para la remoción de nutrientes. Los RALFCI, que utilizan una alta concentración de biomasa activa, han demostrado capacidad para remover materia orgánica y nitrógeno. Estudios han evaluado la eficiencia de remoción de fósforo reactivo y total en diferentes configuraciones de RALFCI, utilizando medios de soporte como arena y carbón activado granular. Estos reactores ofrecen una alternativa compacta y potencialmente eficiente para el tratamiento de aguas residuales domésticas y de sistemas acuícolas.
Tratamiento de Aguas por Método de Lodos Activados
Recuperación de Fósforo: Un Enfoque de Economía Circular
Dada la finitud de las reservas mundiales de roca fosfática y su importancia crítica para la seguridad alimentaria, la recuperación de fósforo de las aguas residuales se presenta como una solución sostenible y económicamente viable. Las plantas de tratamiento de aguas residuales pueden considerarse "minas líquidas" de fósforo, recuperando este valioso nutriente de las excreciones humanas, detergentes y fertilizantes.
El informe "Our Phosphorus Future" aboga por objetivos ambiciosos para 2050: una reducción del 50% en la contaminación mundial por fósforo y un aumento del 50% en el reciclaje del fósforo perdido en residuos y aguas residuales. El Programa de las Naciones Unidas para el Medio Ambiente (PNUMA) lidera la Alianza Mundial sobre la Gestión de Nutrientes, promoviendo estrategias para frenar la contaminación por fósforo sin comprometer la producción de alimentos.
La precipitación química de estruvita, un mineral que contiene fósforo, es un método bien establecido para la recuperación de fósforo, especialmente aplicado a lodos provenientes de digestión anaerobia. Sin embargo, para plantas que no incorporan digestión anaerobia, se exploran nuevos métodos. La investigación en la Universidad de Málaga, por ejemplo, se centra en la revalorización del fósforo contenido en las aguas residuales como fertilizante, fomentando la economía circular y reduciendo el impacto ambiental.
El Papel de la Normativa y la Innovación
La normativa ambiental, como la NOM-001-SEMARNAT-2021 en México, establece límites estrictos para la descarga de fósforo en cuerpos de agua. La Directiva Marco del Agua y la Directiva de Tratamiento de Aguas Residuales Urbanas de la Unión Europea también imponen valores máximos de concentración de fósforo en los efluentes. El cumplimiento de estas normativas representa un desafío para las EDAR, impulsando la innovación en tecnologías de tratamiento y recuperación.
La medición precisa del fósforo en las aguas residuales es fundamental para la gestión del agua, el cumplimiento normativo y la protección de los ecosistemas. Existen diversos métodos analíticos, desde pruebas colorimétricas hasta equipos de laboratorio de alta precisión, para cuantificar las diferentes formas de fósforo (ortofosfato, polifosfatos, fósforo orgánico y fósforo total).
La innovación continua en las tecnologías de medición y tratamiento del fósforo será crucial para la sostenibilidad hídrica futura, permitiendo no solo mitigar los impactos negativos de la contaminación por fósforo, sino también aprovechar este recurso vital de manera más eficiente y responsable.