El cloruro de aluminio (AlCl3) y el hipoclorito de sodio (NaClO) son dos compuestos químicos con propiedades y aplicaciones diversas, cuyas interacciones y comportamientos son de gran interés en distintos ámbitos industriales y de tratamiento de aguas. Si bien a primera vista pueden parecer dispares, su estudio conjunto revela complejidades químicas y sinergias potenciales, así como incompatibilidades que son cruciales de comprender para su manejo seguro y eficiente.
Cloruro de Aluminio: Un Compuesto Anfotérico y Reactivo
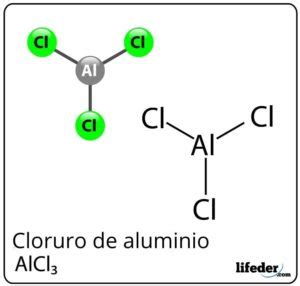
El cloruro de aluminio es un compuesto formado por aluminio y cloro. Una de sus características notables es que, a pesar de estar compuesto por un metal y un no metal, presenta un enlace covalente. Este sólido posee un bajo punto de fusión y ebullición, y su sublimación ocurre a 178 °C. A diferencia de muchos haluros iónicos como el cloruro de sodio, el AlCl3 fundido es un mal conductor de la electricidad.
Una propiedad fundamental del cloruro de aluminio es su naturaleza anfótera, lo que significa que exhibe propiedades tanto ácidas como básicas. Puede actuar como un ácido de Lewis o como una base de Lewis. Al disolverse en agua destilada, el AlCl3 se disocia en cationes aluminio (Al3+) y aniones cloruro (Cl-).
La reacción entre el aluminio elemental (Al) y el cloro (Cl2) es un proceso altamente exotérmico, liberando una cantidad considerable de energía en forma de calor y luz. Durante esta reacción, los enlaces Al-Cl en el cloruro de aluminio son significativamente más fuertes y estables que los enlaces originales en las moléculas de cloro y el metal de aluminio. La energía previamente almacenada en los reactivos se libera a medida que se forman estos nuevos enlaces estables. Una vez iniciada, la reacción, por ejemplo, mediante una chispa o el contacto con cloro gaseoso, el calor generado puede ser suficiente para mantenerla y acelerar la formación de AlCl3. Estas reacciones son frecuentemente empleadas en demostraciones químicas para ilustrar la síntesis y la alta reactividad del aluminio con los halógenos.
El aluminio, un metal blanco ligero y plateado, es muy abundante en la corteza terrestre y se utiliza ampliamente en diversas industrias debido a su excelente relación resistencia-peso y su resistencia a la corrosión. El cloro, por otro lado, es un gas altamente reactivo de color amarillo verdoso con un olor penetrante e irritante. Cuando el aluminio entra en contacto con el cloro, se produce una reacción química en la que cada átomo de aluminio pierde sus tres electrones de valencia, los cuales son absorbidos por los átomos de cloro. Cada átomo de cloro necesita un electrón para completar su octeto, alcanzando una configuración electrónica estable.
El cloruro de aluminio resultante es un sólido blanco o amarillento a temperatura ambiente. Es muy soluble en agua, y al disolverse, se hidroliza, reaccionando con las moléculas de agua para producir hidróxido de aluminio y ácido clorhídrico. Esta reacción es importante industrialmente, ya que el cloruro de aluminio se utiliza como catalizador en numerosas reacciones químicas, especialmente en la producción de compuestos orgánicos, como en las reacciones de Friedel-Crafts, fundamentales para la síntesis de compuestos aromáticos.
Corrosión del Aluminio y sus Aleaciones en Ambientes Marinos
El aluminio y sus aleaciones son susceptibles a la corrosión, especialmente en ambientes marinos. El estudio de las formas de corrosión que pueden presentarse en aleaciones de extrusión y laminación (familias 1000, 3000, 5000 y 6000) y aleaciones de moldeo con silicio o magnesio en el ambiente marino es de gran relevancia.
Corrosión Uniforme: Este tipo de corrosión se manifiesta como una disminución regular y uniforme del espesor del metal en toda su superficie. La velocidad de disolución puede variar enormemente, desde unas pocas micras por año en medios no agresivos hasta muchas micras por hora en soluciones ácidas o básicas. Sin embargo, en el ambiente marino, ya sea por inmersión o por la atmósfera marina, la corrosión uniforme es ínfima y, en general, no medible.
Corrosión por Picaduras: Es una forma de corrosión localizada, común en muchos metales. Consiste en la formación de cavidades en el metal, cuya geometría depende de factores inherentes al metal (aleación, condiciones de fabricación) y al medio (concentración de sales minerales). El aluminio es sensible a la corrosión por picaduras en medios con pH cercano a la neutralidad, como las aguas superficiales, el agua de mar o la humedad del aire. A diferencia de otros metales, las picaduras de corrosión en el aluminio suelen estar recubiertas por voluminosas pústulas blancas de alúmina hidratada gelatinosa (Al(OH)3), cuyo volumen es mayor que el de la cavidad subyacente.
La corrosión por picaduras se inicia en sitios donde la capa de óxido natural del aluminio presenta defectos, como reducciones de espesor, roturas o lagunas, provocados por condiciones de procesamiento, manipulación defectuosa o elementos de aleación. Las zonas lijadas, rayadas o sometidas a operaciones de calderería, plegado o soldadura son puntos propensos al desarrollo de picaduras, especialmente durante las primeras semanas de inmersión en agua de mar.
La velocidad de penetración de estas picaduras es un factor crucial. A diferencia del zinc, cuyos productos de corrosión son solubles, la alúmina hidratada (Al(OH)3) es insoluble en agua. Una vez formados, los productos de corrosión permanecen adheridos al metal dentro de las cavidades, frenando significativamente el intercambio entre el agua de mar o la humedad del aire y el metal. Por ello, la velocidad de corrosión por picaduras del aluminio y sus aleaciones disminuye rápidamente en la mayoría de los medios, incluso en el agua de mar. Estudios demuestran que la velocidad de ataque de las picaduras está ligada al tiempo por una relación del tipo V = Kt1/3. La amplia experiencia en el uso de aluminio sin protección en construcciones costeras (techos, cubiertas) y en la construcción naval confirma que la profundidad de las picaduras, una vez formadas en los primeros meses, tiende a estabilizarse y no evoluciona significativamente. Esta ralentización explica la durabilidad del aluminio en algunos medios naturales sin necesidad de protección durante décadas. La corrosión por picaduras ocurre tanto en atmósfera marina como en inmersión en agua de mar.

Hipoclorito de Sodio en el Tratamiento de Aguas
El hipoclorito de sodio (NaClO) es un compuesto químico con un gran poder oxidante, fundamental en una amplia gama de procesos de desinfección. Sus propiedades desinfectantes se deben a su capacidad para destruir la estructura celular de los microorganismos. La acción desinfectante se basa en la liberación de cloro, un potente oxidante que reacciona con componentes celulares esenciales de los microorganismos, interrumpiendo sus funciones vitales y provocando su muerte.
La eficacia y el comportamiento del hipoclorito de sodio dependen del pH de la solución. En aguas con un pH entre 6.5 y 8.5, ambas especies (ácido hipocloroso y ion hipoclorito) se encuentran en equilibrio. Por debajo de un pH de 5, todo el cloro está presente en forma de ácido hipocloroso (HClO), que es un poderoso agente oxidante y desinfectante, pero de baja estabilidad.
En la industria alimentaria, el hipoclorito de sodio se emplea extensivamente para la desinfección de equipos, instalaciones y superficies (biocida PT4), así como para la potabilización del agua (biocida PT5). Los productos desinfectantes basados en hipoclorito de sodio requieren autorización como biocidas, según el tipo de aplicación (PT). En España, la normativa establecida por el Real Decreto 3349/1983 sobre plaguicidas y el Real Decreto 3360/1983 sobre lejías sigue vigente durante el periodo transitorio.
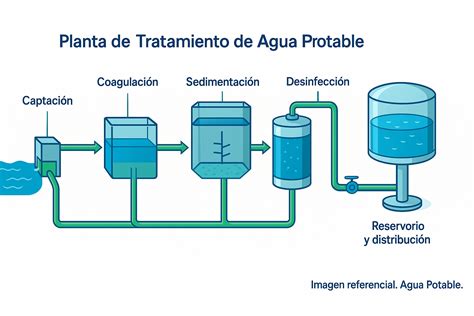
Un estudio observacional y cualitativo realizado en la Planta de Tratamiento de Agua Potable (PTAP) Quequeña - Arequipa buscó potabilizar agua para consumo humano utilizando hipoclorito de calcio y sulfato de aluminio. Se tomaron muestras de 24 litros de agua superficial, tratadas mediante goteo con hipoclorito de sodio y sulfato de aluminio en dosis de 3 ppm (0.12 g/L), 5 ppm (0.2 g/L) y 7 ppm (0.3 g/L). Cada tratamiento contó con tres repeticiones, vertidas en peceras de 10 litros para lograr una desinfección eficiente. Las concentraciones se aplicaron cada 10 días para ambos tratamientos. Los resultados, analizados mediante la prueba Tukey, fueron significativos.
Incompatibilidades Químicas y Consideraciones de Seguridad
La manipulación segura de productos químicos requiere un conocimiento profundo de sus incompatibilidades. El hipoclorito de sodio, por su naturaleza oxidante, presenta incompatibilidades con una amplia gama de sustancias.
En el contexto del tratamiento de aguas, la combinación de hipoclorito de sodio y sulfato de aluminio es común. El sulfato de aluminio, un coagulante, ayuda a agrupar las partículas suspendidas en el agua, facilitando su posterior eliminación. El hipoclorito de sodio, como desinfectante, elimina los microorganismos patógenos. La dosificación controlada de ambos es clave para la potabilización.
Sin embargo, es crucial tener en cuenta las incompatibilidades generales de compuestos relacionados. Por ejemplo, el 1,1,1-tricloroetano es incompatible con bases fuertes, aluminio, oxidantes fuertes, magnesio, sodio, potasio, luz ultravioleta, calor, acetona, óxidos de nitrógeno y metales pulverulentos. El cloro reacciona con muchos compuestos orgánicos, amoníaco y partículas metálicas, presentando riesgo de incendio y explosión.
El cloruro de aluminio, por su parte, también tiene incompatibilidades. Por ejemplo, el diclorometano es incompatible con metales alcalinos y alcalinotérreos, metales en polvo, óxidos de nitrógeno, alcoholatos, amidas alcalinas, ácido perclórico, nítrico, óxidos no metálicos, oxígenos, alcoholes, hidrocarburos aromáticos, agua/KMnO, hidrocarburos aromáticos/ácidos, oxidantes fuertes, metanol, aluminio, ácido nítrico y bases fuertes.
La información sobre incompatibilidades químicas, como la proporcionada en listados de seguridad, es orientativa y puede estar incompleta. Es imperativo contrastar siempre los datos de seguridad con la ficha de datos de seguridad específica del producto que se esté utilizando.
Reacción de ácido clorhídrico y aluminio | Experimento de Química
La comprensión detallada de las propiedades del cloruro de aluminio y del hipoclorito de sodio, sus reacciones químicas, su comportamiento en diferentes entornos y sus incompatibilidades es esencial para su aplicación segura y eficaz en la industria, el tratamiento de aguas y la investigación.
tags: #hipoclorito #de #sodio #aluminio