El hipoclorito de sodio (NaOCl), comúnmente conocido como lejía o cloro, es un compuesto químico omnipresente en nuestro día a día, actuando como un pilar fundamental en la limpieza, desinfección y diversos procesos industriales. Su aparente simplicidad esconde una química compleja y un potencial considerable, que abarca desde la eliminación de gérmenes hasta aplicaciones en la industria textil y el tratamiento de aguas. A pesar de su eficacia, es crucial comprender sus propiedades para garantizar un uso seguro y responsable.
Naturaleza Química y Mecanismo de Acción
El hipoclorito de sodio es una sal de hipoclorito, fácilmente soluble en agua. Al hidrolizarse en solución acuosa, genera dos sustancias de vital importancia: el ácido hipocloroso (HOCl) y el hidróxido de sodio (NaOH). Es el ácido hipocloroso el principal responsable de las potentes propiedades desinfectantes del hipoclorito de sodio. Actúa como un agente biocida que destruye la estructura celular de microorganismos, interrumpiendo sus funciones vitales y provocando su muerte. Esta acción se debe a su gran capacidad oxidante, liberando cloro en un estado de oxidación +1 que reacciona enérgicamente con los componentes celulares esenciales de los patógenos.
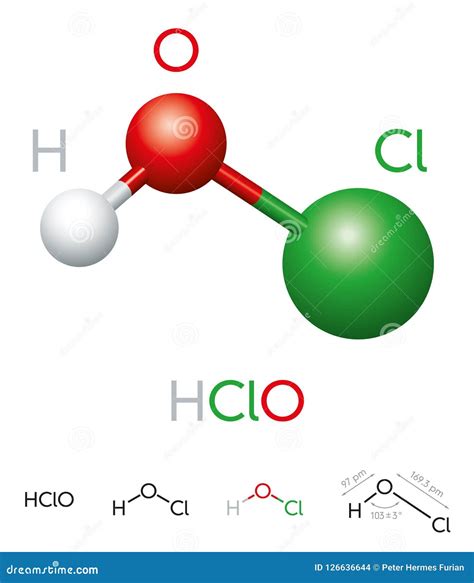
La proporción entre el ácido hipocloroso (HOCl) y el ion hipoclorito (OCl⁻) en una solución acuosa depende en gran medida del valor del pH. En un rango de pH entre 6,5 y 8,5, ambas especies se encuentran en equilibrio. Sin embargo, si el pH desciende por debajo de 5, todo el cloro se presenta en forma de ácido hipocloroso, que es un agente oxidante y desinfectante de gran poder, pero de baja estabilidad. Por el contrario, a medida que el pH aumenta, la concentración de ion hipoclorito (OCl⁻) se incrementa, y aunque sigue siendo un agente desinfectante, su eficacia disminuye en comparación con el HOCl. La presencia de hidróxido de sodio (NaOH) en la solución, producto de la hidrólisis, tiende a elevar el pH, haciendo que las soluciones de hipoclorito de sodio sean inherentemente alcalinas, con un pH que puede oscilar entre 9 y 14.
El Hipoclorito de Sodio en el Cuerpo Humano y en la Industria
Curiosamente, el mecanismo oxidante del ácido hipocloroso no es exclusivo de las aplicaciones industriales. En el cuerpo humano, el ácido hipocloroso se produce de forma natural dentro del fagosoma de células inmunitarias como los neutrófilos, macrófagos y células de Von Kupffer. Esta generación endógena es parte de la respuesta inmunitaria innata del organismo, utilizada para destruir microorganismos patógenos fagocitados.
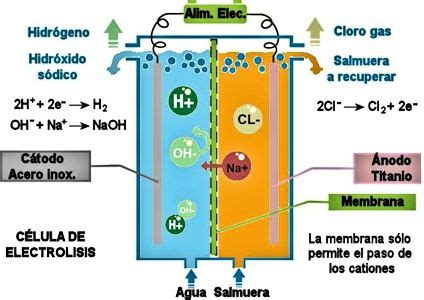
Artificialmente, la producción de hipoclorito de sodio puede lograrse mediante diversos métodos. La Activación Electro-Química (ECA) es una técnica que utiliza agua, sal y electricidad para generar este compuesto. Otros métodos industriales incluyen la electrólisis de soluciones salinas y la cloración de sosa cáustica. La electrólisis de una solución de cloruro de sodio produce hidróxido de sodio y cloro, los cuales reaccionan posteriormente para formar hipoclorito de sodio y cloruro de sodio. Alternativamente, el burbujeo de gas cloro en una solución de hidróxido de sodio (sosa cáustica) también genera hipoclorito de sodio.
Aplicaciones Diversas y Específicas
El hipoclorito de sodio es un compuesto versátil con una amplia gama de aplicaciones:
- Desinfección y Blanqueo Doméstico: Es el ingrediente principal de la lejía o lavandina, utilizada para desinfectar superficies, eliminar manchas y blanquear tejidos. Su capacidad para descomponer moléculas orgánicas, incluyendo los cromóforos responsables del color, lo convierte en un potente agente blanqueador.
- Tratamiento de Aguas: A gran escala, se emplea en la potabilización de agua y el tratamiento de aguas residuales. En dosis controladas (partes por millón - PPM), oxida contaminantes sin alterar significativamente el sabor ni el olor del agua. Es efectivo contra bacterias, virus, algas y otros microorganismos.
- Industria Alimentaria: Se utiliza para la desinfección de equipos, instalaciones y superficies en la industria alimentaria (biocida PT4), garantizando la seguridad microbiológica de los productos.
- Industria Textil y Papelera: Su poder blanqueador es fundamental en los procesos de producción de textiles y papel.
- Sanidad y Hospitales: Se emplea para la desinfección de superficies y equipos en hospitales e instalaciones sanitarias, ayudando a prevenir la propagación de infecciones.
- Piscinas: Es un desinfectante común en el mantenimiento de piscinas, ya sea en forma líquida, pastillas o polvo, o a través de sistemas de electrólisis salina. Su acción ayuda a eliminar algas, bacterias y previene la formación de biofilm, incluso siendo efectivo contra la bacteria Legionela.

Estabilidad, Incompatibilidades y Riesgos
A pesar de su utilidad, el hipoclorito de sodio no está exento de desafíos. Su estabilidad es un factor crítico. En disolución acuosa, es más estable a bajas temperaturas (entre 15-25 °C), especialmente en soluciones diluidas. Sin embargo, se descompone con el tiempo, la exposición a la luz (particularmente la luz ultravioleta) y el calor. Temperaturas elevadas, especialmente alrededor de los 70 °C, pueden acelerar drásticamente su descomposición, generando especies reactivas de oxígeno y provocando una descomposición potencialmente explosiva.
La presencia de ciertas impurezas, como algunos metales, también puede acelerar su descomposición. Por ello, el almacenamiento y transporte adecuados son esenciales. Debe guardarse alejado de la luz solar directa, fuentes de calor y, fundamentalmente, separado de otras sustancias químicas.
Las incompatibilidades del hipoclorito de sodio son notables y presentan riesgos significativos:
- Ácidos: Al entrar en contacto con ácidos, incluso diluidos, el hipoclorito de sodio libera gas cloro (Cl₂), un gas altamente tóxico, asfixiante y corrosivo. La reacción con ácidos concentrados puede ser aún más violenta. Por ello, está estrictamente prohibido mezclar lejía con ácidos como el vinagre o ciertos limpiadores de baño.
- Amoniaco y Aminas: La mezcla con amoniaco o aminas forma cloraminas, compuestos que son generalmente tóxicos y, en algunos casos, explosivos. Esta es la razón por la que nunca se debe mezclar lejía con productos que contengan amoniaco.
- Compuestos Combustibles y Reductores: Como agente oxidante fuerte, el hipoclorito de sodio puede reaccionar vigorosamente con materiales combustibles y reductores.
Productos de limpieza e intoxicaciones
Peligros para la Salud y Precauciones de Seguridad
El hipoclorito de sodio es un compuesto corrosivo y debe manipularse con extrema precaución.
- Contacto con la Piel y Ojos: El contacto directo puede causar irritación severa, enrojecimiento y quemaduras químicas. En los ojos, puede provocar daños graves, incluyendo pérdida de visión. En caso de contacto, es fundamental lavar la zona afectada de inmediato con abundante agua corriente durante al menos 20 minutos y buscar atención médica.
- Inhalación: La inhalación de vapores puede irritar las vías respiratorias, provocando tos, dolor de garganta y dificultad para respirar. En concentraciones elevadas o en espacios mal ventilados, puede causar daños pulmonares graves. Si se inhala, se debe trasladar a la persona a un lugar con aire fresco y buscar asistencia médica.
- Ingestión: La ingestión es peligrosa y puede causar quemaduras en la boca, garganta y tracto digestivo, además de náuseas, vómitos y dolor abdominal. No se debe inducir el vómito. Se recomienda beber agua tibia y buscar atención médica de inmediato.
Para un manejo seguro, se deben seguir rigurosas precauciones:
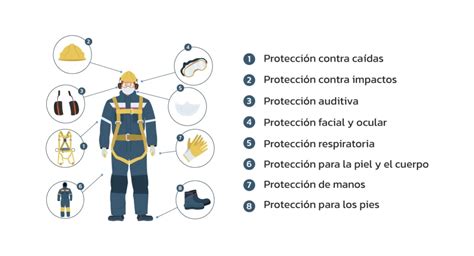
- Equipo de Protección Personal (EPP): Utilizar guantes resistentes a productos químicos (nitrilo o neopreno), gafas de seguridad química y, en caso de trabajar con concentraciones elevadas, una pantalla facial y ropa protectora.
- Ventilación: Asegurar una ventilación adecuada del área de trabajo abriendo ventanas o utilizando extractores de aire.
- Dilución: Seguir las instrucciones de dilución recomendadas. Generalmente, se recomienda mezclar una parte de lejía con nueve partes de agua para limpieza general. Es importante verter la lejía en el agua, y no al revés, para evitar salpicaduras.
- Almacenamiento: Guardar el hipoclorito de sodio en su envase original, bien cerrado, en un lugar fresco, seco y alejado de la luz solar directa, calor y sustancias incompatibles. Mantener fuera del alcance de niños y mascotas.
- Manipulación: Evitar el contacto con la piel, ojos y ropa. No fumar, comer ni beber en el área de trabajo. Lavarse las manos a fondo después de su manipulación.
Marco Normativo
El uso de productos desinfectantes basados en hipoclorito de sodio está regulado y debe contar con la autorización correspondiente como biocida, según el tipo de aplicación (PT). En España, por ejemplo, durante ciertos periodos transitorios, se han mantenido marcos normativos establecidos por reales decretos específicos para plaguicidas y lejías. La Agencia Internacional para la Investigación del Cáncer de la Organización Mundial de la Salud ha incluido los hipocloritos en la lista de carcinógenos del grupo 3, lo que indica que no hay evidencia suficiente para clasificarlos como carcinógenos para los humanos.
En conclusión, el hipoclorito de sodio es un compuesto químico de gran valor por sus propiedades desinfectantes y blanqueadoras. Sin embargo, su naturaleza corrosiva y sus incompatibilidades exigen un conocimiento profundo de sus características y la estricta observancia de las medidas de seguridad para garantizar su uso eficaz y, sobre todo, seguro.
tags: #hipoclorito #de #sodio #base