El nivel de pH es un indicador fundamental de la calidad y seguridad del agua, midiendo su grado de acidez o alcalinidad en una escala que va del 0 al 14. Un valor de 7 se considera neutro, mientras que valores superiores indican alcalinidad y menores indican acidez. El agua destilada, un producto de alta pureza obtenido mediante un riguroso proceso de destilación, se encuentra en la intersección de esta escala, presentando características únicas que la hacen indispensable en diversas aplicaciones.
Comprendiendo el pH: La Ciencia Detrás de la Medida
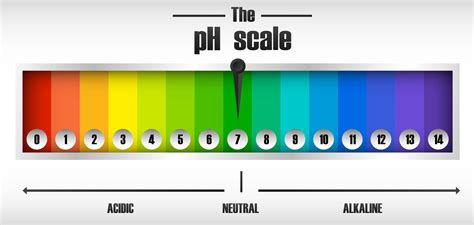
La escala de pH, un concepto científico esencial, cuantifica la concentración de iones de hidrógeno (H+) e hidróxido (OH-) en una solución acuosa. Los ácidos, al liberar iones H+, disminuyen el pH, mientras que las bases, al liberar iones OH-, lo incrementan. Esta escala logarítmica significa que cada cambio unitario en el pH representa una variación de diez veces en la acidez o alcalinidad, subrayando la importancia de incluso las pequeñas diferencias.
La medición del pH se puede realizar mediante métodos variados, desde las sencillas tiras reactivas que ofrecen una estimación aproximada, hasta los precisos medidores electrónicos de pH. Los indicadores de pH, que cambian de color en función del nivel de acidez o alcalinidad, también proporcionan una forma visual de determinar el pH.
Monitorear el nivel de pH del agua destilada es crucial para garantizar su calidad y adecuación a usos específicos. Niveles de pH extremos, ya sean muy altos o muy bajos, pueden hacer que el agua sea insegura para el consumo humano o inadecuada para aplicaciones científicas e industriales que exigen un control preciso.
El pH del Agua Destilada: Una Inmersión Profunda
En teoría, el agua destilada pura debería exhibir un pH perfectamente neutro de 7.0. El proceso de destilación, al eliminar todos los solutos, minerales e iones, elimina las sustancias que podrían alterar el pH. En su estado más puro, sin la adición de iones de hidrógeno o hidróxido, el agua destilada no favorece ni a los ácidos ni a las bases, manteniéndose en un estado neutro.
Sin embargo, el agua recién destilada, al entrar en contacto con el aire, tiende a absorber dióxido de carbono atmosférico. Este gas se disuelve formando ácido carbónico, lo que libera iones de hidrógeno y reduce ligeramente el pH. Por esta razón, la mayoría del agua destilada inmediatamente después de la destilación presenta un pH cercano a 5.8. Es importante contrastar esto con el agua alcalina, que a menudo mide entre 8 y 9 en la escala de pH debido a la adición intencionada de minerales como calcio y magnesio para aumentar su alcalinidad.
A pesar de esta ligera desviación del 7.0, el agua destilada se mantiene mucho más cerca de un pH neutro ideal que la mayoría de las fuentes de agua naturales y tratadas. Esta característica la convierte en una opción deseable para aplicaciones donde se requiere un pH neutro.
Varios factores pueden alterar o desviar el nivel de pH del agua destilada de su punto neutro teórico:
- Exposición al aire: La absorción continua de dióxido de carbono de la atmósfera reduce gradualmente el pH con el tiempo después de la destilación.
- Interacciones con el material del recipiente: Ciertos materiales de los recipientes, como el vidrio, pueden lixiviar iones al agua, modificando su pH de forma gradual, ya sea hacia arriba o hacia abajo.
- Adición de solutos o sustancias: Cualquier ion, ácido, base u otro soluto adicional introducido afectará el pH en consecuencia.
Por lo tanto, se requiere una manipulación y almacenamiento cuidadosos del agua destilada para mantener su pH neutro y su frescura, especialmente para aplicaciones científicas y médicas críticas. Las pruebas y regulaciones frecuentes del pH son clave para asegurar su idoneidad. Los recipientes de almacenamiento deben ser químicamente inertes, mantenerse sellados y el agua debe conservarse en un lugar fresco.
El pH objetivo para el agua destilada varía según su uso previsto. Para el consumo general, se recomienda un pH entre 6.5 y 7.5. Sin embargo, los experimentos de laboratorio sensibles pueden requerir un control más estricto, a menudo alrededor de 7.0 ±0.2, para cumplir con los estándares metodológicos. Comprender las necesidades específicas de pH es vital al trabajar con agua destilada.
El Impacto del pH en la Salud y el Uso: Por Qué es Importante
El pH del agua influye significativamente en sus diversas aplicaciones, desde el consumo y la cocina hasta experimentos científicos, aplicaciones médicas y procesos industriales. Mantener un equilibrio de pH adecuado es crucial en todos estos ámbitos.
Para la salud general, el agua potable debe tener un pH que oscile entre 6.5 y 8.5. Niveles de pH excesivamente bajos o altos pueden dañar las células y los órganos con el tiempo. La mayoría de las aguas embotelladas se encuentran dentro de un rango de pH seguro, pero siempre es prudente realizar pruebas, especialmente para el consumo a largo plazo.
En la cocina, el pH del agua puede alterar las texturas y los sabores de los alimentos. El agua ácida puede impartir un sabor picante a los alimentos, mientras que el agua alcalina tiende a suavizar las preparaciones. El pH ideal dependerá del tipo de alimento que se esté cocinando.
En el ámbito científico y médico, el pH neutro del agua destilada la convierte en un recurso invaluable. Las reacciones químicas sensibles requieren un pH controlado, a menudo alrededor de 7, para desarrollarse correctamente. El uso de agua destilada asegura que los experimentos comiencen desde una línea de base neutral, minimizando variables.
En la industria farmacéutica, el agua destilada se utiliza para ajustar el pH en medicamentos líquidos e inyecciones. Su pureza evita la contaminación y asegura que el pH preciso sea fundamental para la administración eficaz de fármacos en el cuerpo.
En la industria cosmética y del cuidado de la piel, el agua destilada, al carecer de minerales, es menos probable que irrite la piel sensible. Su pH limpio proporciona estabilidad a los ingredientes del producto, como conservantes y vitaminas.
En contextos industriales, como en calderas y torres de enfriamiento, el control del pH del agua es esencial para prevenir la corrosión de metales y la acumulación de incrustaciones. El pH predecible del agua destilada ayuda a reducir el daño a los equipos.
Por lo tanto, desde el consumo diario hasta los laboratorios de química, el nivel de pH del agua destilada juega un papel importante. Aunque rara vez es exactamente 7.0, su rango de pH casi neutro le permite mantener de manera única la pureza y la consistencia en una amplia gama de aplicaciones exigentes. Monitorear y gestionar el pH es fundamental para optimizar los resultados en cada uno de estos campos.
El Destilador de Agua VEVOR: Garantizando Niveles Óptimos de pH
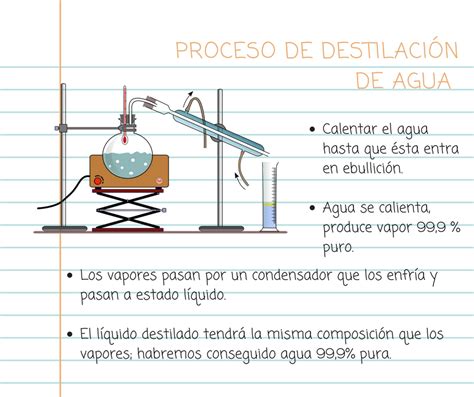
El Destilador de Agua VEVOR emplea un eficiente proceso de destilación por vapor para producir agua destilada fresca con un pH neutro ideal. Este proceso hierve el agua del grifo, convirtiéndola en vapor que asciende y pasa a través de un serpentín condensador. El agua destilada pura condensada gotea, dejando atrás impurezas insolubles y sólidos disueltos.
Este método elimina todos los iones y minerales que podrían alterar el pH. El agua recién destilada resultante presenta un pH neutro de alrededor de 5.8, caracterizándose por ser segura y energéticamente eficiente. Para laboratorios, centros médicos y empresas que requieren agua destilada con un pH controlado, el Destilador de Agua VEVOR se presenta como una solución excelente.
Destilador de agua
Preguntas Frecuentes: Abordando Consultas Comunes sobre el pH y el Agua Destilada
¿Qué pH tiene el agua destilada?El pH del agua recién destilada es cercano a neutro, alrededor de 5.8. Puede oscilar entre 5.7 y 7 después de absorber dióxido de carbono atmosférico.
¿El agua destilada es ácida o alcalina?El agua destilada no es ni ácida ni alcalina. Al carecer de iones añadidos, permanece neutra y no favorece a los ácidos ni a las bases.
¿Cómo se compara el pH del agua destilada con el del agua del grifo?El agua del grifo tiende a ser ligeramente ácida o alcalina, con un pH que generalmente oscila entre 6.5 y 8.5. El agua destilada está más cerca de un pH neutro de 7.
¿Por qué es importante el pH del agua destilada?El control preciso del pH es fundamental para aplicaciones médicas, científicas e industriales que dependen de la pureza del agua destilada.
¿Qué factores afectan el equilibrio del pH del agua destilada?La exposición al aire, la temperatura de almacenamiento, el material del recipiente de agua y cualquier soluto agregado pueden alterar el pH con el tiempo.
¿Cómo puedo bajar o aumentar el pH de mi agua destilada?Puede ajustar el pH utilizando soluciones ácidas o básicas diluidas. Sin embargo, esto afectará la pureza, por lo que se deben tomar precauciones.
¿Cuál es el rango de pH ideal para beber agua destilada?Para beber, se recomienda un pH entre 6.5 y 7.5 para asegurar la salud y una hidratación adecuada.
Palabras Finales: El Papel Crucial del Agua Destilada y su pH
Comprender el pH del agua destilada es esencial para aquellos que dependen de su pureza y neutralidad. Aunque teóricamente es 7.0, su pH real, tras la absorción de dióxido de carbono atmosférico, se sitúa entre 5.7 y 7. Este pH, ligeramente ácido pero cercano a la neutralidad, hace que el agua destilada sea ideal para experimentos científicos, aplicaciones médicas y otros usos sensibles donde el control preciso del pH es primordial. Desde mantener la consistencia en pruebas de laboratorio hasta asegurar la seguridad de las inyecciones, monitorear y gestionar el equilibrio del pH del agua destilada es clave.
El agua destilada desempeña un papel fundamental en la investigación médica y científica, así como en aplicaciones industriales. Investigar su valor de pH es crucial tanto para el avance científico como para la optimización de procesos industriales.
El agua destilada suele ser ligeramente ácida, con un rango de pH de aproximadamente 5.0 a 6.5. Esto se debe a su capacidad para absorber dióxido de carbono (CO₂) del aire, formando ácido carbónico débil. Generalmente es segura para el consumo humano y el uso industrial a corto plazo, pero no es naturalmente alcalina.
Su característica principal es su altísima pureza, pero también es químicamente inestable, lo que la hace adecuada para aplicaciones muy sensibles a los contaminantes, como las médicas, de laboratorio y farmacéuticas. Es importante destacar que el agua destilada es propensa a la contaminación durante el almacenamiento y su pH puede fluctuar fácilmente.
En el ámbito de la calidad del agua, el pH es un indicador clave. Según las Normas de Agua Potable de la Organización Mundial de la Salud (OMS) y la Agencia de Protección Ambiental de los Estados Unidos (EPA), el rango de pH recomendado para el agua potable es de 6.5 a 8.5. Un pH inferior a 6.5 puede hacer que el agua sea ácida y corrosiva, aumentando el riesgo de disolución de metales pesados y poniendo en peligro la salud humana. Un pH superior a 8.5 puede hacer que el agua sea alcalina, afectar su sabor y causar molestias gastrointestinales.
Medir el pH del agua destilada presenta desafíos debido a su conductividad extremadamente baja, lo que puede generar lecturas inestables. Para garantizar resultados precisos, se deben utilizar electrodos de pH especializados y realizar mediciones en un entorno controlado para minimizar la absorción de CO₂ atmosférico.
En resumen, la elección entre agua destilada y agua alcalina depende de las necesidades específicas. Mientras que el agua destilada se prefiere por su pureza y neutralidad en aplicaciones científicas y médicas, el agua alcalina se consume a menudo por sus supuestos beneficios para la salud o por su sabor. La comprensión del pH y su impacto es fundamental para tomar decisiones informadas sobre el uso del agua en diversas facetas de la vida.