El hipoclorito de sodio (NaOCl) es un compuesto químico versátil y potente, ampliamente reconocido por sus propiedades desinfectantes y blanqueadoras. Su uso se extiende desde aplicaciones domésticas hasta procesos industriales a gran escala, siendo un pilar fundamental en el tratamiento de aguas y la limpieza. La eficacia y seguridad de este compuesto dependen en gran medida de su concentración, un factor clave que determina su idoneidad para diversas aplicaciones.
Orígenes Históricos y Descubrimiento
El descubrimiento del hipoclorito de sodio está intrínsecamente ligado al hallazgo del cloro. Alrededor del año 1785, el químico francés Claude Louis Berthollet desarrolló líquidos blanqueantes utilizando hipoclorito de sodio. La compañía Javel, introdujo este producto en el mercado bajo el nombre de "licor de Javel", encontrando su aplicación inicial en el blanqueo de algodón. La capacidad del hipoclorito para eliminar manchas a temperatura ambiente facilitó su rápida adopción. En Francia, el hipoclorito de sodio aún es conocido como 'eau de Javel', un testimonio de sus orígenes históricos. Posteriormente, en 1799, Charles Tennant patentó un método para fabricar hipoclorito de calcio, haciendo reaccionar cloro con hidróxido de calcio, y estableció una fábrica en St. para su producción masiva.
Características y Propiedades del Hipoclorito de Sodio
El hipoclorito de sodio se presenta típicamente como una solución acuosa de color amarillo claro y un olor característico a cloro. Su densidad relativa para una solución al 5,5% es de aproximadamente 1,1. La concentración de hipoclorito de sodio en productos de uso doméstico suele rondar el 5%, con un pH de alrededor de 11, lo que lo hace irritante. Las soluciones de mayor concentración, entre el 10% y el 15%, presentan un pH cercano a 13, volviéndose corrosivas y capaces de causar quemaduras.
Es fundamental comprender que el hipoclorito de sodio es una sustancia inestable. El cloro activo puede evaporarse de la solución a razón de aproximadamente 0,75 gramos por día. El calentamiento acelera su descomposición, al igual que el contacto con ácidos, la luz solar directa, ciertos metales y gases corrosivos, incluido el gas de cloro. Como agente oxidante fuerte, reacciona vigorosamente con compuestos combustibles y reductores. Su naturaleza básica débil también requiere precauciones durante su transporte, almacenamiento y manipulación.
La Influencia del pH en la Desinfección
La presencia de hidróxido de sodio (soda cáustica) en las formulaciones de hipoclorito de sodio eleva el pH del agua al disolverse. En solución acuosa, el hipoclorito de sodio genera dos especies químicas con actividad desinfectante: el ácido hipocloroso (HOCl) y el ion hipoclorito (OCl-), siendo el primero considerablemente más activo. El pH del medio determina la proporción de ácido hipocloroso formada; a mayor acidez, mayor concentración de HOCl y, por ende, mayor poder desinfectante. Para ajustar el pH y optimizar la desinfección, se suele emplear ácido acético. Una alternativa es el ácido sulfúrico, que produce menos gases dañinos, aunque su naturaleza fuerte y corrosiva exige precauciones adicionales.
Métodos de Producción del Hipoclorito de Sodio
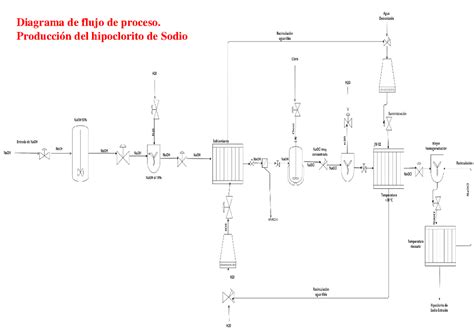
Existen dos métodos principales para la producción de hipoclorito de sodio:
- Electrólisis de Soluciones Salinas: Se disuelve cloruro de sodio (sal común) en agua blanda para generar una solución salina. Esta solución es luego sometida a electrólisis, produciendo hipoclorito de sodio en agua. Este proceso puede generar soluciones con hasta 150 gramos de cloro activo por litro. Un subproducto de esta reacción es el gas hidrógeno, que es explosivo y requiere ventilación adecuada.
- Reacción de Cloro Gaseoso con Soda Cáustica: Se hace pasar cloro gaseoso (Cl2) a través de una solución de hidróxido de sodio (NaOH). La reacción química resultante produce hipoclorito de sodio, cloruro de sodio y agua:Cl2 + 2NaOH → NaOCl + NaCl + H2O
Aplicaciones Industriales y Comerciales
La versatilidad del hipoclorito de sodio se refleja en su amplia gama de aplicaciones industriales y comerciales:
Tratamiento de Agua Potable y Residual
Las plantas potabilizadoras, como las de Monterrey, utilizan hipoclorito de sodio industrial para eliminar bacterias patógenas como E. coli y diversos virus, garantizando la seguridad del agua de consumo. En el ámbito industrial, se aplica en el tratamiento de aguas residuales para neutralizar microorganismos y reducir la carga contaminante antes de su vertido.
Desinfección de Aguas de Piscinas
El hipoclorito de sodio, especialmente en concentraciones del 13%, es fundamental para mantener las aguas de piscinas industriales y comerciales libres de bacterias y algas, asegurando un entorno seguro y agradable para el baño.
Limpieza y Desinfección Industrial
En industrias como la alimentaria, de bebidas y farmacéutica, el hipoclorito de sodio se emplea para la limpieza y desinfección de equipos sin necesidad de desmontarlos, garantizando altos estándares de higiene.
Otras Aplicaciones Industriales
- Agricultura: Se utiliza para la desinfección de instalaciones y equipos.
- Industria Química: Como reactivo o agente de limpieza.
- Industria Textil: Ampliamente utilizado como agente blanqueador.
- Industria del Papel: Para el blanqueo de la pulpa de celulosa.
- Industria Metalúrgica: Para la detoxificación de baños de cianuro.
- Sistemas de Enfriamiento: Previene la formación de algas y el crecimiento biológico en torres de enfriamiento.
- Eliminación de Olores: Neutraliza compuestos como el sulfuro de hidrógeno (H2S) y el amoniaco (NH3) en aguas residuales.
Concentraciones Comunes y su Uso
El hipoclorito de sodio se comercializa en diversas concentraciones, adaptándose a las necesidades específicas de cada aplicación:
- Uso Doméstico y Blanqueadores: Típicamente al 5% de hipoclorito de sodio. Es efectivo para la limpieza general y desinfección del hogar.
- Uso Industrial y Tratamiento de Aguas: Concentraciones del 10% al 15%. Estas soluciones más concentradas ofrecen un mayor poder desinfectante y son ideales para aplicaciones exigentes en plantas de tratamiento y procesos industriales. La concentración del 13% se considera ideal para una limpieza segura, rápida y efectiva en estos contextos.
- Desinfección de Pozos y Cloración de Choque: Se recomiendan concentraciones que permitan alcanzar niveles efectivos de cloro activo. Por ejemplo, para la desinfección de pozos, se sugiere alrededor de 1.9 litros de solución de hipoclorito por cada 30 metros de profundidad, la cual debe ser mezclada con agua antes de su aplicación.
- Grados Específicos: Existen grados de hipoclorito de sodio con concentraciones que van desde el 0.5% hasta el 5.25%, utilizados históricamente como antisépticos (soda clorada en odontología) o para desinfección de heridas abiertas durante la Primera Guerra Mundial.
CÓMO USAR LAS PASTILLAS DE HIPOCLORITO
Seguridad y Manipulación del Hipoclorito de Sodio
Dada su naturaleza corrosiva y oxidante, la manipulación del hipoclorito de sodio exige precauciones rigurosas:
Medidas de Protección Personal
Es crucial evitar el contacto directo con la piel, ojos y vías respiratorias. Se debe utilizar equipo de protección personal adecuado, incluyendo guantes resistentes a químicos, gafas de seguridad y, en caso de riesgo de inhalación de vapores, protección respiratoria.
Almacenamiento
El almacenamiento debe realizarse en áreas frescas, secas, bien ventiladas y lejos de la luz solar directa, fuentes de calor y materiales incompatibles. No debe almacenarse cerca de ácidos o amoniaco, ya que su mezcla puede liberar gases tóxicos y peligrosos.
Incompatibilidades y Reacciones Peligrosas
- Mezcla con Ácidos: La acidulación del hipoclorito de sodio libera gas cloro molecular (Cl2), que es tóxico y asfixiante.
- Mezcla con Amoniaco y Aminas: Forma cloraminas, compuestos generalmente tóxicos y explosivos.
- Contacto con Metales: Algunos metales pueden acelerar su descomposición.
- Calentamiento y Fricción: El hipoclorito de sodio en estado sólido es altamente inestable y puede descomponerse explosivamente.
Efectos para la Salud
La exposición al hipoclorito de sodio puede causar tos, dolor de garganta, dolor de estómago, sensación de quemazón, diarrea y vómitos si se ingiere. El contacto con los ojos y la piel provoca enrojecimiento y daños. La exposición prolongada puede sensibilizar la piel. En altas concentraciones, es altamente corrosivo y puede dañar superficies metálicas, telas y plásticos.
Legislación y Normativas
La legislación que rige el uso del hipoclorito de sodio a menudo se alinea con la del cloro, especialmente en lo que respecta a la desinfección de aguas. Normativas como el Reglamento (CE) No. 1907/2006 (REACH) establecen directrices para la seguridad química.
Proveedores y Consideraciones Comerciales
Al adquirir hipoclorito de sodio industrial al por mayor, es fundamental elegir un proveedor confiable. Empresas como Productos Químicos Xasali, con presencia estratégica en Monterrey (ubicada en 18 de Marzo No. 3122-A, Col. Centro), se especializan en la venta de este producto, ofreciendo formulaciones de alta estabilidad química y poder desinfectante. La demanda en ciudades con alta actividad industrial y de tratamiento de aguas, como Monterrey, impulsa la disponibilidad y la competencia en el mercado.
Al comprar hipoclorito de sodio, se debe considerar la concentración adecuada para la aplicación deseada, la estabilidad del producto, la reputación del proveedor y las garantías de seguridad y calidad.
Conclusión Parcial
El hipoclorito de sodio es un desinfectante y blanqueador de gran eficacia, cuya utilidad se maximiza mediante la correcta comprensión de su concentración, propiedades y precauciones de manejo. Su papel en la purificación del agua, la higiene industrial y diversas aplicaciones cotidianas es insustituible, siempre y cuando se emplee con la debida diligencia y respeto por las normativas de seguridad. La elección de la concentración adecuada, como el 13% para aplicaciones industriales exigentes, es clave para garantizar resultados óptimos y seguros.
tags: #porcentaje #de #hipoclorito #de #sodio