La metalurgia, ciencia fundamental para el desarrollo industrial y tecnológico, se cimienta en la capacidad de transformar los minerales extraídos de la tierra en metales puros y funcionales. Este intrincado proceso, conocido como purificación o refinación de metales, es esencial para dotar a estos materiales de las propiedades físicas y químicas requeridas para una vasta gama de aplicaciones, desde la electrónica de vanguardia hasta la construcción de infraestructuras vitales. La pureza de un metal no es un mero detalle estético; es el factor determinante de su eficacia, durabilidad y conductividad, impactando directamente en el rendimiento de innumerables productos y tecnologías que definen nuestra vida moderna.
La Imperiosa Necesidad de la Pureza Metálica
La razón primordial detrás de la purificación de metales reside en la optimización de sus propiedades intrínsecas. Las impurezas, incluso en concentraciones mínimas, pueden actuar como disruptores, alterando drásticamente las características deseables de un metal. Por ejemplo, la presencia de ciertos contaminantes en el cobre, un conductor eléctrico por excelencia, puede disminuir significativamente su conductividad, comprometiendo el funcionamiento de dispositivos electrónicos y sistemas de transmisión de energía. La purificación, por tanto, se traduce directamente en una calidad mejorada de los metales, asegurando que posean las propiedades físicas óptimas para su uso previsto.
Además de la mejora de la conductividad y otras propiedades físicas, la eliminación de impurezas específicas confiere a los metales una mayor resistencia a la oxidación. Ciertos elementos presentes en los metales en bruto pueden actuar como catalizadores o puntos de inicio para procesos de corrosión, mermando la integridad estructural y la vida útil del material. Al purificar el metal, se eliminan estas sustancias promotoras de la degradación, prolongando su durabilidad y reduciendo la necesidad de mantenimiento o reemplazo.
La industria tecnológica es, quizás, el sector que más exige niveles de pureza extrema. En la fabricación de semiconductores, por ejemplo, la presencia de impurezas a nivel atómico puede alterar irreversiblemente las propiedades electrónicas del material, haciendo que componentes enteros fallen. Para estas aplicaciones avanzadas, la pureza no es una opción, sino una condición sine qua non. El cobre destinado a aplicaciones electrónicas de alta gama, por ejemplo, debe alcanzar una pureza mínima del 99.99%, un estándar que solo se logra a través de procesos de refinación sofisticados.
La eficacia de cualquier proceso de purificación puede ser cuantificada mediante modelos matemáticos. Una métrica común es la eficacia de extracción de impurezas, que se puede expresar mediante la siguiente ecuación:
[ E = \left( 1 - \frac{Cf}{Ci} \right) \times 100 ]
Donde ( Ci ) representa la concentración inicial de la impureza o del metal impuro, y ( Cf ) es la concentración final después del proceso de purificación. El valor ( E ) se expresa en porcentaje y refleja la efectividad del método empleado para reducir la concentración de sustancias indeseadas.
Diversidad de Métodos: Herramientas para Cada Metal
La elección del método de purificación de metales depende intrínsecamente de la naturaleza del metal en cuestión, sus propiedades físicas y químicas, y el nivel de pureza requerido. No existe una solución única; la metalurgia ofrece un abanico de técnicas, desde las más sencillas hasta las más complejas, para abordar este desafío.
Destilación: Separando por Puntos de Ebullición
La destilación es un método de purificación particularmente eficaz para metales que poseen bajos puntos de ebullición. El principio fundamental se basa en la diferencia de volatilidad entre el metal y sus impurezas. El metal impuro se calienta hasta alcanzar su punto de ebullición, transformándose en vapor. Este vapor se dirige luego a un sistema de enfriamiento, donde se condensa y se recolecta en forma de un metal más puro. Este proceso es ideal para la purificación de metales volátiles como el zinc y el mercurio.
Una variante avanzada de esta técnica es la destilación fraccionada. Este método se emplea cuando las impurezas tienen puntos de ebullición cercanos a los del metal deseado. Mediante el uso de una columna de fraccionamiento, se logra una separación más precisa al permitir múltiples ciclos de evaporación y condensación a diferentes temperaturas. La columna está diseñada con superficies internas que facilitan la condensación y re-evaporación, concentrando progresivamente el componente más volátil en la parte superior y el menos volátil en la inferior. Esta técnica es crucial en la industria de semiconductores para obtener materiales de altísima pureza.
Un ejemplo clásico de destilación es la purificación del mercurio. Dada su baja temperatura de ebullición (356.7 °C), el mercurio se vaporiza fácilmente. Al condensar este vapor, se obtiene un metal considerablemente más puro, eliminando impurezas menos volátiles.
Electrólisis: La Fuerza de la Corriente Eléctrica
La electrólisis es un método electroquímico robusto y ampliamente utilizado para la purificación de metales, especialmente aquellos que forman iones estables en solución. Este proceso aprovecha la corriente eléctrica para inducir reacciones químicas que separan el metal puro de sus impurezas.
En la electrólisis de metales, el metal impuro se utiliza como ánodo (electrodo positivo) y una lámina de metal puro se emplea como cátodo (electrodo negativo). Ambos se sumergen en una solución electrolítica que contiene iones del metal a purificar. Al aplicar una corriente eléctrica, los iones del metal presente en el electrolito migran hacia el cátodo. En el cátodo, estos iones ganan electrones y se depositan como metal puro. Simultáneamente, en el ánodo, el metal impuro se disuelve, liberando iones metálicos a la solución. Las impurezas que no son conductoras o que tienen una tendencia electroquímica diferente se desprenden del ánodo y se acumulan en el fondo de la celda electrolítica, formando lo que se conoce como "barro anódico". Este barro, a menudo, contiene metales preciosos como oro, plata o platino, que pueden ser recuperados en procesos posteriores, añadiendo valor económico a la purificación.
El proceso de electrólisis es fundamental para la obtención de cobre de alta pureza, necesario para la industria eléctrica. En la electrólisis del cobre, el ánodo está hecho de cobre impuro, y el cátodo es una fina lámina de cobre puro. El electrolito es una solución de sulfato de cobre. Al aplicar corriente, el cobre del ánodo se disuelve como iones ( \text{Cu}^{2+} ) y se deposita como cobre metálico en el cátodo. El resultado es la obtención de cobre con una pureza que supera el 99.99%, superando con creces la calidad del cobre original. Este método no solo garantiza la pureza del cobre, sino que también maximiza la recuperación de subproductos valiosos presentes en el barro anódico.
La electrólisis también es la base de la galvanoplastia, un proceso de recubrimiento que utiliza la deposición electroquímica para aplicar una capa fina de un metal a otro objeto.
Zona de Fusión: El Poder de la Solidificación Selectiva
La zona de fusión es una técnica de purificación altamente especializada, especialmente valorada en la producción de materiales semiconductores de ultra alta pureza, como el silicio. Este método se fundamenta en el principio de que las impurezas son generalmente más solubles en el estado líquido (fundido) de un metal que en su estado sólido cristalino.
El proceso comienza con una barra de metal impuro. Se utiliza un calentador circular móvil que genera una pequeña zona fundida a lo largo de la barra. A medida que el calentador se desplaza a lo largo de la barra, la zona fundida se mueve con él. El metal en la zona fundida se solidifica a medida que el calentador se aleja, pero lo hace de manera selectiva. El metal puro tiende a cristalizar y formar una estructura sólida ordenada, mientras que las impurezas, al ser más solubles en el líquido, permanecen concentradas en la zona fundida. Al repetir este proceso varias veces, moviendo la zona fundida de un extremo al otro de la barra, las impurezas se van concentrando gradualmente en un extremo de la barra, dejando el resto del material con una pureza cada vez mayor. Al final, el extremo enriquecido en impurezas se desecha, obteniendo una barra de metal de una pureza excepcional.
Amalgamación: El Papel del Mercurio
La amalgamación es un proceso histórico, utilizado a menudo en la extracción y purificación de oro. Consiste en el uso de mercurio para formar una amalgama (una aleación líquida) con el metal deseado. El oro, por ejemplo, se disuelve fácilmente en mercurio, formando una amalgama. Las impurezas que no reaccionan con el mercurio pueden ser separadas. Posteriormente, el mercurio se evapora mediante calentamiento, dejando atrás el oro purificado. Si bien este método ha sido históricamente importante, su uso se ha visto restringido debido a la alta toxicidad del mercurio y los graves riesgos ambientales y para la salud que conlleva su manipulación y emisión.
Técnicas de Ingeniería para la Metrología Moderna
La ingeniería juega un papel crucial en el desarrollo y optimización de las técnicas de purificación de metales, buscando no solo la alta pureza sino también la eficiencia y la sostenibilidad de los procesos.
Filtración: Reteniendo lo Indeseado
La filtración es una técnica de purificación física que, aunque básica, resulta fundamental en muchas etapas del procesamiento de metales. Su objetivo principal es la eliminación de partículas sólidas suspendidas en una fase líquida o gaseosa. En el contexto de la purificación de metales, se aplica comúnmente al metal en estado fundido o disuelto.
El proceso de filtración mecánica implica hacer pasar el metal líquido a través de un medio poroso diseñado para retener las impurezas sólidas. Los filtros pueden variar desde mallas metálicas hasta materiales cerámicos avanzados o membranas con poros de tamaño nanométrico. La eficacia de la filtración depende del tamaño de los poros del filtro y de la velocidad del flujo del metal.

En la purificación de aluminio fundido, por ejemplo, se utilizan filtros cerámicos especiales capaces de soportar las altas temperaturas y el ambiente corrosivo del aluminio derretido. Estos filtros atrapan inclusiones de óxido y otras partículas sólidas, mejorando la calidad del aluminio final.
Los avances en nanotecnología han permitido el desarrollo de filtros con nanoestructuras que ofrecen una superficie de filtración enormemente ampliada, permitiendo la captura de partículas extremadamente pequeñas. Los filtros de carbón activado, por su parte, aprovechan las propiedades adsorbentes del carbón para capturar sustancias no deseadas a nivel molecular, siendo especialmente útiles en la purificación de metales preciosos o en el tratamiento de aguas residuales de procesos metalúrgicos.
La velocidad del flujo (( v )) a través de un filtro está directamente relacionada con el caudal volumétrico (( Q )) y el área transversal del filtro (( A )), según la ecuación:
[ v = \frac{Q}{A} ]
Controlar esta velocidad es crucial, especialmente para metales sensibles a la degradación térmica o a la formación de óxidos a altas temperaturas.
Uso de Disolventes: Extracción Selectiva
El uso de disolventes es una técnica de purificación versátil que se basa en la capacidad de un líquido (el disolvente) para disolver selectivamente uno o más componentes de una mezcla. En metalurgia, este método se emplea para extraer metales específicos de sus minerales o aleaciones, dejando atrás las impurezas insolubles o menos solubles.
La clave de la eficacia de la extracción por disolventes radica en la afinidad química entre el disolvente y el metal deseado. Se seleccionan disolventes que tengan una alta afinidad por el metal a extraer, mientras que las impurezas permanecen sin disolver o con una solubilidad muy limitada. La eficiencia de la separación se puede cuantificar mediante la constante de distribución (( K )), que describe cómo se distribuye un soluto entre dos fases inmiscibles en equilibrio. En el caso de la extracción líquido-líquido, se define como:
[ K = \frac{[\text{metal}]{\text{orgánico}}}{[\text{metal}]{\text{acuoso}}} ]
Donde ( [\text{metal}]{\text{orgánico}} ) y ( [\text{metal}]{\text{acuoso}} ) son las concentraciones del metal en la fase orgánica (disolvente) y acuosa, respectivamente. Un valor de ( K ) elevado indica una preferencia del metal por la fase orgánica, facilitando su extracción.
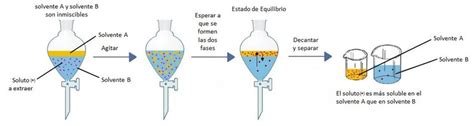
Un ejemplo notable es la purificación del uranio, donde se utiliza un disolvente orgánico como el fosfato de tributilo (TBP) en un sistema acuoso para extraer selectivamente el uranio de sus impurezas. La manipulación del pH del medio acuoso puede alterar significativamente la solubilidad de los metales, permitiendo optimizar la selectividad y la eficiencia de la separación.
Casos Prácticos: La Purificación en Acción
La teoría cobra vida en las aplicaciones prácticas de la purificación de metales, demostrando su importancia en industrias clave.
El Refinado del Cobre: Conduciendo la Electricidad
Como se mencionó anteriormente, el cobre es indispensable en la industria electrónica debido a su excepcional conductividad eléctrica. La electrólisis es el método predilecto para alcanzar la pureza requerida (superior al 99.99%). En este proceso, el cobre impuro, extraído de minas o reciclado, se utiliza como ánodo. Al pasar una corriente eléctrica a través de una solución de sulfato de cobre, los iones de cobre del ánodo se disuelven y se redepositan como cobre puro en el cátodo. Las impurezas como el hierro, el plomo, la plata y el oro quedan en el ánodo o se depositan en el fondo de la celda electrolítica como barro anódico, del cual se pueden recuperar posteriormente los metales preciosos. Este método no solo eleva la pureza y la conductividad del cobre, sino que también mejora su resistencia a la corrosión.
Refinería Electrolítica Codelco División Ventanas
El Oro: Brillo y Valor Protegidos
El oro, un metal de gran valor en joyería, finanzas y tecnología, también requiere procesos de purificación específicos. Uno de los métodos más comunes es la lixiviación por cianuro. En este proceso, el oro se disuelve en una solución acuosa de cianuro en presencia de oxígeno. El oro forma un complejo soluble de cianuro de oro, separándose así de la mayoría de las impurezas. Posteriormente, el oro se recupera de la solución mediante la adición de polvo de zinc, que precipita el oro en forma sólida. Este oro precipitado se funde para obtener lingotes de alta pureza.
Para aplicaciones que demandan pureza extrema, como en la industria electrónica, se recurre a métodos más rigurosos. El agua regia, una mezcla de ácido nítrico y ácido clorhídrico concentrados, es capaz de disolver el oro y también muchas de las impurezas de platino que a menudo lo acompañan. El oro disuelto en agua regia puede luego precipitarse o recuperarse mediante procesos electroquímicos.
El Tratamiento de Minerales: Del Yacimiento al Producto Útil
El tratamiento de minerales es el conjunto de operaciones físicas y químicas destinadas a aumentar el contenido de minerales valiosos en una mena extraída, separándolos de la roca estéril (ganga). Este proceso es fundamental para hacer que la minería sea rentable y para preparar los minerales para etapas posteriores de refinación.
Reducción de Tamaño: Trituración y Molienda
El primer paso en el tratamiento de minerales es la reducción del tamaño de las partículas. Esto se logra mediante trituración y molienda. Las trituradoras (de mandíbulas, giratorias, de cono) reducen el tamaño de la mena en etapas, preparándola para la molienda. Los molinos (de bolas, de barras) fragmentan aún más el mineral hasta alcanzar un tamaño de partícula que permita la liberación de los compuestos metálicos valiosos, un proceso conocido como molienda fina.
Separación y Concentración: Métodos Clave
Una vez reducido el tamaño, se aplican diversos métodos para separar los minerales valiosos de la ganga:
Separación por Gravedad: Aprovecha las diferencias en la densidad (peso específico) entre los minerales valiosos y la ganga. Se utilizan equipos como mesas vibratorias, espirales y esclusas, que utilizan la fuerza de la gravedad y el agua para separar las partículas más pesadas. Es un método eficaz para minerales pesados como el estaño, el wolframio, la cromita y, por supuesto, el oro.

Separación Magnética: Se basa en las propiedades magnéticas de ciertos minerales. Los separadores magnéticos utilizan campos magnéticos para atraer y separar minerales ferromagnéticos o paramagnéticos de la ganga no magnética. Es crucial para la concentración de minerales de hierro como la magnetita y la hematita.
Flotación por Espuma: Una técnica química y física muy extendida, especialmente para minerales sulfurados complejos de cobre, plomo, zinc y platino. Se añaden reactivos químicos (colectores, espumantes, depresores) al mineral molido suspendido en agua. Los colectores hacen que las partículas del mineral valioso se adhieran a las burbujas de aire introducidas en la celda de flotación, provocando que floten hacia la superficie, donde se recogen. La ganga, que no se adhiere a las burbujas, permanece en el fondo.

Separación Electrostática: Utiliza las diferencias en la conductividad eléctrica de los minerales. Las partículas se cargan eléctricamente y luego pasan a través de un campo eléctrico. Su trayectoria se desvía según su carga, permitiendo la separación. Es útil para minerales como la ilmenita, el rutilo (minerales de titanio) y el circón.
Beneficio Químico (Lixiviación): Implica el uso de reactivos químicos para disolver selectivamente los minerales valiosos. La lixiviación con ácidos (como ácido sulfúrico) o bases (como hidróxido de sodio) es común para extraer metales como el cobre, el uranio y el oro. La lixiviación con cianuro es un método clave para la extracción de oro, aunque requiere precauciones especiales debido a la toxicidad del cianuro.
Deshidratación y Secado: Preparando el Producto Final
Tras la concentración, los minerales a menudo se encuentran en forma de suspensiones acuosas o lodos. Las etapas de deshidratación (espesamiento) y secado son cruciales para eliminar el exceso de agua y obtener un producto sólido y manejable. El espesamiento utiliza la gravedad para separar el agua, mientras que el secado emplea calor (hornos rotatorios, secadores de lecho fluidizado) para eliminar la humedad residual. Estos pasos son vitales para la calidad y la viabilidad económica del producto final.
Retos y Futuro de la Metalurgia
La industria metalúrgica, a pesar de su importancia histórica y actual, enfrenta significativos desafíos de futuro. Uno de los más apremiantes es la reducción del consumo energético y la adopción de procesos más eficientes y limpios. La metalurgia es intrínsecamente intensiva en energía, y la búsqueda de fuentes de energía renovables y tecnologías de bajo consumo es fundamental. El reciclaje de metales juega un papel cada vez más importante, no solo para conservar recursos naturales sino también para reducir la energía y el impacto ambiental asociados a la extracción primaria.
La extracción de metales es una actividad económica global de gran envergadura, que genera millones de empleos y contribuye significativamente al PIB de muchos países. La innovación continua en los procesos de extracción, purificación y aleación de metales es esencial para satisfacer la creciente demanda mundial de materiales, al tiempo que se minimiza el impacto ambiental y se promueve un desarrollo sostenible. La metalurgia del futuro deberá equilibrar la necesidad de recursos con la responsabilidad ambiental, impulsando la economía circular y la adopción de tecnologías verdes.
La metalurgia como ciencia y tecnología abarca la extracción de metales de sus minerales, su purificación y su aleación para obtener propiedades deseadas. Los procesos de extracción pueden ser pirometalúrgicos (altas temperaturas), hidrometalúrgicos (soluciones acuosas) o electrometalúrgicos (corriente eléctrica). Cada uno de estos enfoques presenta sus propias ventajas y desafíos, y la elección depende del mineral y el metal objetivo.
La extracción de hierro, por ejemplo, se realiza principalmente mediante el proceso de reducción en altos hornos, donde el mineral de hierro (hematita o magnetita) reacciona con carbono y aire caliente para producir hierro fundido. La purificación posterior se lleva a cabo en convertidores para eliminar impurezas.
Para el aluminio, el proceso Hall-Héroult es el método dominante. Implica la electrólisis de alúmina (óxido de aluminio) disuelta en criolita fundida. La electrólisis descompone la alúmina, depositando aluminio metálico en el cátodo.
La extracción de cobre se realiza comúnmente por pirometalurgia (fundición) o hidrometalurgia (lixiviación con ácido sulfúrico seguida de extracción por solventes o electrólisis).
Estos procesos demuestran la complejidad y la escala de la metalurgia moderna, una disciplina que continúa evolucionando para satisfacer las demandas de un mundo en constante progreso.