La ósmosis es un proceso físico-químico de vital importancia que se manifiesta tanto en los sistemas biológicos como en diversas aplicaciones tecnológicas. Se define como el movimiento de un disolvente, típicamente agua, a través de una membrana semipermeable. Este fenómeno ocurre cuando existen dos soluciones con diferentes concentraciones de solutos separadas por dicha membrana, la cual permite el paso del disolvente pero restringe el de los solutos. La ósmosis es un proceso pasivo, lo que significa que no requiere un aporte externo de energía para llevarse a cabo.
¿Qué es la Ósmosis y Cómo se Produce?
En esencia, la ósmosis es un mecanismo natural que busca el equilibrio. Cuando una membrana semipermeable separa dos soluciones de distinta concentración, el disolvente (agua) tiende a desplazarse desde la solución menos concentrada (hipotónica) hacia la solución más concentrada (hipertónica). Este movimiento continúa hasta que las concentraciones de solutos en ambos lados de la membrana se igualan, o hasta que la presión ejercida por el disolvente contrarreste el flujo.
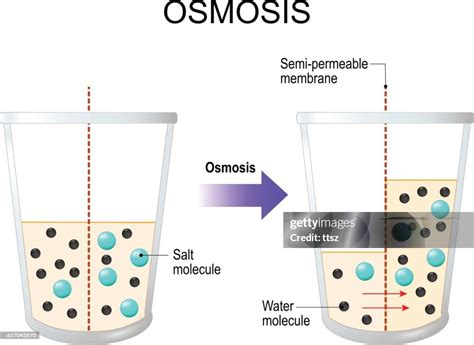
El proceso se puede visualizar con un ejemplo sencillo. Imaginemos un recipiente dividido por una membrana semipermeable. En un lado, colocamos agua pura, y en el otro, una solución salina. La membrana permitirá que las moléculas de agua crucen libremente, pero las moléculas de sal, al ser más grandes, quedarán retenidas. De esta manera, el agua fluirá desde el lado de menor concentración de solutos (agua pura) hacia el lado de mayor concentración (solución salina), buscando diluir esta última y alcanzar un estado de equilibrio.
Este fenómeno fue observado y descrito inicialmente en el siglo XVIII por el abad Nollet, quien notó el paso de agua a través de la vejiga de un animal separando agua y alcohol. Posteriormente, en el siglo XIX, Henri Dutrochet acuñó los términos "endosmosis" y "exosmosis" para describir este movimiento direccional del disolvente. El descubrimiento de membranas artificiales, como la de ferrocianuro de cobre por M. Traube en 1864, y los trabajos de Jacobus Henricus van 't Hoff sobre la analogía entre soluciones acuosas y gases perfectos, sentaron las bases para una comprensión más profunda de la ósmosis y la presión osmótica.
La Membrana Semipermeable: El Corazón del Proceso
La característica fundamental que permite la ósmosis es la presencia de una membrana semipermeable. Estas membranas, ya sean de origen biológico o artificial, poseen poros de tamaño molecular. El tamaño de estos poros es crucial, ya que permite el paso de moléculas pequeñas, como las del disolvente, pero impide el paso de moléculas más grandes, como las de los solutos. Las membranas celulares de los organismos vivos son ejemplos primordiales de membranas semipermeables, desempeñando un papel esencial en el mantenimiento de la homeostasis celular.
Presión Osmótica: La Fuerza Impulsora
La presión osmótica es la presión mínima que debe aplicarse a una solución para evitar el flujo de disolvente a través de una membrana semipermeable, desde una solución pura o menos concentrada hacia ella. En términos más sencillos, es la presión que ejerce el disolvente (agua) sobre la cara de la membrana donde se encuentra la solución de mayor concentración, como resultado del movimiento del disolvente para equilibrar las concentraciones. Esta presión está directamente relacionada con la osmolaridad de la solución, es decir, la concentración total de partículas de soluto disueltas. Cuanto mayor sea la concentración de solutos, mayor será la presión osmótica.
A modo de ejemplo, la diferencia de presión osmótica entre agua desalinizada y agua de mar puede ser de aproximadamente 50 atmósferas. Este concepto es fundamental para comprender cómo funcionan los procesos biológicos y para el diseño de tecnologías de separación y purificación.
Ósmosis en los Seres Vivos: Un Equilibrio Delicado
La ósmosis juega un papel crucial en la fisiología de todos los organismos vivos. Las membranas celulares, al ser semipermeables, regulan el paso de agua y otras sustancias, manteniendo el equilibrio osmótico necesario para la supervivencia celular.
En Células Animales: Citólisis y Crenación
El interior de las células animales, como los glóbulos rojos, contiene una concentración de solutos específica. Cuando estas células se encuentran en diferentes medios acuosos, la ósmosis puede tener efectos drásticos:
- Medio Hipotónico: Si una célula se encuentra en una solución hipotónica (menor concentración de solutos que el interior celular), el agua tenderá a entrar en la célula para equilibrar las concentraciones. Este exceso de entrada de agua puede hacer que la célula se hinche y, en casos extremos, estalle, un fenómeno conocido como citólisis.
- Medio Hipertónico: Por el contrario, si la célula se encuentra en una solución hipertónica (mayor concentración de solutos que el interior celular), el agua saldrá de la célula hacia el medio exterior. Esta pérdida de agua puede provocar que la célula se encoja y se arrugue, un proceso llamado crenación. La deshidratación severa puede llevar a la muerte celular.
Para evitar estas consecuencias, las células animales poseen mecanismos activos, como bombas de iones, que les permiten expulsar el exceso de agua o regular la concentración de solutos, incluso en contra de los gradientes osmóticos.
En Células Vegetales: Turgencia y Plasmólisis
Las células vegetales también están rodeadas por membranas semipermeables y experimentan fenómenos osmóticos similares, con algunas particularidades debido a la presencia de la pared celular:
- Turgencia: Cuando una célula vegetal se encuentra en un medio hipotónico, el agua entra en la vacuola central, aumentando el volumen celular y ejerciendo presión contra la pared celular. Esta presión, conocida como turgencia, confiere rigidez a los tejidos vegetales y es esencial para el soporte estructural de las plantas.
- Plasmólisis: En un medio hipertónico, el agua sale de la célula vegetal. A diferencia de las células animales, la pared celular rígida mantiene parcialmente la forma de la célula. Sin embargo, la membrana plasmática puede separarse de la pared celular a medida que el citoplasma se deshidrata, un proceso llamado plasmolisis. En algunos casos, la plasmolisis puede ser un estado irreversible.
Los organismos han desarrollado adaptaciones para manejar estos procesos. Por ejemplo, los riñones en vertebrados, las branquias en peces y las glándulas de sal en aves son órganos especializados que participan en la regulación del equilibrio hídrico y salino, utilizando principios osmóticos. Las plantas absorben agua del suelo a través de sus raíces por ósmosis directa, un proceso vital para su crecimiento y supervivencia.
Ósmosis Inversa: Tecnología al Servicio de la Purificación
Mientras que la ósmosis directa es un proceso natural que busca el equilibrio, la ósmosis inversa (OI) es un proceso tecnológico que, mediante la aplicación de presión externa, invierte el flujo natural del disolvente. En la ósmosis inversa, se aplica una presión superior a la presión osmótica en el lado de la solución más concentrada, forzando al disolvente (agua) a pasar a través de la membrana semipermeable hacia la solución menos concentrada.
Este proceso es extremadamente eficaz para la separación de solutos del disolvente. A diferencia de la ósmosis directa, donde se obtienen dos soluciones de igual concentración, la ósmosis inversa produce una solución muy concentrada (rechazo) y otra muy diluida o prácticamente pura (permeado).
Aplicaciones de la Ósmosis Inversa
La ósmosis inversa ha revolucionado numerosas industrias y ha encontrado aplicaciones prácticas en la vida cotidiana:
- Desalación de Agua: Es uno de los usos más importantes de la ósmosis inversa. Permite transformar agua de mar o agua salobre en agua potable de alta calidad, separando las sales disueltas mediante membranas especiales. Este proceso es fundamental para el suministro de agua en regiones áridas o con escasez de recursos hídricos.
- Purificación de Agua Doméstica e Industrial: Los sistemas de ósmosis inversa se utilizan ampliamente para eliminar contaminantes del agua, como cloro, plomo, pesticidas, bacterias y virus, produciendo agua de excelente calidad para consumo humano. En la industria, se emplea para obtener agua desmineralizada o ultrapura para procesos farmacéuticos, electrónicos y de producción de alimentos.
- Procesos Industriales: La ósmosis inversa se aplica en la fabricación de leche en polvo y jugos concentrados, donde se elimina el agua para solidificar los solutos y facilitar su comercialización y transporte. También se utiliza en la recuperación de productos valiosos de efluentes industriales, como la plata de desechos de papel fotográfico o el alcohol de vinazas.
- Agricultura: Permite la irrigación eficiente mediante la filtración de agua, asegurando que las plantas reciban agua libre de sales o contaminantes perjudiciales.
- Tratamiento de Aguas Residuales: Ayuda a tratar efluentes industriales y domésticos, recuperando agua para su reutilización y reduciendo el impacto ambiental.
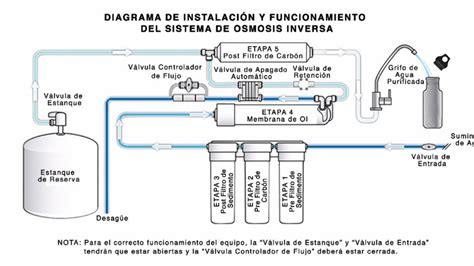
¿Cómo funciona el sistema de purificación de agua por osmosis inversa?
Consideraciones en Sistemas de Ósmosis Inversa
La eficacia de un sistema de ósmosis inversa depende de varios factores clave, incluyendo la calidad del agua de entrada, el tipo de membrana utilizada y el mantenimiento regular. Las membranas de ósmosis inversa, a menudo fabricadas con poliamida, tienen una alta capacidad de rechazo salino, típicamente entre el 96.5% y el 99.8%. Sin embargo, existen algunas restricciones; ciertos compuestos como el arsenito, la sílice neutra y el boro pueden no ser completamente retenidos y requieren tratamientos adicionales.
El mantenimiento es esencial para garantizar el rendimiento óptimo y la longevidad del sistema. Esto incluye el cambio periódico de filtros, la revisión de la membrana semipermeable y la limpieza general del equipo. Los sistemas modernos están diseñados para optimizar la eficiencia y reducir la cantidad de agua desperdiciada en el proceso de rechazo.
En resumen, la ósmosis es un fenómeno fascinante que abarca desde los procesos biológicos más fundamentales hasta las tecnologías más avanzadas. Su comprensión es clave para apreciar la complejidad de la vida y para desarrollar soluciones innovadoras a desafíos como la escasez de agua y la purificación de recursos.