El hidróxido de sodio (NaOH), comúnmente conocido como sosa cáustica, y el hipoclorito de sodio (NaOCl) son dos compuestos químicos de gran relevancia en diversas facetas de la industria y la vida cotidiana. A pesar de compartir la presencia del sodio en su composición, sus propiedades, métodos de producción y aplicaciones presentan diferencias significativas, aunque ambos son reconocidos por su poder limpiador y desinfectante.
La Sosa Cáustica: Versatilidad y Reactividad
La sosa cáustica, o hidróxido de sodio, es un compuesto alcalino de alta reactividad, fundamental en una extensa gama de industrias. Su naturaleza sólida y cristalina, de color blanco en estado puro, se disuelve en agua liberando calor, lo que exige precauciones extremas durante su manipulación. Identificada en el siglo XVIII, su producción se intensificó con la Revolución Industrial, facilitando su aplicación masiva en la fabricación de papel, jabones y textiles.
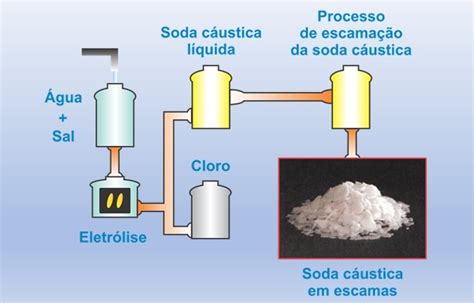
La producción industrial del hidróxido de sodio se basa principalmente en la electrólisis de una solución de cloruro de sodio (sal común). Existen tres tecnologías principales para este proceso: celdas de diafragma, celdas de cátodo de mercurio y celdas de membrana. El método de membrana es considerado el más innovador y eficiente energéticamente. La sosa cáustica se comercializa en distintos grados de pureza y concentraciones, siendo las soluciones acuosas entre el 20% y el 50% las más habituales. Su alta higroscopicidad, es decir, su capacidad para absorber la humedad del aire, requiere un almacenamiento adecuado.
La sosa cáustica es esencial en aquellas industrias que demandan un agente de limpieza, neutralización o saponificación. Su fuerte alcalinidad le permite neutralizar ácidos y elevar el pH, siendo crucial en procesos como:
- Industria de pulpa y papel: El NaOH se utiliza para disolver la lignina, la sustancia que une las fibras de celulosa en la madera. Este proceso facilita la separación de las fibras, permitiendo la producción de papel de alta calidad. En la industria papelera, la sosa actúa sobre la pulpa y diluye la lignina para producir celulosa. La sosa fabricada mediante procesos electrolíticos de alta pureza es apta para los usos más exigentes.
- Industria textil: En la fase de mercerización, el hidróxido de sodio otorga mayor consistencia y brillo a las fibras de algodón, mejorando su resistencia y su capacidad para absorber colorantes.
- Fabricación de jabones (saponificación): La sosa cáustica es un componente indispensable en la reacción química que convierte grasas en jabón. La elaboración de jabones artesanales, utilizando únicamente agua, sosa cáustica y aceite, es uno de sus usos más tradicionales.
- Industria química y de productos de limpieza: Actúa como agente neutralizante y reactivo base en la producción de detergentes, desinfectantes y limpiadores industriales. Es un componente esencial en la fabricación de otros productos químicos, como la alúmina a partir de bauxita. También se utiliza para el control del pH en la neutralización de ácidos residuales.
- Tratamiento de aguas: El hidróxido de sodio aumenta el pH del agua, siendo útil para equilibrar el pH de piscinas y asegurar la efectividad del cloro como desinfectante.
- Agricultura: Se emplea para remover la piel de tubérculos, verduras y frutas como patatas, tomates y zanahorias.
- Decapante de pinturas: Especialmente para retirar esmaltes, pinturas y barnices de superficies de madera.
- Producción de alimentos: Aunque no se detalla explícitamente en la información proporcionada, su uso en la industria alimentaria es también relevante, como en el curado de aceitunas.
- Producción de gas y petróleo: La sosa se emplea en perforación para controlar el pH de los lodos y como bactericida.
Que es La SOSA Cáustica? y Para que Sirve?
La sosa cáustica reacciona vigorosamente con ácidos, disuelve grasas y aceites, y al contacto con ciertos metales como aluminio, magnesio, zinc y estaño, libera gas hidrógeno, un compuesto inflamable y explosivo. Su naturaleza altamente alcalina y corrosiva exige medidas de seguridad estrictas, incluyendo el uso de equipo de protección personal (guantes, gafas, ropa protectora) y la manipulación en áreas bien ventiladas. La neutralización previa a su eliminación es crucial para evitar la contaminación ambiental.
Hipoclorito de Sodio: El Desinfectante y Blanqueador
El hipoclorito de sodio (NaOCl) es un compuesto químico conocido principalmente por sus propiedades desinfectantes, blanqueantes y eliminadoras de olores. Alrededor de 1785, el químico francés Berthollet desarrolló líquidos blanqueantes a base de hipoclorito de sodio, que la compañía Javel introdujo al mercado como "licor de Javel", inicialmente para el blanqueo de algodón. En Francia, aún se le conoce como "eau de Javel".
El hipoclorito de sodio se presenta como una solución clara, de ligero color amarillento y con un olor característico. Su densidad relativa es de 1,1. Las soluciones de uso doméstico suelen contener alrededor del 5% de hipoclorito de sodio y tienen un pH cercano a 11, lo que las hace irritantes. Concentraciones mayores (10-15%) presentan un pH más elevado (alrededor de 13), siendo corrosivas y capaces de causar quemaduras.

Este compuesto es inestable y tiende a perder su eficacia con el tiempo debido a la evaporación del cloro activo. Se desintegra al ser calentado, al entrar en contacto con ácidos, luz solar directa, ciertos metales y sustancias corrosivas. Como oxidante fuerte, reacciona con compuestos combustibles y reductores.
La producción de hipoclorito de sodio puede realizarse de dos maneras principales:
- Electrólisis de salmuera: Se disuelve sal en agua blanda para generar una solución salina, que luego se somete a electrólisis. Este proceso genera una solución de hipoclorito de sodio en agua, que puede contener hasta 150 gramos de cloro activo por litro. Durante la reacción se produce gas hidrógeno, que es explosivo.
- Reacción de cloro gaseoso con sosa cáustica: La adición de cloro gaseoso (Cl2) a una solución de sosa cáustica (NaOH) produce hipoclorito de sodio, agua y sal, según la reacción: Cl2 + 2NaOH → NaOCl + NaCl + H2O.
El hipoclorito de sodio es ampliamente utilizado en:
- Desinfección y purificación de agua: Es un agente desinfectante eficaz para el agua potable, piscinas y aguas residuales. En piscinas, ayuda a mantener un nivel de pH adecuado y previene el crecimiento de algas.
- Blanqueo: Se utiliza en la industria textil y en el hogar para eliminar manchas de la ropa a temperatura ambiente.
- Limpieza doméstica e industrial: Es un componente clave en la fabricación de lejía y lavandina, y se usa para la purificación y desinfección de superficies.
- Industria alimentaria, química, papelera y farmacéutica: Su aplicación abarca diversos procesos, incluyendo la desintoxicación de baños de cianuro en industrias del metal.
- Eliminación de olores: Neutraliza gases como el sulfuro de hidrógeno (SH) y el amoníaco (NH3) en aguas residuales.
Al disolverse en agua, el hipoclorito de sodio genera ácido hipocloroso (HOCl) y ion hipoclorito (OCl-), ambos con poder oxidante y desinfectante. El ácido hipocloroso es el agente más activo. El pH del agua influye en la cantidad de HOCl formado; para optimizar su acción, se suele ajustar el pH con ácidos como el acético o el sulfúrico.

La exposición al hipoclorito de sodio puede causar irritación en las vías respiratorias, dolor de estómago, quemaduras, diarrea y daños en ojos y piel. En concentraciones elevadas, como las utilizadas en piscinas, puede provocar enrojecimiento ocular y el característico "olor a cloro" debido a la formación de cloraminas, especialmente cuando hay presencia de urea (orina y sudor). La legislación para su uso a menudo se equipara a la del cloro.
Consideraciones sobre la Saponificación y Sustitución
Existe un debate y consulta en torno a la posibilidad de utilizar hipoclorito de sodio en lugar de sosa cáustica para la saponificación. Si bien el hipoclorito de sodio tiene un pH alcalino y se le atribuye poder limpiador por saponificar grasas, su composición molecular difiere significativamente de la sosa cáustica. El hipoclorito de sodio contiene cloro en su molécula, y su reacción con aceites puede ser compleja y potencialmente generar subproductos no deseados o inseguros. Expertos advierten que, aunque ambos compuestos contienen sodio y tienen propiedades alcalinas, no son sustituibles directamente en la reacción de saponificación sin un conocimiento químico profundo y la debida precaución. La sosa cáustica (NaOH) es la base tradicionalmente empleada para provocar la reacción de saponificación que da lugar al jabón (una sal de ácidos grasos) y glicerina.
Innovación en la Producción de Sosa Cáustica
En la actualidad, la industria busca optimizar la producción de sosa cáustica a través de la innovación, la eficiencia y la sostenibilidad. Empresas como Welysis ofrecen soluciones modulares para integrar la producción de sosa cáustica de alta pureza directamente en las operaciones de sus clientes. Este enfoque no solo optimiza costos y asegura el suministro, sino que también promueve un modelo industrial más competitivo e independiente. El control directo sobre la producción de un químico tan fundamental se presenta como una ventaja estratégica insustituible en un mercado en constante evolución.
tags: #soda #caustica #hipoclorito #de #sodio