La interacción entre el ácido sulfúrico (H₂SO₄) y el hipoclorito de sodio (NaOCl) es una reacción química que, si bien puede parecer sencilla en su formulación, encierra complejidades y potenciales peligros que merecen una comprensión detallada. Este análisis busca desentrañar la naturaleza de esta reacción, sus productos, sus aplicaciones y las precauciones necesarias, basándose en observaciones experimentales y conocimientos químicos establecidos.
Fundamentos de la Reacción: Ácido Sulfúrico e Hipoclorito de Sodio
El ácido sulfúrico es un ácido mineral fuerte, conocido por su naturaleza corrosiva y su alta reactividad. Se utiliza en una vasta gama de aplicaciones industriales, desde la producción de fertilizantes hasta el refinado de petróleo y la fabricación de baterías. Su capacidad para donar protones lo convierte en un agente eficaz para neutralizar bases y catalizar diversas reacciones.
Por otro lado, el hipoclorito de sodio (NaOCl) es una sal derivada del ácido hipocloroso. Es ampliamente reconocido por sus propiedades desinfectantes y blanqueantes, siendo un componente común en productos de limpieza doméstica y en el tratamiento de aguas. Históricamente, su descubrimiento se remonta a alrededor de 1785, cuando el químico francés Berthollet desarrolló líquidos blanqueantes basados en este compuesto, que la compañía Javel introdujo al mercado como "licor de Javel", conocido aún hoy en Francia como 'eau de Javel'.
El hipoclorito de sodio se presenta típicamente como una solución acuosa de ligero color amarillento y un olor característico, a menudo descrito como similar al cloro. Su concentración en productos domésticos varía, con soluciones al 5% siendo comunes para blanqueamiento general, mientras que concentraciones más altas (10-15%) son más corrosivas y requieren mayor precaución. Una característica crucial del hipoclorito de sodio es su inestabilidad; se descompone con el tiempo, al calentarse, o en contacto con ácidos, luz solar, ciertos metales y gases corrosivos, liberando cloro.
La Reacción Química Específica: NaOCl + H₂SO₄
Cuando el ácido sulfúrico concentrado entra en contacto con el hipoclorito de sodio, se produce una reacción química vigorosa. La naturaleza exacta de esta reacción depende de las condiciones, pero generalmente implica la liberación de gases y la formación de subproductos.
Una de las reacciones esperadas, al mezclar un ácido fuerte como el sulfúrico con una sal de un ácido débil como el hipocloroso, es la protonación del ion hipoclorito (OCl⁻) para formar ácido hipocloroso (HOCl):
NaOCl + H₂SO₄ → HOCl + NaHSO₄ (o Na₂SO₄ dependiendo de la estequiometría)
Sin embargo, el ácido hipocloroso es inestable y puede descomponerse o reaccionar adicionalmente. En presencia de un ácido fuerte, también puede haber una reacción de oxidación-reducción. El hipoclorito de sodio es un oxidante fuerte. El ácido sulfúrico, en ciertas condiciones, puede actuar como agente reductor o facilitar la descomposición de otros compuestos.
La descripción experimental de un burbujeo similar a un refresco, seguido de un olor que no es a azufre sino a cloro o hidrógeno, y la formación de una sustancia amarilla, sugiere la liberación de gases y la posible formación de azufre elemental o compuestos de azufre. Si el gas no se quema fácilmente, es más probable que sea cloro o una mezcla de gases. La reacción detallada puede ser compleja, pero la liberación de cloro gaseoso (Cl₂) es una posibilidad significativa, especialmente si el ácido sulfúrico promueve la descomposición del ácido hipocloroso.
Una posible vía de reacción que explica la liberación de cloro es:
2NaOCl + H₂SO₄ → Cl₂ + Na₂SO₄ + H₂O
En esta reacción, el cloro gaseoso es liberado, lo cual es consistente con la descripción del olor y la dificultad para quemar el gas (a diferencia del hidrógeno). La sustancia amarilla observada podría ser azufre elemental (S), que se forma en reacciones secundarias o por la descomposición de compuestos de azufre.
Implicaciones y Peligros de la Reacción
La mezcla de ácido sulfúrico y hipoclorito de sodio es intrínsecamente peligrosa. El ácido sulfúrico es altamente corrosivo y puede causar quemaduras graves en la piel y los ojos, además de dañar el tracto respiratorio si se inhalan sus vapores. El hipoclorito de sodio, especialmente en concentraciones elevadas, también es corrosivo e irritante.
La liberación de cloro gaseoso (Cl₂) es una preocupación seria. El cloro es un gas tóxico y asfixiante que, incluso en bajas concentraciones, puede causar irritación severa en los ojos, la nariz y la garganta, tos y dificultad para respirar. La exposición prolongada o a altas concentraciones puede ser fatal. La experiencia de sentirse mareado tras oler la mezcla subraya la toxicidad del cloro.
Además de la liberación de cloro, la reacción puede generar calor significativo, lo que aumenta el riesgo de salpicaduras y la evaporación de sustancias peligrosas. La formación de compuestos de azufre, como el sulfuro de hidrógeno (H₂S), aunque menos probable en esta reacción directa con ácido sulfúrico concentrado y hipoclorito, es una posibilidad en mezclas más complejas o con impurezas, y el H₂S es conocido por su olor a huevo podrido y su alta toxicidad.
Aplicaciones y Contextos de Uso
Aunque la mezcla directa de ácido sulfúrico y hipoclorito de sodio no es una práctica común o recomendada debido a sus peligros, la comprensión de sus interacciones es relevante en varios contextos:
Tratamiento de Aguas Residuales: En algunas aplicaciones industriales, se utilizan agentes oxidantes como el hipoclorito de sodio para neutralizar compuestos malolientes como el sulfuro de hidrógeno (H₂S) y el amoníaco (NH₃). Si bien el ácido sulfúrico no se añade directamente para este propósito, su presencia como contaminante o subproducto en aguas residuales podría interactuar con el hipoclorito. El hipoclorito de sodio también se utiliza para la desinfección del agua, un proceso donde el pH juega un papel crucial. Se ha mencionado que el ácido acético o el ácido sulfúrico se pueden usar para disminuir el pH, facilitando la formación de ácido hipocloroso (HOCl), que es el principal agente desinfectante. Sin embargo, se advierte que el uso de ácido sulfúrico en este contexto puede generar gases dañinos, aunque en menor cantidad que con otros ácidos.
Limpieza Industrial y Doméstica: El hipoclorito de sodio es un agente blanqueante y desinfectante doméstico. El ácido sulfúrico se utiliza en productos de limpieza para baños y desagües, a menudo formulado para eliminar óxido y depósitos minerales. La advertencia implícita es nunca mezclar productos de limpieza que contengan hipoclorito de sodio con limpiadores ácidos (como los que contienen ácido sulfúrico o clorhídrico), ya que esto liberaría cloro gaseoso tóxico. La observación del usuario sobre la reacción en la batea, donde el ácido sulfúrico reaccionaba con restos de hipoclorito, ilustra precisamente este peligro potencial en entornos domésticos o de laboratorio.
Síntesis Química: En entornos de laboratorio controlados, las reacciones de oxidación-reducción y la generación de gases como el cloro pueden ser de interés para la síntesis de otros compuestos. Sin embargo, esto requiere un conocimiento profundo de la química, equipos de seguridad adecuados (campanas de extracción, equipos de protección personal) y protocolos rigurosos.
El Papel del pH y la Formación de Especies Activas
El pH de la solución es un factor determinante en la eficacia desinfectante del hipoclorito de sodio. Al disolver NaOCl en agua, se establece un equilibrio:
NaOCl + H₂O ⇌ HOCl + NaOH
El ácido hipocloroso (HOCl) es el agente desinfectante y oxidante más potente. El ion hipoclorito (OCl⁻) es menos efectivo. El pH influye en la proporción de HOCl a OCl⁻:
- A pH bajo (ácido), predomina el HOCl, maximizando la desinfección.
- A pH alto (alcalino), predomina el OCl⁻, reduciendo la eficacia.
Por esta razón, en aplicaciones como el tratamiento de piscinas, a menudo se ajusta el pH. Si bien el hipoclorito de sodio en sí mismo tiende a elevar el pH debido a la formación de NaOH, la adición de ácidos como el acético o el sulfúrico se emplea para mantener el pH en un rango óptimo para la desinfección. La mención de que el ácido sulfúrico produce "menor producción de gases dañinos" en comparación con el ácido acético es una afirmación que requiere matización; ambos pueden liberar gases peligrosos si la reacción es inadecuada o si se producen reacciones secundarias indeseadas. La reacción de NaOCl con H₂SO₄, como se describió anteriormente, puede liberar cloro, un gas muy dañino.
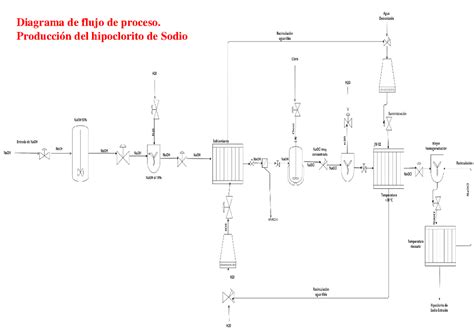
Métodos de Producción y Aplicación de Hipoclorito de Sodio
El hipoclorito de sodio se puede producir de diversas maneras:
Electrólisis de Salmuera: Disolviendo sal (NaCl) en agua blanda y sometiendo la solución a electrólisis. Las reacciones en los electrodos generan cloro gas (Cl₂) y hidróxido de sodio (NaOH). Posteriormente, el cloro reacciona con el hidróxido de sodio para formar hipoclorito de sodio:
- 2Cl⁻ → Cl₂ + 2e⁻ (en el ánodo)
- 2H₂O + 2e⁻ → H₂ + 2OH⁻ (en el cátodo)
- OH⁻ + Cl₂ → HOCl + Cl⁻ (formación de ácido hipocloroso, que luego se equilibra con OCl⁻ y NaOH)
Una ventaja de este método, especialmente la electrólisis "in situ" (en el lugar de uso), es que evita el transporte y almacenamiento de hipoclorito de sodio, que es inestable y puede volverse inactivo con el tiempo. Sin embargo, la producción de gas hidrógeno (H₂) es un riesgo de explosión que requiere ventilación adecuada. Los sistemas de electrólisis también implican un costo inicial y de mantenimiento mayor que la compra de hipoclorito de sodio prefabricado. La producción en el sitio a través de electrólisis puede ayudar a mantener bajos los niveles de pH, reduciendo la necesidad de ácidos adicionales.
Adición de Cloro Gas a Soda Cáustica: La reacción directa entre cloro gas (Cl₂) y una solución de hidróxido de sodio (NaOH) produce hipoclorito de sodio, cloruro de sodio (NaCl) y agua:
- Cl₂ + 2NaOH → NaOCl + NaCl + H₂O
Este método es común en la producción industrial a gran escala.
Aplicaciones Diversas del Hipoclorito de Sodio
El hipoclorito de sodio tiene un espectro de aplicaciones muy amplio, abarcando múltiples sectores industriales y de consumo:
- Industria Textil: Como agente blanqueante para fibras y tejidos.
- Tratamiento de Aguas: Desinfección de aguas potables y residuales, eliminación de olores (neutralizando H₂S y NH₃), prevención del crecimiento de algas en torres de enfriamiento.
- Industria Alimentaria: Desinfección de superficies y equipos.
- Industria Química y Farmacéutica: Como reactivo o agente de limpieza.
- Minería y Metalurgia: Desintoxicación de baños de cianuro.
- Fabricación de Papel: Blanqueamiento de pulpa de madera.
- Limpieza Doméstica: Desinfección general, blanqueo de ropa, eliminación de moho y olores.
En piscinas, el hipoclorito de sodio se utiliza para desinfectar el agua y oxidar contaminantes orgánicos (como sudor, orina y cosméticos). La concentración requerida depende de la carga de contaminantes. La filtración previa del agua puede reducir la cantidad de hipoclorito necesaria.
Efectos para la Salud y Consideraciones de Seguridad
La exposición al hipoclorito de sodio, incluso en concentraciones bajas, puede tener efectos adversos para la salud. Los valores límite de exposición están establecidos para proteger a los trabajadores.
- Inhalación: Puede causar tos, dolor de garganta y daño al tracto respiratorio. La formación de cloraminas (por reacción con amoníaco presente en la orina y el sudor) en piscinas es una causa común de irritación ocular y del sistema respiratorio, produciendo el característico "olor a cloro".
- Ingestión: Provoca dolor de estómago, quemazón, tos, diarrea y vómitos.
- Contacto con Piel y Ojos: Causa enrojecimiento, irritación y daños. La exposición prolongada puede hacer la piel sensible.
- Toxicidad Ambiental: Es tóxico para la vida acuática. Cuando se combina con sales de amonio, puede formar compuestos muy tóxicos y mutagénicos.
Es fundamental destacar que el hipoclorito de sodio, al igual que el cloro gaseoso, no desactiva eficazmente ciertos patógenos resistentes como Giardia lamblia o Cryptosporidium.
La legislación sobre el hipoclorito de sodio suele equipararse a la del cloro en términos de manejo y seguridad.
[TUTORIAL] Manejo de Productos de Limpieza
Conclusión Provisional sobre la Reacción
La reacción entre el ácido sulfúrico y el hipoclorito de sodio es una demostración clara de la reactividad de estos compuestos y de los peligros inherentes a la mezcla de sustancias químicas sin conocimiento previo. La liberación de cloro gaseoso es el resultado más preocupante y potencialmente peligroso. La observación experimental de un joven químico aficionado, aunque arriesgada, ilustra la importancia de la precaución y el conocimiento en cualquier manipulación química. La comprensión de las propiedades del hipoclorito de sodio, su inestabilidad, su interacción con ácidos y su papel en diversas aplicaciones, subraya la necesidad de un manejo responsable y seguro, tanto en entornos industriales como domésticos. La advertencia contra la mezcla de productos de limpieza es, en este contexto, de vital importancia.
tags: #valoracion #hipoclorito #de #sodio #con #sulfurico