El agua, sustancia fundamental para la vida y omnipresente en el laboratorio, adquiere un rol protagónico en técnicas analíticas de alta sensibilidad como la Cromatografía Líquida de Alto Rendimiento (HPLC). La pureza del agua utilizada en estos procesos es un factor determinante para la exactitud y fiabilidad de los resultados, ya que actúa como disolvente, componente de la fase móvil y en la preparación de soluciones y estándares. En el contexto del HPLC, el término "agua destilada" a menudo se refiere a agua "purificada", sometida a rigurosos procesos para eliminar impurezas orgánicas e inorgánicas que podrían interferir con las separaciones y detecciones.
La Naturaleza del Agua: Un Disolvente Universal
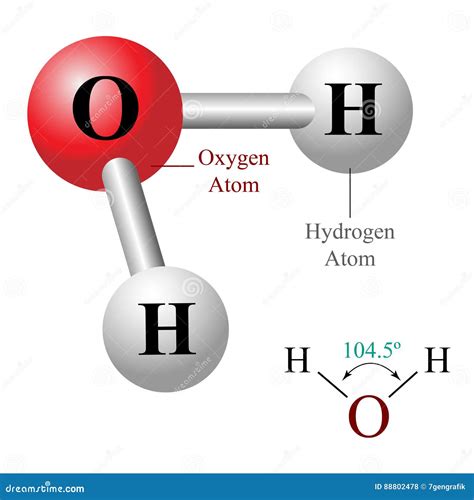
El agua, cuya fórmula química es H2O, es una sustancia inorgánica y polar. A temperatura ambiente, se presenta como un líquido transparente, insípido e inodoro, con un ligero matiz azul que no es perceptible en pequeñas cantidades. Su estructura molecular, compuesta por un átomo de oxígeno y dos de hidrógeno unidos por enlaces covalentes, le confiere propiedades únicas. El átomo de oxígeno, al ser altamente electronegativo, atrae los electrones compartidos con mayor fuerza que el hidrógeno, generando una distribución asimétrica de la densidad electrónica. Esta polaridad resulta en un momento dipolar eléctrico significativo, lo que permite a las moléculas de agua establecer fuertes interacciones electrostáticas con otras moléculas polares o átomos cargados.
La capacidad del agua para formar "enlaces de hidrógeno" entre sus propias moléculas y con otras sustancias es la clave de su excepcional poder disolvente. Estos enlaces, una forma especial de interacción dipolo-dipolo fuerte, se forman cuando el hidrógeno, unido a un átomo electronegativo como el oxígeno, es atraído hacia el extremo negativo de una molécula polar o hacia un par de electrones solitarios. Esta afinidad permite al agua disolver una vasta gama de sustancias, clasificadas como "hidrófilas", que son aquellas polares y capaces de formar enlaces de hidrógeno o interacciones ión-dipolo. Ejemplos de solutos hidrófilos incluyen sales, azúcares y ácidos. Por el contrario, las sustancias "hidrofóbicas", como las grasas y aceites, al ser no polares, no se disuelven bien en agua.
El agua es un disolvente inorgánico, polar y prótico, lo que significa que no contiene carbono, presenta un dipolo permanente y puede donar protones (H+) a los solutos. Es el disolvente más importante para los seres vivos y el líquido que más sustancias disuelve. El agua es una de las pocas sustancias que se encuentra de forma natural en los tres estados de la materia: sólido (hielo), líquido (agua) y gaseoso (vapor de agua). Constituye el principal componente de la hidrosfera terrestre y de los fluidos de todos los organismos vivos.
Propiedades Físicas del Agua y su Relevancia Analítica
Las propiedades físicas del agua, como su punto de fusión, punto de ebullición y densidad, aunque parezcan básicas, tienen implicaciones en su uso y purificación. El punto de fusión del agua pura a 1 atmósfera de presión se aproxima a 0 °C (273.15 K), mientras que su punto de ebullición es de 100 °C (373.15 K) a la misma presión. Sin embargo, estos valores pueden variar ligeramente en función de la presión atmosférica y la presencia de impurezas. Por ejemplo, el agua con impurezas, como el agua salada, hierve a una temperatura más alta.
La densidad máxima del agua se alcanza a 3.98 °C, siendo de 1.00000 g/mL. Esta propiedad, junto con su polaridad, influye en cómo interactúa con otras sustancias durante los procesos de separación y análisis.
La ionización del agua, aunque mínima, es un aspecto fundamental. El agua puede actuar como ácido al donar un protón (H+) y como base al aceptarlo, dando lugar a las especies iónicas hidronio (H3O+) y hidroxilo (OH-). En agua pura a 25 °C, la concentración de ambas especies es igual (1.0 x 10^-7 M), lo que resulta en una solución neutra con un pH de 7. La constante de disociación del agua, Kw = [H+][OH-] = 1.0 x 10^-14, indica el equilibrio de esta ionización. Cualquier impureza que altere estas concentraciones de iones puede afectar la neutralidad del agua.
Ionización del agua y su relación con el pH
La Importancia de la Pureza del Agua en HPLC
En la Cromatografía Líquida de Alto Rendimiento (HPLC), la pureza del agua es un requisito indispensable. Las impurezas, incluso en concentraciones muy bajas, pueden tener efectos significativos en el análisis:
- Interferencia en la Detección: Las impurezas pueden absorber luz UV o fluorescente, generando picos en el cromatograma que enmascaran los analitos de interés o provocan señales falsas. Por ejemplo, un gradiente a 210 nm con una absorbancia máxima permitida de 0.01 mUA y a 254 nm de 0.5 mUA indica la necesidad de una transparencia UV excepcional. La fluorescencia a 254 nm en quinina de 1 ppb y a 365 nm de 0.5 ppb resalta la sensibilidad requerida para detectar incluso trazas de impurezas fluorescentes.
- Alteración de la Fase Móvil: La presencia de iones o solutos disueltos puede modificar la polaridad y la fuerza eluyente de la fase móvil, afectando la separación de los compuestos. Una conductancia específica a 25 °C de 1.0 x 10^-6 ohm^-1 cm^-1 es un indicador de la mínima presencia de iones disueltos.
- Daño a la Columna Cromatográfica: Las partículas o iones presentes en el agua pueden obstruir los poros de la columna o reaccionar con la fase estacionaria, reduciendo su vida útil y el rendimiento del análisis.
- Resultados Inexactos: Las impurezas pueden reaccionar con los analitos o actuar como contaminantes, llevando a cuantificaciones erróneas o identificaciones incorrectas.
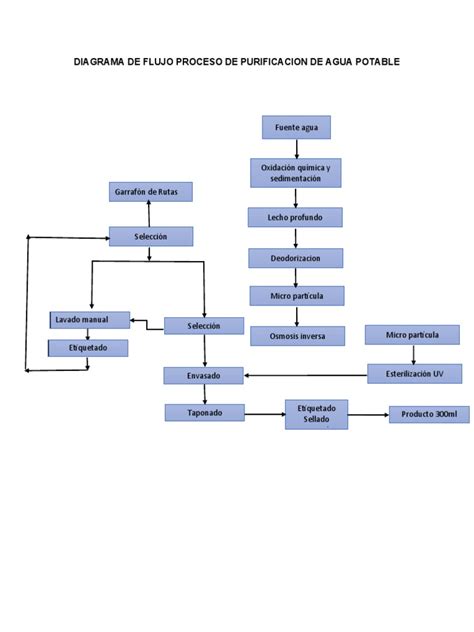
Para garantizar la pureza necesaria, se emplean diversas técnicas de purificación, como la destilación, la ultrafiltración, la ósmosis inversa y la desionización, a menudo en combinación. El agua utilizada en laboratorios, comúnmente denominada "agua destilada", es en realidad agua "purificada" mediante estos métodos.
Especificaciones y Grados de Pureza para HPLC
La calidad del agua para aplicaciones analíticas está definida por organismos normalizadores como la ISO (ISO 3696) y la ASTM (ASTM D1193), así como por farmacopeas (EP, Ph. Eur.). Estas normativas establecen las especificaciones para diferentes grados de pureza del agua, adaptados a diversas aplicaciones.
Para HPLC, se requieren grados de agua con especificaciones rigurosas:
- Residuo Fijo: Un límite máximo de 0.0001% indica la ausencia casi total de sólidos disueltos.
- Impurezas Iónicas: Límites extremadamente bajos para cloruro (Cl: 0.000001%), sulfato (SO4: 0.00001%), fluoruro (F: 0.000001%) y nitrato (NO3: 0.00001%) son cruciales para evitar interferencias en la detección y la estabilidad de la fase móvil.
- Absorbancia UV: La baja absorbancia en el rango UV (por ejemplo, Amax: 0.01 a 205 nm y 210 nm, y 0.005 a 250-400 nm) es vital para la detección sensible de analitos, especialmente en gradientes cromatográficos.
- Contenido de Metales y Compuestos Orgánicos: Para técnicas como LC-MS, se requiere agua compatible, implicando un control estricto de metales y compuestos orgánicos. El ensayo "LC-MS: Conforme" asegura la aptitud para esta técnica sensible.
Aplicaciones Específicas del Agua de Alta Pureza
El agua de alta pureza encuentra aplicación en diversas áreas dentro del laboratorio, más allá de ser un simple disolvente:
- Fase Móvil en Cromatografía: Es un componente esencial de la fase móvil en técnicas como HPLC, UHPLC (Cromatografía Líquida de Ultra Alto Rendimiento) y LC-MS. Para UHPLC, que ofrece análisis más rápidos y mayor resolución, se requiere agua con alta transparencia a longitudes de onda bajas y máxima estabilidad de línea de base.
- Preparación de Soluciones Estándar y Tampones: La preparación de soluciones de referencia y tampones para procesos como la lisis celular o el ajuste del pH es crítica. La pureza del agua asegura la exactitud de las concentraciones y la estabilidad de estas soluciones.
- Análisis de Trazas Metálicas: Para análisis de ultra-trazas de metales mediante ICP-MS, se utiliza agua especialmente purificada (a menudo por destilación múltiple) con límites de detección en el rango de partes por billón (ppb) o partes por trillón (ppt).
- Limpieza y Lavado: Aunque el agua de grado reactivo es costosa, su uso para el lavado final de material de vidrio o equipos críticos puede ser necesario para evitar la contaminación residual.
Consideraciones sobre la Selección y Manipulación
La elección del grado de agua adecuado depende directamente de la aplicación analítica. El agua para HPLC, por ejemplo, debe cumplir con las especificaciones mencionadas para garantizar la calidad del análisis. La formulación "Agua para UV, HPLC, ACS" indica su idoneidad como disolvente polivalente para HPLC y espectroscopia UV-Vis/IR. El agua para UHPLC, con especificaciones aún más estrictas, es apropiada para esta técnica avanzada.
El envasado del agua de alta pureza también es importante. Las botellas de disolvente de diseño avanzado, como las de 4L con tecnología de sellado mejorada, están diseñadas para minimizar fugas y garantizar la seguridad y conveniencia en su manipulación. La filtración a través de un filtro de 0.2 μm antes de su uso es una práctica común para eliminar partículas finas.
En resumen, el agua destilada o purificada para HPLC no es simplemente H2O, sino un reactivo de alta tecnología cuya pureza es fundamental para obtener resultados analíticos precisos y fiables en el complejo mundo de la química analítica. Su selección, manipulación y uso adecuado son pilares para el éxito de cualquier investigación o control de calidad que dependa de técnicas cromatográficas.