El agua, esa sustancia omnipresente que cubre el 71% de la superficie terrestre, es mucho más que un simple líquido. Su estructura atómico-molecular única, H2O, es la clave de sus extraordinarias propiedades, que la convierten en el pilar fundamental para la vida en nuestro planeta. Desde su estado líquido fluyendo por ríos hasta su forma sólida en los polos, el agua desempeña roles insustituibles en los ecosistemas y en la salud humana.
Composición y Estructura Molecular del Agua
La molécula de agua, formalmente conocida como oxidano, se compone de dos átomos de hidrógeno (H) unidos a un átomo de oxígeno (O) mediante enlaces covalentes. Sin embargo, la disposición de estos átomos no es lineal; forman una estructura angular. El átomo de oxígeno, con una electronegatividad significativamente mayor que la del hidrógeno, atrae los electrones compartidos con mayor fuerza. Esta distribución desigual de la carga eléctrica genera una polaridad en la molécula: el átomo de oxígeno adquiere una carga parcial negativa, mientras que los átomos de hidrógeno presentan cargas parciales positivas. Esta polaridad es fundamental y explica muchas de las propiedades anómalas y vitales del agua.
Henry Cavendish, en 1782, fue el primero en descubrir que la molécula de agua estaba formada por dos elementos: un átomo de oxígeno y dos de hidrógeno. La estructura angular, con un ángulo de aproximadamente 104.45°, no es una casualidad. Se debe a la hibridación del átomo de oxígeno y a la presencia de dos pares de electrones no enlazantes que repelen a los enlaces H-O. Esta geometría dipolar, con cargas negativas concentradas en el vértice del ángulo (donde está el oxígeno) y cargas positivas en los extremos (donde están los hidrógenos), permite que las moléculas de agua se atraigan fuertemente entre sí.
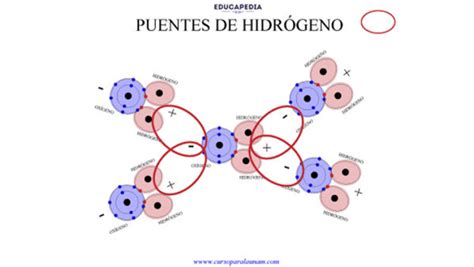
Puentes de Hidrógeno
Propiedades Únicas del Agua Derivadas de su Estructura
La polaridad del agua y su capacidad para formar enlaces por puentes de hidrógeno son la base de sus propiedades distintivas:
Solvente Universal: El agua es descrita frecuentemente como el "solvente universal" debido a su excepcional capacidad para disolver una vasta gama de sustancias. Su naturaleza polar le permite interactuar con compuestos iónicos y polares, como las sales (por ejemplo, el cloruro de sodio), los azúcares y muchos alcoholes, formando disoluciones moleculares. Sin embargo, no disuelve de manera apreciable sustancias fuertemente apolares, como el azufre en sus formas alotrópicas más comunes, y es inmiscible con disolventes apolares como el hexano. Esta selectividad es crucial en los procesos biológicos y químicos. La capacidad de disolver sustancias se debe a la polaridad de la molécula de agua y a su capacidad de formar enlaces por puentes de hidrógeno con otras sustancias que presenten grupos polares o cargas iónicas.
Cohesión y Tensión Superficial: La cohesión, la atracción entre moléculas de agua, es una consecuencia directa de los puentes de hidrógeno. Estos enlaces mantienen las moléculas fuertemente unidas, haciendo que el agua sea un líquido casi incompresible. Esta incompresibilidad permite que algunos animales, como ciertos gusanos perforadores, utilicen el agua como un esqueleto hidrostático para generar presión y realizar trabajos mecánicos. La cohesión en la superficie del agua genera una elevada tensión superficial. Esta propiedad actúa como una fina película elástica, capaz de soportar objetos ligeros e incluso permitir que insectos y pequeños animales caminen sobre ella sin hundirse. Las gotas de agua, esféricas por naturaleza, son también una manifestación de esta alta tensión superficial.
Capilaridad: La capilaridad es la propiedad por la cual el agua puede ascender o descender dentro de un tubo capilar. Cuando un capilar se introduce en agua, esta asciende espontáneamente, "agarrándose" a las paredes del tubo, hasta que la presión ejercida por la columna de agua se equilibra con la presión capilar. Esta propiedad, íntimamente ligada a la capacidad del agua para formar puentes de hidrógeno intermoleculares y a su adhesión a otras superficies polares, es vital para el transporte de agua en las plantas, desde las raíces hasta las hojas.
Alto Calor Específico y Calor Latente: El agua posee una capacidad excepcional para absorber grandes cantidades de calor con un aumento relativamente pequeño de su temperatura. Esto se debe a que gran parte de la energía absorbida se utiliza para romper los puentes de hidrógeno. Esta propiedad la convierte en un excelente regulador térmico, tanto a nivel planetario (suavizando las temperaturas en las zonas costeras) como a nivel biológico (protegiendo a los organismos de cambios bruscos de temperatura). De manera similar, se requiere una cantidad considerable de energía para evaporar el agua, ya que primero deben romperse los puentes de hidrógeno y luego las moléculas deben adquirir suficiente energía cinética para pasar a estado gaseoso. El punto de ebullición del agua es de 100 °C (373.15 K) a 1 atmósfera de presión, y su punto de fusión es de 0 °C (273.15 K) a la misma presión.
Densidad Anómala del Hielo: Una de las propiedades más sorprendentes del agua es que su forma sólida (hielo) es menos densa que su forma líquida. Al congelarse, las moléculas de agua se organizan en una estructura cristalina de tetraedros, formada por puentes de hidrógeno. Esta estructura es muy abierta y poco compacta, lo que resulta en una menor densidad. Esta dilatación del agua al solidificarse tiene profundas implicaciones: el hielo flota sobre el agua, aislando las capas inferiores y permitiendo la supervivencia de la vida acuática en climas fríos. Además, la expansión del agua al congelarse contribuye a procesos geológicos de erosión.
El Ciclo del Agua: Un Proceso Bioquímico Fundamental
El ciclo hidrológico, o ciclo del agua, es uno de los procesos bioquímicos más importantes para la salud del planeta. Este ciclo continuo se compone de varias etapas interconectadas:
- Evaporación: La energía solar calienta las superficies acuáticas (océanos, ríos, lagos), provocando que el agua se evapore y ascienda a la atmósfera en forma de vapor.
- Condensación: A medida que el vapor de agua se enfría en las capas altas de la atmósfera, sus moléculas pierden movilidad y se unen sobre partículas sólidas suspendidas en el aire (núcleos de condensación), formando nubes.
- Precipitación: Cuando las gotas de agua o los cristales de hielo en las nubes alcanzan un tamaño suficiente, caen a la superficie terrestre en forma de lluvia, nieve, granizo o aguanieve.
- Derretimiento y Aguas Escurridas: Una vez en la superficie, el agua puede derretirse (si cae en forma de nieve o hielo) y escurrirse, formando arroyos, ríos y alimentando cuerpos de agua subterránea, para finalmente regresar a los océanos, reiniciando el ciclo.
El vapor de agua y el dióxido de carbono en la atmósfera juegan un papel crucial en el efecto invernadero, manteniendo la temperatura superficial de la Tierra relativamente constante y permitiendo la existencia de agua líquida.
La Distribución del Agua en el Planeta y el Acceso al Agua Potable
A pesar de que el 71% de la superficie terrestre está cubierta por océanos, la mayor parte de esta agua es salada y no apta para el consumo directo. Solo el 2.5% del agua total del planeta es agua dulce. De esta pequeña fracción, cerca del 70% se encuentra congelada en los polos, nieves y glaciares. Como resultado, apenas un 1% del agua dulce total está disponible en forma líquida y accesible en la superficie.
La escasez de agua potable es un problema global crítico. El organismo internacional estimaba que 884 millones de personas no contaban con acceso a agua potable. En respuesta, las Naciones Unidas aprobaron la Agenda 2030 sobre el Desarrollo Sostenible, con el Objetivo de Desarrollo Sostenible número 6, que busca lograr el acceso universal y equitativo al agua potable, así como garantizar servicios de saneamiento e higiene adecuados. La pandemia mundial de COVID-19 evidenció aún más la importancia vital del saneamiento y la higiene, siendo el lavado de manos una medida fundamental para prevenir la propagación de enfermedades.
Agua Destilada: Pureza y Aplicaciones
El agua destilada es agua que ha sido purificada mediante el proceso de destilación, que imita el ciclo natural de evaporación y condensación. Este método elimina minerales, sales y otros contaminantes, resultando en un líquido de alta pureza. La fórmula química del agua destilada es, al igual que el agua común, H2O.
Proceso de Destilación:
- Preparación: Se utiliza un equipo de destilación, que incluye un recipiente para hervir el agua, un tubo conductor de vapor y un condensador.
- Hervido: El agua común se calienta hasta su punto de ebullición, convirtiéndose en vapor.
- Condensación: El vapor asciende y se enfría en el condensador, volviendo a su estado líquido, pero ahora purificado.
- Recolección: El agua destilada se recoge en un recipiente limpio.

¿Es Seguro Beber Agua Destilada?
Si bien beber agua destilada en cantidades moderadas no suele ser perjudicial, su consumo excesivo es objeto de debate. Su pureza extrema implica la ausencia de minerales esenciales para el cuerpo. Aunque hidrata, no aporta nutrientes, y su consumo prolongado podría teóricamente llevar a desequilibrios electrolíticos si no se compensa con una dieta rica en minerales. Por ello, para el consumo humano, se prefieren otras formas de agua purificada que conserven minerales beneficiosos, como el agua de ósmosis inversa.
Usos del Agua Destilada:
La alta pureza del agua destilada la hace invaluable en una amplia gama de aplicaciones:
- Laboratorio y Medicina: Preparación de soluciones, calibración de equipos, fabricación de medicamentos y productos farmacéuticos.
- Industria: Electrónica, automotriz, alimentaria, textil, fabricación de productos químicos y de limpieza de componentes electrónicos.
- Hogar y Cuidado Personal: Planchas de vapor (evita depósitos minerales), baterías de plomo-ácido, cosméticos, limpieza de cristales (sin dejar marcas), riego de plantas sensibles, preparación de alimentos para bebés.
- Higiene: Enjuagues bucales y limpieza de prótesis dentales.
- Acuarios y Terrarios: Para mantener condiciones específicas del agua.
¿Cómo Hacer Agua Destilada en Casa?
Es posible obtener agua destilada casera utilizando una olla grande, un recipiente más pequeño que flote dentro, una tapa invertida y hielo. Al hervir el agua de la olla, el vapor se condensa en la tapa fría (cubierta con hielo) y gotea en el recipiente interior, separándose de las impurezas.
El Agua como Factor Clave para la Vida
La presencia de agua líquida en la Tierra, junto con la distancia adecuada al Sol y una atmósfera propicia, ha sido fundamental para el origen y la evolución de la vida. El agua no es solo un medio para el metabolismo de las biomoléculas, sino que su estructura molecular dinámica y su capacidad para interactuar con ellas son esenciales para los procesos biológicos. La búsqueda de vida en otros mundos se centra, en gran medida, en la detección de agua. A pesar de siglos de estudio, el agua sigue revelando aspectos fascinantes, como las complejas interacciones moleculares en su superficie, que continúan siendo objeto de investigación. El agua, en su aparente simplicidad, es un compuesto extraordinario que sustenta la existencia tal como la conocemos.