El agua, esa sustancia tan omnipresente en nuestra vida cotidiana que a menudo pasa desapercibida, es en realidad un compuesto de asombrosa complejidad y vital importancia. Desde la sed que saciamos hasta los vastos océanos que cubren gran parte de nuestro planeta, el agua es fundamental para la supervivencia de toda forma de vida conocida. Más allá de su utilidad básica, el agua presenta una serie de propiedades físicas y químicas únicas que la distinguen y la hacen indispensable para innumerables procesos naturales y aplicaciones humanas. Comprender su estructura molecular, las interacciones entre sus moléculas y su comportamiento en la naturaleza nos permite apreciar su verdadero valor y los desafíos asociados a su pureza y disponibilidad.
La Molécula de Agua: H₂O y sus Enlaces
A nivel molecular, el agua es un compuesto químico inorgánico cuya fórmula, H₂O, nos revela su composición fundamental: dos átomos de hidrógeno (H) unidos a un átomo de oxígeno (O). Estos átomos se enlazan mediante un enlace covalente, una unión fuerte y estable donde los átomos comparten pares de electrones. Los átomos de hidrógeno involucrados son, en su gran mayoría, el isótopo protio, conocido como Hidrógeno-1. Si bien existen otras formas isotópicas menos comunes, como el deuterio (con un protón y un neutrón) y el tritio (con un protón y dos neutrones), estas no definen la molécula de agua común. El agua con una proporción elevada de deuterio se denomina agua pesada, y aquella con mayor contenido de tritio, además de ser radiactiva, se conoce como superpesada, constituyendo un tema de estudio aparte.
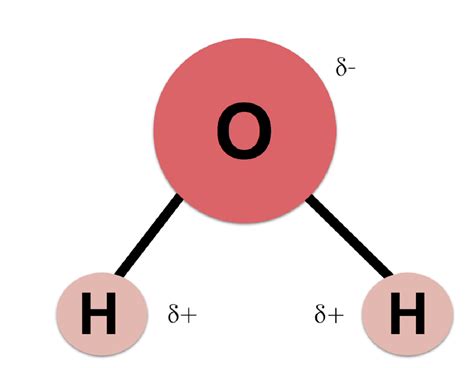
La particularidad de la molécula de agua reside en la electronegatividad del átomo de oxígeno. Este átomo atrae los electrones del enlace covalente con mucha más fuerza que los átomos de hidrógeno. Como resultado, el oxígeno adquiere una carga parcial negativa, mientras que los hidrógenos desarrollan una carga parcial positiva. Esta distribución desigual de carga genera un momento dipolar en la molécula de agua, convirtiéndola en una molécula polar.
Esta polaridad es la clave para la formación de los puentes de hidrógeno. A diferencia del enlace covalente, los puentes de hidrógeno son enlaces relativamente débiles que se establecen entre el átomo de hidrógeno de una molécula de agua y el átomo de oxígeno de otra molécula adyacente. Estos enlaces se rompen y forman constantemente, pero son los responsables de muchas de las propiedades físicas distintivas del agua, como sus altos puntos de fusión y ebullición, su elevada tensión superficial y el peculiar comportamiento del hielo al flotar en agua líquida. Cada molécula de agua puede formar hasta cuatro puentes de hidrógeno.
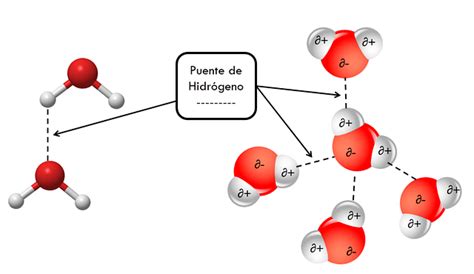
La fuerza de estos puentes de hidrógeno explica por qué el agua es líquida en condiciones ambientales estándar. Se requiere una cantidad considerable de energía para romper estos enlaces y permitir que las moléculas de agua pasen al estado gaseoso. Por el contrario, en estado sólido, las moléculas de agua se organizan en una estructura cristalina de tipo tetraedro, donde cada molécula se une a otras cuatro mediante enlaces de hidrógeno. Esta estructura, al ser muy abierta y poco compacta, hace que el hielo sea menos denso que el agua líquida, provocando que flote. Este fenómeno tiene profundas implicaciones geológicas, como la erosión.
Además de su comportamiento en los puentes de hidrógeno, el agua posee una propiedad química fundamental: es anfótera. Esto significa que puede actuar tanto como ácido como base en reacciones químicas, una característica que la convierte en un medio excepcional para una vasta gama de procesos bioquímicos.
Propiedades Físicas del Agua: Un Solvente Extraordinario
El agua es descrita frecuentemente como el "solvente universal" debido a su excepcional capacidad para disolver una gran cantidad de sustancias, tanto sólidas, líquidas como gaseosas. Su naturaleza polar le permite disolver eficazmente compuestos iónicos y polares, como la sal de mesa (cloruro de sodio). Los iones de sodio y cloruro se rodean de moléculas de agua, separándose del cristal y disolviéndose. Sin embargo, el agua no disuelve de manera apreciable sustancias fuertemente apolares, como el azufre, y es inmiscible con disolventes apolares como el hexano. Esta selectividad se debe a su capacidad para formar puentes de hidrógeno con otras sustancias que presentan grupos polares o cargas iónicas, como alcoholes, azúcares, aminoácidos y proteínas, dando lugar a disoluciones moleculares.
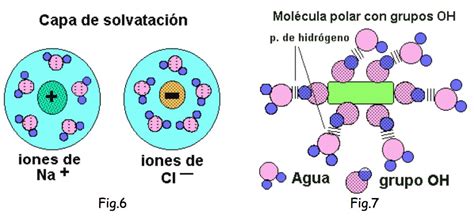
Esta propiedad de disolución es crucial para la vida, ya que permite el transporte de nutrientes y la eliminación de desechos en los organismos vivos. El citoplasma acuoso de las células, por ejemplo, actúa como un medio para las reacciones metabólicas. Sin embargo, esta misma cualidad también es la causa de la contaminación del agua. La desintegración de materiales como el plástico o la madera arrojados al agua puede liberar sustancias peligrosas que circulan libremente, afectando a la vida acuática. Del mismo modo, los naufragios y el vertido de sustancias químicas complejas representan fuentes significativas de contaminación.
Propiedades Clave del Agua:
- Alta Tensión Superficial: Debido a la cohesión entre sus moléculas (la atracción entre ellas), la superficie del agua se comporta como una película elástica. Esto permite que objetos ligeros floten, que insectos caminen sobre ella e incluso que animales como el basilisco corran sobre la superficie. La formación de gotas estables también es una consecuencia de esta propiedad.
- Capilaridad: El agua tiene la capacidad de ascender o descender dentro de tubos capilares. Al introducir un capilar en agua, esta asciende "agarrándose" a las paredes del tubo hasta que la presión de la columna de agua se equilibra con la presión capilar. Esta propiedad, relacionada con los puentes de hidrógeno, es vital para el transporte de agua en las plantas y en el suelo.
- Alto Calor Específico: El agua puede absorber grandes cantidades de calor antes de que su temperatura aumente significativamente. Esto se debe a que la energía absorbida se utiliza para romper los puentes de hidrógeno. Esta propiedad la convierte en un excelente regulador térmico, tanto a nivel planetario (suavizando las temperaturas en zonas costeras) como en los organismos vivos (protegiendo las células de cambios bruscos de temperatura).
- Alto Calor Latente de Vaporización: Se necesita una gran cantidad de energía para evaporar el agua. Primero, se deben romper los puentes de hidrógeno, y luego, las moléculas deben adquirir suficiente energía cinética para pasar del estado líquido al gaseoso.
- Puntos de Fusión y Ebullición: A presión atmosférica estándar (nivel del mar), el agua se congela a 0 °C y hierve a 100 °C. Sin embargo, investigaciones recientes sugieren que el hielo no se solidifica completamente hasta los -13 °C, momento en el cual su estructura molecular cambia definitivamente.
¿Que es la tensión superficial?
El Concepto de Agua Pura: ¿Mito o Realidad?
La idea de "agua pura" es, en términos científicos, aquella que está compuesta exclusivamente por moléculas de H₂O, libre de cualquier otra sustancia disuelta, como minerales, gases o microorganismos. Sin embargo, obtener agua en este estado de pureza absoluta es prácticamente imposible fuera de laboratorios con condiciones de experimentación extremadamente controladas y, a menudo, utilizando vacío.
La profesora May Nyman, de la Universidad Estatal de Oregón, explica que la naturaleza polar del agua y su capacidad para formar puentes de hidrógeno le confieren una afinidad intrínseca por disolver casi cualquier sustancia con la que entra en contacto. Incluso el agua considerada "ultrapura" en entornos de laboratorio contiene trazas de otras sustancias.
Agua Potable vs. Agua Pura:
Es crucial distinguir entre agua potable y agua pura. El agua que llega a nuestros hogares a través de la red de suministro es agua potable, lo que significa que ha sido tratada para garantizar su seguridad e higiene para el consumo humano. Sin embargo, este tratamiento a menudo implica la adición de productos químicos para cumplir con los estándares de salubridad. Estos pueden incluir fungicidas, conservantes, antioxidantes, colorantes, gases, restos de medicamentos, metales pesados, estabilizantes, suavizantes, saborizantes, insecticidas, herbicidas y emulsionantes. Aunque se regulan en concentraciones que no deberían suponer un riesgo para la salud, su presencia compromete la pureza absoluta del agua y puede afectar su sabor y calidad. Muchas de estas sustancias pueden estar presentes de forma natural (como el fluoruro, hierro, aluminio y sulfatos) o ser de origen artificial (como el cloruro, nitritos, cobre o mercurio).

La necesidad de tratar el agua del grifo, a pesar de que los organismos sanitarios la declaren potable, surge porque existen personas con condiciones de salud particulares para quienes el agua sin purificar puede presentar problemas. Además, aspectos como el sabor y la turbidez son factores que influyen en la percepción de calidad. Los filtros de agua domésticos actúan sobre estos parámetros, permitiendo corregir las características que merman la calidad del agua antes de su consumo, convirtiéndola en una alternativa más saludable para algunos usuarios.
El Mito del Lago Baikal y la Realidad de los Lagos Subglaciales:
Existe un mito popular que atribuye al agua del Lago Baikal, en Rusia, una pureza tan extrema que podría disolver un vaso de cristal. Si bien esta afirmación es una exageración, se basa en la excepcional pureza del agua de este lago, que le permite interactuar de manera única con otras partículas.
Sin embargo, en la naturaleza, el agua pura es un concepto elusivo. Incluso en entornos remotos, el agua interactúa con su entorno. Un ejemplo fascinante de agua en condiciones extremas se encuentra en el Lago Vostok, el mayor de los más de 400 lagos subglaciales conocidos en la Antártida. Este lago ha registrado temperaturas de hasta -89 °C, una de las más bajas jamás medidas en la Tierra. La superficie de este lago se estima en 14.000 kilómetros cuadrados.
En la Antártida, el agua glacial sometida a temperaturas y presiones criogénicas extremas puede experimentar sublimación, pasando directamente del estado sólido al gaseoso. El calor atrapado durante su proceso de congelación-expansión genera vapor, que puede socavar y formar cavernas en el interior de los glaciares, un fenómeno conocido como deshielo parcial.

El Agua como Fundamento de la Vida y la Tierra
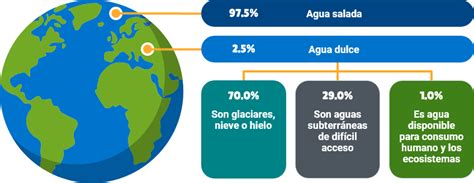
La presencia del agua en sus tres estados -sólido, líquido y gaseoso- es vital para comprender el origen y la evolución de la vida en la Tierra. Su existencia en estado líquido, en particular, es un requisito fundamental para la vida tal como la conocemos. El agua ocupa aproximadamente el 70% de la superficie terrestre y constituye una proporción significativa del cuerpo de los seres vivos.
La masa de la Tierra juega un papel crucial en la retención de una atmósfera que, junto con el vapor de agua y el dióxido de carbono, genera el efecto invernadero. Este efecto mantiene la temperatura superficial relativamente constante, permitiendo la existencia de agua líquida. Si la Tierra tuviera menos masa, una atmósfera más delgada resultaría en temperaturas extremas. De manera similar, la distancia al Sol y la cantidad de radiación solar recibida, en combinación con el efecto invernadero, aseguran que la superficie terrestre no sea ni demasiado fría ni demasiado caliente para el agua líquida. Si la Tierra estuviera más alejada del Sol, el agua se congelaría; si estuviera más cerca, las altas temperaturas limitarían la formación de capas polares o forzarían al agua a existir solo como vapor.
La salinidad del mar, por ejemplo, es el resultado de la disolución de sales provenientes de la atmósfera, ríos, glaciares, aguas hidrotermales y erupciones volcánicas submarinas. El valor medio de salinidad del agua marina es de 35 por mil. La temperatura de las aguas superficiales varía significativamente según la latitud, desde -2 °C en las zonas polares hasta 30 °C en las ecuatoriales. La temperatura también cambia con la profundidad, experimentando un descenso pronunciado entre los 100 y 1.500 metros (la termoclina), con pocas variaciones por debajo de esa cota.
En resumen, el agua es mucho más que una simple sustancia química. Es una fuerza dinámica con propiedades extraordinarias que moldean nuestro planeta, sustentan la vida y presentan desafíos constantes en cuanto a su pureza y gestión. Desde la intrincada danza de sus moléculas y puentes de hidrógeno hasta su papel fundamental en los ciclos geológicos y climáticos, el agua continúa siendo un misterio fascinante y un recurso insustituible.