El agua, esa sustancia omnipresente y fundamental para la vida, adquiere una relevancia insoslayable en el ámbito de los laboratorios. Lejos de ser un simple reactivo, su pureza y calidad son pilares sobre los que se asientan la exactitud y fiabilidad de innumerables análisis y experimentos científicos. Desde la preparación de soluciones hasta las técnicas analíticas más sensibles, la elección del grado de agua adecuado es un factor crítico que impacta directamente en la validez de los resultados. Este artículo explora en profundidad la naturaleza del agua pura en el contexto de laboratorio, los métodos para su análisis y purificación, las normativas que rigen su calidad y su indispensable papel en diversas aplicaciones científicas.
La Naturaleza del Agua: Más Allá de H₂O
El agua, con su fórmula química H₂O, es una sustancia inorgánica y polar. A temperatura ambiente, se presenta como un líquido transparente, insípido e inodoro. Cada molécula de agua consta de un átomo de oxígeno unido a dos átomos de hidrógeno mediante enlaces covalentes. La alta electronegatividad del oxígeno atrae los electrones compartidos con mayor fuerza, generando una distribución asimétrica de la carga electrónica. Esta polaridad confiere al agua un momento dipolar eléctrico significativo, permitiendo interacciones electrostáticas con otras moléculas polares o iones cargados.
Una de las propiedades más notables del agua es su excepcional capacidad como disolvente. Esta cualidad se debe a su polaridad y a su habilidad para formar enlaces de hidrógeno, tanto entre sus propias moléculas como con otras sustancias. Los enlaces de hidrógeno son interacciones dipolo-dipolo fuertes, donde el hidrógeno unido a un átomo electronegativo (como el oxígeno) se siente atraído por el extremo negativo de otra molécula polar o por un par de electrones solitario. Las sustancias que interactúan favorablemente con el agua se clasifican como hidrófilas, típicamente polares y capaces de formar enlaces de hidrógeno (ej. glucosa). Por el contrario, las sustancias hidrofóbicas, no polares (ej. grasas, aceites), no se disuelven bien en agua.
El agua existe naturalmente en los tres estados de la materia: sólido (hielo), líquido (agua) y gaseoso (vapor de agua). Su punto de fusión se aproxima a 0 °C (273.15 K) a 1 atmósfera de presión, mientras que su punto de ebullición es de 100 °C (373.15 K) bajo las mismas condiciones. Sin embargo, estos puntos pueden variar ligeramente con la presión y la presencia de impurezas. La densidad máxima del agua se alcanza a 3.98 °C.
La ionización del agua es un fenómeno clave. El agua puede actuar como ácido (donando un protón, H⁺) y como base (aceptando un protón), generando iones hidronio (H₃O⁺) e hidroxilo (OH⁻). En agua pura a 25 °C, la concentración de ambos iones es de 1.0 × 10⁻⁷ mol/L, lo que resulta en una solución neutra con un pH de 7. La constante de disociación del agua, Kw = [H⁺][OH⁻] = 1.0 × 10⁻¹⁴, es sensible a la temperatura y la presión.
La Importancia Crítica del Agua en el Laboratorio
En el entorno de laboratorio, el agua es el reactivo más utilizado, presente en la mayoría de los procesos y soluciones. Su pureza es un factor determinante para la fiabilidad y exactitud de los resultados analíticos. Las impurezas, ya sean iónicas, orgánicas o coloidales, pueden interferir en reacciones, alterar mediciones y, en última instancia, invalidar experimentos. Por ello, transformar el agua común en un reactivo de alta calidad para laboratorio requiere tecnologías de purificación avanzadas y un control riguroso de los parámetros de calidad.

La elección del grado de agua apropiado depende de la aplicación específica. Desde el lavado de material hasta técnicas de alta sensibilidad como la espectrometría de masas (MS) o la cromatografía líquida de ultra alto rendimiento (UHPLC), cada proceso demanda un nivel de pureza particular. La cromatografía, por ejemplo, un método fundamental para la separación y análisis de mezclas, se apoya en agua de alta pureza para la elución de columnas y la preparación de fases móviles, asegurando la correcta separación de compuestos en análisis ambientales, farmacéuticos y alimentarios.
Clasificación y Estándares de Calidad del Agua de Laboratorio
Diversos organismos normalizadores, como ISO (International Organization for Standardization) y ASTM (American Society for Testing and Materials), establecen especificaciones para el agua utilizada en laboratorios analíticos. La norma ISO 3696, por ejemplo, clasifica el agua para uso en análisis de laboratorio en tres tipos, cada uno con requisitos específicos de pureza:
Agua Tipo I (Agua Ultrapura): Prácticamente libre de impurezas iónicas, coloidales y orgánicas. Su resistividad es superior a 18.2 MΩ·cm y el carbono orgánico total (COT) es ≤ 10 ppb. Es esencial para aplicaciones que exigen la máxima pureza, como electroforesis, cromatografía de alta resolución (HPLC), espectrometría de masas (MS) y biología molecular (PCR, secuenciación de ADN).
Agua Tipo II (Agua Desionizada o de Ósmosis Inversa): Puede contener trazas de impurezas inorgánicas, orgánicas y coloidales. Su resistividad es ≥ 1 MΩ·cm y el COT es ≤ 50 ppb. Es adecuada para análisis químicos y bioquímicos generales, preparación de tampones y medios de cultivo, y diluciones de muestras.
Agua Tipo III (Agua Destilada): Adecuada para pruebas de laboratorio generales y análisis químicos de rutina. Su resistividad es ≥ 0.05 MΩ·cm y el COT es ≤ 200 ppb. Se utiliza principalmente para el lavado de cristalería, humidificadores y otros equipos, así como para el pretratamiento en la obtención de agua Tipo I y II.
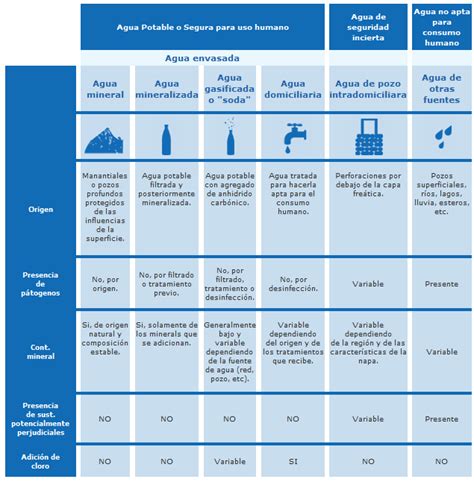
Además de estas clasificaciones, el agua de laboratorio puede distinguirse por su método de producción:
Agua Destilada: Elimina la mayoría de los contaminantes, pero no las impurezas volátiles. Su conductividad suele ser de 0.1-0.5 µS/cm.
Agua de Ósmosis Inversa (OI): Elimina eficazmente sales disueltas, virus, bacterias y la mayoría de las sustancias orgánicas. La conductividad puede reducirse a 0.05-0.5 µS/cm.
Agua Desionizada: Purificada adicionalmente a partir de agua de ósmosis inversa para eliminar minerales disueltos, resultando en una conductividad entre 0.05 y 0.2 µS/cm.
Agua Ultrapura: Contiene únicamente moléculas de agua, con una conductividad de 0.055 µS/cm o inferior. Es altamente reactiva y susceptible a la contaminación, requiriendo uso inmediato.
Es fundamental recordar que todos los tipos de agua de laboratorio son susceptibles a la contaminación por bacterias y gases (como el dióxido de carbono), lo que puede generar contaminación secundaria. Por ello, el almacenamiento adecuado y la minimización de la exposición al aire son cruciales.
Técnicas de Purificación de Agua para Laboratorio
La obtención de agua de alta pureza en laboratorio se logra mediante diversas técnicas, a menudo combinadas para maximizar la eficacia:
Destilación
La destilación es un proceso histórico que consiste en calentar el agua hasta su punto de ebullición, vaporizarla y luego condensar el vapor para obtener líquido purificado. Aunque efectiva para eliminar muchas impurezas, no retiene compuestos volátiles.
Ósmosis Inversa (OI)
Este método emplea membranas semipermeables que, bajo presión, permiten el paso del agua mientras retienen hasta el 99% de sales disueltas, virus, bacterias y otras moléculas. La ósmosis inversa es energéticamente eficiente y no requiere reacciones químicas, pero necesita agua de alimentación de buena calidad y un pretratamiento para eliminar partículas.
¿QUE ES LA OSMOSIS INVERSA? CÓMO FUNCIONA LA OSMOSIS INVERSA? SISTEMA DE FILTRACIÓN DE AGUA RO/OI
Desionización
La desionización utiliza sistemas de intercambio iónico con resinas especializadas que sustituyen los iones disueltos en el agua por otros iones (generalmente H⁺ y OH⁻). Es muy eficaz para eliminar contaminantes iónicos, pero las resinas requieren regeneración periódica y el agua de entrada no debe contener altos niveles de oxidantes.
Electrodesionización (EDI)
La electrodesionización combina resinas de intercambio iónico, membranas selectivas y electrodiálisis. Un campo eléctrico impulsa la migración de iones, eliminándolos del agua de forma continua. Los sistemas EDI producen agua de altísima pureza sin necesidad de productos químicos para la regeneración de resinas, pero requieren estrictos requisitos de calidad del agua de entrada, a menudo precedida por ósmosis inversa.
La combinación estratégica de estas técnicas, como la integración de filtración, ósmosis inversa y desionización, permite alcanzar niveles superiores de pureza, asegurando la remoción efectiva de partículas, iones y microorganismos.
Control de Calidad y Verificación de Parámetros
La verificación de la calidad del agua en laboratorio es un proceso continuo que involucra el análisis de diversos parámetros. La conductividad eléctrica es un indicador clave de la presencia de iones disueltos. Un conductivímetro mide la capacidad del agua para conducir electricidad, que es inversamente proporcional a su pureza. El agua ultrapura presenta una conductividad extremadamente baja (idealmente cercana a 0.055 µS/cm).
Otros parámetros importantes incluyen:
- Carbono Orgánico Total (COT): Mide la cantidad de carbono orgánico presente, que puede provenir de fuentes biológicas o químicas y afectar reacciones sensibles.
- Microorganismos: La presencia de bacterias y otros microorganismos puede contaminar experimentos biológicos y afectar resultados analíticos.
- Partículas: Las partículas en suspensión pueden interferir en técnicas ópticas o cromatográficas.
- pH: Indica la acidez o alcalinidad del agua, fundamental en muchas aplicaciones.
- Residuo Fijo y Residuos de Calcinación: Miden la cantidad de sólidos inorgánicos que quedan tras la evaporación y calcinación del agua.
- Resistencia al KMnO₄: Evalúa la presencia de materia orgánica oxidable.
- Metales Pesados y Otros Elementos: La espectrometría de masas con plasma acoplado inductivamente (ICP-MS) y la espectrometría de emisión óptica con plasma acoplado inductivamente (ICP-OES) son técnicas avanzadas para detectar y cuantificar trazas de metales y otros elementos.
La estandarización, a través de normativas como la ISO 3696, y el uso de equipos analíticos de alta precisión son esenciales para garantizar que el agua utilizada en el laboratorio cumple con las especificaciones requeridas para cada aplicación. La elección del equipo analítico y la calidad de los análisis deben ser igualmente rigurosas.
Proveedores y Soluciones de Agua Pura
Empresas como Tecnal se dedican a la fabricación y comercialización de equipos científicos, ofreciendo soluciones para la purificación y análisis de agua. Su misión es contribuir al desarrollo científico y tecnológico mediante equipos de alta calidad y servicios especializados. La oferta de agua ultrapura, como la propuesta por Agualab, enfocada en laboratorios que demandan la máxima pureza, libre de flúor y metales pesados, y con análisis exhaustivos por laboratorios externos acreditados, subraya la importancia de contar con proveedores confiables y productos certificados para asegurar la integridad de los procesos de laboratorio.
En conclusión, el agua pura es un componente indispensable en cualquier laboratorio moderno. Su calidad, rigurosamente controlada y analizada, es la base para la obtención de resultados precisos y fiables en una vasta gama de aplicaciones científicas. La comprensión de sus propiedades, los métodos de purificación y las normativas vigentes es fundamental para cualquier profesional del ámbito científico.
tags: #agua #pura #laboratorio