Las terapias depurativas renales, en el contexto de situaciones agudas, constituyen una herramienta fundamental en las unidades de cuidados intensivos (UCI). Estas terapias se basan en principios clave para sustituir la función renal: la convección, la difusión y la adsorción. De estos, la adsorción ha emergido como un principio particularmente efectivo para la depuración de sustancias tóxicas en la sangre, logrando este fin mediante el uso de membranas especializadas y sorbentes incorporados en circuitos extracorpóreos. El control de mediadores proinflamatorios, como los que desencadenan la "tormenta de citoquinas" en pacientes sépticos, y la eliminación de toxinas urémicas unidas a proteínas son áreas de intensa investigación para estas técnicas depurativas adsortivas. La capacidad inherente de estas terapias para eliminar endotoxinas y citoquinas, tanto en pacientes con lesión renal aguda (LRA) como en aquellos sin ella, las posiciona como medidas complementarias de gran valor en el soporte vital de pacientes en estado crítico. Actualmente, el arsenal terapéutico adsortivo incluye sistemas como MARS, Cytosorb®, CPFA, OXIRIS® y Seraph®.
La Complejidad de la Lesión Renal Aguda y la Inflamación Sistémica
La incidencia de la lesión renal aguda (LRA) es un fenómeno de gran variabilidad, presentando una prevalencia del 7-18% en pacientes hospitalizados y alcanzando hasta el 50% en aquellos admitidos en unidades de cuidados intensivos. Diversas comorbilidades, como la edad avanzada, la hipertensión arterial y la diabetes, incrementan significativamente este riesgo. Factores adicionales que predisponen al desarrollo de LRA incluyen la sepsis, las intoxicaciones y la respuesta inflamatoria desproporcionada conocida como tormenta de citoquinas. La detección tardía y la demora en la implementación de medidas terapéuticas adecuadas pueden derivar en un aumento de la mortalidad, secuelas a largo plazo y una prolongación de la estancia hospitalaria.
En el paciente crítico, la acumulación de sustancias nocivas en el torrente sanguíneo representa un factor de deterioro. Entre estas sustancias se encuentran las toxinas urémicas unidas a proteínas y la respuesta proinflamatoria exacerbada, la mencionada tormenta de citoquinas. Ambas entidades actúan como agresores directos sobre tejidos y órganos, conduciendo a un empeoramiento del estado clínico del paciente.
Estrategias Terapéuticas para la Depuración Sanguínea
Una estrategia que se ha explorado para mitigar el daño causado por estos agresores es la administración de flujos altos en terapias depurativas, superando los valores convencionales de 20-35 mL/kg/h en pacientes sépticos. Esta técnica, conocida como hemofiltración de alto volumen (HFHV), busca la eliminación de mediadores inflamatorios de tamaño pequeño y mediano (5-60 kDa) mediante el aumento de la convección y la potenciación de las propiedades adsortivas de las membranas. La HFHV puede administrarse de forma continua o intermitente, en "pulsos", con flujos que varían entre 50-70 mL/kg/h durante 24 horas o 100-120 mL/kg/h en periodos cortos de cuatro a ocho horas. Sin embargo, estudios como el IVOIRE de Joannes-Boyau et al. no lograron demostrar diferencias significativas en la mortalidad a 28 días al incrementar los flujos hasta 70 mL/kg/h. Actualmente, la evidencia de su beneficio es limitada y existe el riesgo de inducir un "dialitrauma" asociado a la eliminación de sustancias de pequeño tamaño, como los iones.
Ante estas limitaciones, se han desarrollado las técnicas adsortivas como un método alternativo para eliminar o modular la respuesta inflamatoria. La adsorción es un fenómeno físico-químico en el cual un sólido o líquido atrae y retiene en su superficie gases, vapores, líquidos o sustancias disueltas. Este principio se aplica en circuitos extracorpóreos para fijar en la superficie de las membranas sustancias que, por su tamaño, no pueden ser eliminadas por métodos convencionales de filtración, como las toxinas urémicas ligadas a proteínas o las citoquinas. Otra aproximación consiste en la adición de filtros con capacidad adsortiva a sistemas extracorpóreos, que pueden eliminar sustancias unidas a proteínas mediante el uso de sistemas con alta afinidad por la albúmina. Para las sustancias liberadas en el plasma, se han diseñado técnicas que emplean plasmafiltros específicos previos a cartuchos adsortivos, capaces de lograr la detoxificación por adsorción. Diversos sorbentes, como las resinas, han demostrado eficacia en la eliminación de sustancias, por ejemplo, de tóxicos biliares en casos de insuficiencia hepática.
La afinidad intrínseca de las membranas en los circuitos extracorpóreos por determinadas sustancias es un factor de especial interés en las terapias adsortivas. Idealmente, las membranas deben poseer alta biocompatibilidad, durabilidad, una gran superficie de contacto, alta permeabilidad a solutos y líquidos, y un costo reducido. Los polímeros se han consolidado como materiales idóneos para alcanzar estos objetivos, siendo el polimetacrilato de metilo, el poliacrilonitrilo y la polietilamina los más utilizados. Para las técnicas adsortivas, son cruciales la afinidad de la membrana por las sustancias a eliminar, su carga eléctrica y el tamaño de poro adecuado para la adsorción. La investigación continúa en la búsqueda de materiales que potencien las capacidades adsortivas de las membranas, incorporando elementos que atraigan selectivamente distintas moléculas. Un ejemplo de ello es la polimixina B, añadida a algunas membranas, que ha demostrado reducir la mortalidad a 28 días en pacientes sépticos al actuar como un péptido que destruye la membrana de bacterias gramnegativas. La adsorción de sustancias mediante circuitos extracorpóreos representa, por tanto, un área activa de investigación.
Indicaciones de las Terapias Adsortivas
Las indicaciones de las terapias adsortivas se dividen en dos categorías principales: aquellas de causa no renal y las de causa renal.
Indicaciones No Renales: Modulación de la Respuesta Inflamatoria
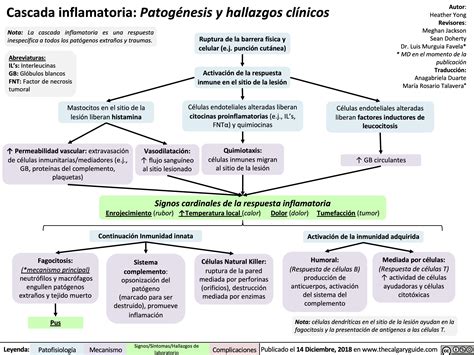
En el ámbito no renal, el objetivo primordial de las terapias adsortivas es la eliminación de la mayor cantidad posible de mediadores que puedan inducir respuestas inflamatorias desadaptativas, modulando así la tormenta inflamatoria. Esta cascada inflamatoria, amplificada por el propio sistema inmune, genera reacciones adversas que dañan diversos órganos. Las principales responsables de esta situación son las altas concentraciones de citoquinas en el torrente sanguíneo. Entre las citoquinas más estudiadas por su influencia en estas respuestas desadaptativas se encuentran las linfoquinas, monokinas, quimiocinas, interleucinas (IL) y el factor de necrosis tumoral α (TNF-α).
Durante la pandemia de COVID-19, la necesidad de controlar las citoquinas cobró una relevancia particular, evidenciada por estudios que demostraron respuestas proinflamatorias desproporcionadas en pacientes críticos con esta enfermedad. Las terapias adsortivas demostraron ser técnicas depurativas eficaces para la retirada de estos mediadores proinflamatorios de la sangre. Ante la incertidumbre inicial sobre el manejo de esta nueva enfermedad, se adaptaron recomendaciones de expertos. Ronco et al. sugirieron la utilización de membranas con capacidades adsortivas para controlar y eliminar la respuesta inflamatoria desproporcionada. Estudios previos ya habían constatado beneficios asociados a las terapias adsortivas y la retirada de citoquinas, como la disminución de la dosis de catecolaminas, la reducción de los niveles de procalcitonina y ácido láctico, el descenso en los valores de la escala Sequential Organ Failure Assessment Score (SOFA), el aumento de la presión arterial media y la disminución de los niveles plasmáticos de interleucinas como IL-1, IL-4, IL-6 e IL-10.
Indicaciones Renales: Eliminación de Toxinas Urémicas
En el contexto renal, las terapias adsortivas, al igual que la convección y la difusión, se centran en la eliminación de productos de desecho metabólico. La adsorción, en esta indicación, se emplea también para eliminar toxinas urémicas unidas a proteínas, que son particularmente difíciles de depurar mediante convección y difusión. Además, se han utilizado membranas con alta capacidad adsortiva para aliviar la sintomatología asociada a los síndromes urémicos.
Por lo tanto, es imperativo que el personal de cuidados críticos comprenda los principios fisicoquímicos y las indicaciones de las técnicas adsortivas empleadas en las unidades de cuidados intensivos.
Técnicas Adsortivas Específicas
Filtración y Adsorción de Plasma Acoplado (CPFA)
La terapia de Filtración y Adsorción de Plasma Acoplado (CPFA, por sus siglas en inglés Coupled Plasma Filtration-Adsorption) combina la filtración de plasma con la adsorción, simultáneamente con la hemofiltración. CPFA fue concebida como un método no selectivo para eliminar mediadores inflamatorios, integrando en un circuito extracorpóreo un plasmafiltro y un cartucho de resina como adsorbente. El sistema consta de una línea principal y una vía accesoria adsortiva por donde circula únicamente el plasma para su detoxificación. CPFA ofrece la versatilidad de asociarse a otras técnicas depurativas, permitiendo el control del volumen y la eliminación de pequeñas moléculas a través del ultrafiltrado. Se ha reportado su uso en casos de rabdomiólisis, en pacientes quemados con sepsis y LRA, y como soporte temporal hasta la recuperación de la función hepática, con o sin trasplante. La indicación más extendida de esta técnica es durante procesos sépticos y en el síndrome de respuesta inflamatoria sistémica (SIRS).
En un estudio de Livigni et al., aunque los datos sobre el tratamiento de pacientes sépticos con CPFA no fueron concluyentes, se observó una reducción en la mortalidad en el subgrupo con un mayor volumen de plasma tratado (> 0.18 mL/kg/día), con un odds ratio (OR) de 0.36 (intervalo de confianza [IC] 95% [0.13-0.99], p = 0.033). Para prolongar la duración del circuito en CPFA, es necesaria la anticoagulación.
En el proceso de CPFA, la sangre del paciente primero pasa por un plasmafiltro que separa una porción del plasma. Este plasma separado se dirige al cartucho de resina adsorbente, donde las sustancias tóxicas son retenidas. Posteriormente, el plasma detoxificado se reincorpora a la sangre para continuar con un proceso de hemofiltración. Un parámetro crucial en esta técnica es el ritmo de la bomba de plasma, que debe situarse entre el 10-22% del flujo de la bomba de sangre del circuito principal.
Sistema de Recirculación de Adsorbente Molecular (MARS)
El sistema MARS (Molecular Adsorbent Recirculating System) se emplea para la diálisis de la albúmina, una proteína que transporta diversas sustancias tóxicas asociadas a la insuficiencia hepática. Además de depurar la albúmina, MARS permite la eliminación de otras moléculas no unidas a proteínas, como amoniaco, creatinina y urea, así como de sustancias ligadas a proteínas, incluyendo ácidos biliares, bilirrubina total e indirecta, ácidos grasos de cadena corta o media, y mediadores inflamatorios (IL-6, TNF-α). Esta técnica depurativa se ha utilizado principalmente como medida de soporte en la insuficiencia hepática aguda y crónica reagudizada.
Es fundamental prestar especial atención a los episodios de sangrado durante la técnica MARS, ya que se han observado alteraciones en los factores de coagulación. Las enfermeras de UCI deben vigilar este aspecto, minimizando la anticoagulación. La coagulación intravascular diseminada constituye una contraindicación absoluta para este tratamiento.
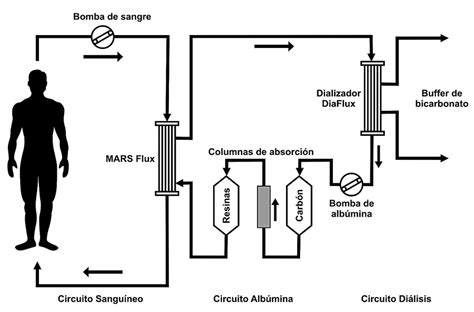
Las sustancias del metabolismo hepático se eliminan mediante una técnica de diálisis que utiliza albúmina. El procedimiento implica la adición a un sistema extracorpóreo de un sistema que contrapone albúmina (entre el 10-25%) a un ritmo variable entre 150-250 mL/min. La duración de esta terapia oscila entre cuatro y ocho horas. El sistema MARS se compone de tres compartimentos interconectados:
- Compartimento 1 (Sanguíneo): El circuito extracorpóreo conecta al paciente, mediante un catéter de doble luz, a un filtro dializador de alto flujo. A través de este filtro, la sangre entra en contacto con la albúmina, facilitando el intercambio de toxinas.
- Compartimento 2 (Dialítico): La albúmina, cargada con las toxinas, fluye hacia un dializador de bajo flujo. Aquí, las sustancias de pequeño tamaño molecular son eliminadas por difusión hacia un líquido de diálisis.
- Compartimento 3 (Adsortivo): Posteriormente, la albúmina circula a través de una columna de carbón activado y, seguidamente, por una columna de resina. En este punto, la albúmina se regenera y retorna al filtro para continuar el proceso de recaptación de toxinas.
Los compartimentos 2 y 3 forman un circuito cerrado de aproximadamente 500-600 mL de albúmina (con concentración variable), donde se ejecutan los procesos de depuración adsortiva y difusiva.
Los resultados de diversos estudios han validado MARS como una medida de soporte segura y factible. La coagulación de los filtros ha representado el principal inconveniente de este tipo de terapias. Gilg et al. emplearon anticoagulación regional con citrato durante la aplicación de MARS sin observar complicaciones significativas. Estos investigadores documentaron una menor mortalidad a 60 y 90 días de la esperada en pacientes con insuficiencia hepática post-hepatectomía al aplicar MARS.
Cytosorb®
Cytosorb® es una técnica adsortiva que recibe su nombre de la marca comercial de la membrana utilizada. Esta membrana, compuesta por perlas de poliestireno divinilbenceno, es reconocida por su biocompatibilidad y hemocompatibilidad.
Características de las Membranas y su Impacto en la Depuración:
La eficacia de las terapias adsortivas está intrínsecamente ligada a las propiedades de las membranas empleadas. Estas membranas se clasifican principalmente en:
Tipos de Membrana:
- Membranas celulósicas.
- Membranas sintéticas.
Espesor de la Membrana: El grosor de la membrana influye directamente en la resistencia al paso de solutos y líquidos.
Definiciones y Propiedades de las Membranas:
- Hidrofilia: Capacidad de atraer y retener agua. Las membranas hidrofílicas interactúan con el agua y pueden activarse con células y proteínas.
- Hidrofobia: Tendencia a repeler el agua. No interactúan con el agua.
- Polaridad: Se refiere a la presencia de carga eléctrica en la superficie de la membrana. Las membranas polares tienen carga eléctrica superficial.
- Membranas Simétricas y Asimétricas: Las membranas simétricas presentan una distribución uniforme de poros, mientras que las asimétricas tienen diferentes distribuciones de tamaño y densidad de poros en su estructura.
Biocompatibilidad: Es la capacidad de una membrana para minimizar las reacciones adversas al contacto con la sangre. Los fenómenos adversos incluyen:
- Activación del complemento (vía alterna).
- Leucopenia y neutropenia transitoria.
- Activación de moléculas de adhesión.
- Activación celular y liberación de citoquinas.
- Alteraciones en el sistema de coagulación y fibrinolisis.
- Reacciones específicas a ciertos tipos de membranas, como la AN69.
Permeabilidad:
- Permeabilidad al agua: Importante para la ultrafiltración.
- Permeabilidad a los solutos: Determina la capacidad de la membrana para eliminar toxinas.
Beneficios de la Alta Permeabilidad:
- Potencial mejora en dislipemia.
- Posible implicación en amiloidosis asociada a diálisis.
- Influencia en la anemia.
- Mayor conservación de la función renal residual.
- Modulación de la respuesta inflamatoria crónica.
- Impacto en la morbilidad y mortalidad.
Adsorción: La capacidad de la membrana para retener sustancias específicas en su superficie.
Otros Factores Relacionados con las Propiedades de las Membranas:
- Esterilización: El método de esterilización puede afectar las propiedades de la membrana.
- Temperatura del líquido de diálisis: Influye en la cinética de difusión y adsorción.
- Reuso: La reutilización de dializadores puede comprometer su eficacia y seguridad.
- Contaminación del líquido de diálisis: Puede introducir sustancias indeseadas en el circuito.
Nuevos Dializadores:
- Membranas de medio y alto cut-off: Diseñadas para eliminar moléculas de mayor peso molecular.
El dializador es un componente esencial de los sistemas de depuración extracorpórea, actuando como el compartimento donde se eliminan las toxinas urémicas y se restaura la homeostasis. Los dializadores se clasifican según su diseño geométrico (placa o fibra hueca/capilar), la composición de la membrana y su capacidad de eliminación de solutos. Actualmente, la tecnología de fibra hueca o capilar es la predominante. La membrana es el corazón del dializador, y su clasificación se basa en su composición química y capacidad depuradora. Las membranas, generalmente polímeros, se dividen en celulósicas, modificadas y sintéticas, aunque la tendencia actual es definirlas por sus propiedades: biocompatibilidad, permeabilidad, eficacia depuradora, distribución de poros (simétrica o asimétrica), polaridad, e interacciones hidrofílicas/hidrofóbicas.
Las membranas celulósicas, compuestas por cadenas de polisacáridos con grupos hidroxilo libres, exhiben hidrofilia y biocompatibilidad variable. La sustitución de estos grupos mejora la biocompatibilidad. El triacetato de celulosa, con casi todos los grupos hidroxilo sustituidos, es una membrana de alta permeabilidad con una estructura multicapa que influye en el transporte difusivo y convectivo.
Las membranas sintéticas, como la polisulfona, polimetilmetacrilato y poliacrilonitrilo, pueden ser de alta o baja permeabilidad y son fundamentales para el transporte difusivo. La difusión, mecanismo principal en hemodiálisis, se ve afectada por el gradiente de concentración, el coeficiente de difusión del soluto (dependiente del peso molecular y radio), la temperatura, la superficie de la membrana y su espesor.
La electronegatividad superficial de las membranas, medida por el potencial Z, influye en la interacción con las partículas cargadas en la sangre y, por ende, en la biocompatibilidad. Las membranas con una fuerte carga negativa, como la AN69, pueden aumentar la generación de bradiquinina, asociándose a reacciones anafilactoides en pacientes que toman inhibidores de la enzima convertidora de angiotensina (IECA).
La interacción de la sangre con los componentes del circuito extracorpóreo induce una respuesta inflamatoria. La activación del complemento, particularmente la vía alterna, se relaciona con la estructura de las membranas celulósicas. Esto conduce a la liberación de anafilatoxinas (C3a, C5a) y otros mediadores que activan leucocitos y monocitos, promoviendo la liberación de citoquinas proinflamatorias. La leucopenia transitoria, especialmente neutropenia, es común al inicio de la diálisis y está relacionada con la activación del complemento y el tipo de membrana.
La activación celular durante la diálisis, incluyendo leucocitos, monocitos, células NK y linfocitos T, puede inducir la liberación de citoquinas proinflamatorias. Asimismo, se activa la vía intrínseca de la coagulación, generando bradiquinina, un péptido vasoactivo. Las membranas celulósicas tienden a incrementar la actividad fibrinolítica.
La biocompatibilidad de los dializadores se evalúa considerando múltiples factores, incluyendo la composición de la membrana, el método de esterilización y las condiciones de uso. Las membranas AN69 sulfonadas han mostrado menores concentraciones de anafilatoxinas C3a y C5a en comparación con las celulósicas, posiblemente debido a su capacidad de adsorber productos de complemento activado.
Las membranas de poliarilsulfona (PSu/PESu) se han asociado con reacciones agudas, incluyendo disnea, hipotensión y broncoespasmo, especialmente en pacientes que toman IECA. Estas reacciones pueden deberse a la generación de bradiquinina y a la presencia de polivinilpirrolidona (PVP), un alérgeno potencial. En contraste, las membranas de triacetato de celulosa, al no generar estas reacciones, muestran una alta capacidad de adsorción de albúmina y apolipoproteínas, lo que podría contribuir a su mayor biocompatibilidad.
La permeabilidad de las membranas, cuantificada por el coeficiente de ultrafiltración (KUf), define su capacidad para eliminar líquidos. Las membranas de alta permeabilidad ("super-flux") están diseñadas para eliminar moléculas de alto peso molecular, aunque con el riesgo de eliminar solutos deseados como la albúmina. La eficacia depuradora (KoA) es otro parámetro clave, modulado por la porosidad y el espesor de la membrana, y es dependiente del tamaño del soluto, y de los flujos de sangre y líquido de diálisis.
Eliminación de Sustancias Perfluoroalquiladas (PFAS)
Las sustancias PFAS representan un grupo de más de 4700 compuestos químicos utilizados en diversas aplicaciones, como ropa impermeable y utensilios de cocina antiadherentes. Su potencial perjudicial para la salud y el medio ambiente ha impulsado la investigación de métodos de eliminación eficientes. Un equipo de investigación ha desarrollado un material adsorbente innovador, basado en nanocristales de celulosa en forma de polvo, que ha demostrado una alta capacidad para capturar PFAS en fluidos.
Los sistemas actuales para la eliminación de PFAS, como el carbón activado y los sistemas de intercambio iónico, presentan limitaciones en cuanto a su eficiencia ante la amplia variedad de PFAS existentes. El enfoque holístico del nuevo material, desarrollado a partir de nanocristales, ha sido clave para observar su potencial. El estudio ha logrado desarrollar un mecanismo de adsorción capaz de atrapar hasta el 99% de las partículas de PFAS.
La contaminación por PFAS puede ocurrir a través de vías fluviales, ya que estas sustancias se liberan al medio ambiente a través de diversos productos. A pesar de que no se fabrican en Canadá, su presencia es ubicua en numerosos productos de consumo. La exposición humana a las PFAS puede darse a través de productos de consumo e incluso de alimentos.
El equipo investigador ha tenido en consideración la necesidad de soluciones de tratamiento de agua para áreas aisladas. El desarrollo de nuevas técnicas, como la propuesta por el Dr. Mohseni y su equipo, abre la puerta al tratamiento de PFAS en aguas residuales, ofreciendo no solo un nuevo mecanismo para su eliminación sino también una alternativa para zonas remotas.

Plasmaféresis y Hemofiltración Combinada
El abordaje terapéutico más común para eliminar mediadores de peso molecular medio-alto implica el uso de terapias convectivas con membranas de porosidad adecuada. Un enfoque específico combina la separación del plasma de la sangre mediante un plasmafiltro, su posterior procesamiento en un cartucho con resina sintética para adsorber mediadores humorales, y la reinfusión del plasma depurado para su paso por un hemofiltro. Este sistema consta de un plasmafiltro (0.45 m²) en serie con un hemofiltro de polifenileno de alta permeabilidad (Kuf 41 mL/h/mmHg, superficie 1.4 m²). El flujo plasmático se sitúa entre 30 y 40 ml/min, y el plasma es dirigido al cartucho de adsorción Mediasorb®, que contiene 70 gramos de una resina de polímero estirénico.
La capacidad adsortiva de la resina en la CPFA es temporalmente limitada, pero la hemofiltración puede continuar incluso después de su agotamiento, sin necesidad de reemplazar el circuito extracorpóreo. En resumen, la CPFA es una terapia de depuración extracorpórea que integra la separación de plasma y la adsorción de citoquinas, mediadores inflamatorios y/o toxinas, seguida de hemofiltración para el control de la sobrecarga de volumen y la eliminación de mediadores hidrosolubles de tamaño pequeño y mediano.
Hemoperfusión y la Eliminación de Mediadores
La mayoría de las citoquinas y mediadores presentes en la sepsis son demasiado grandes para ser eliminados eficazmente mediante convección o difusión. Además del peso molecular, la dimensión molecular (el tamaño de la molécula en solución, expresada como radio de Stokes-Einstein) es un factor relevante. La hemoperfusión permite la unión y eliminación selectiva de mediadores o toxinas específicas. Su principal ventaja radica en la gran superficie de la matriz adsorbente, que puede alcanzar hasta 1000 m²/g.
Se emplean flujos entre 150 y 200 mL/min, lo que permite tratar un mayor volumen de sangre. Sin embargo, esto se asocia a una adsorción más limitada, ya que el flujo rápido puede arrastrar moléculas que de otro modo serían adsorbidas. Los beneficios teóricos de la CPFA se han evaluado en estudios experimentales, demostrando mejoras en diversos mediadores y variables biológicas en modelos de sepsis.
En un estudio de shock endotóxico en conejos, la adición de un cartucho adsorbente mejoró la supervivencia a las 72 horas en comparación con la hemofiltración aislada, independientemente de la carga de lipopolisacárido (LPS) administrada, ya que este cartucho no adsorbe LPS. Esto sugiere que el beneficio observado podría atribuirse a una mayor tasa de adsorción de citoquinas.
Estudios posteriores en modelos porcinos de shock séptico no lograron demostrar diferencias significativas en alteraciones de la microcirculación, marcadores de metabolismo celular energético, lesión endotelial ni inflamación sistémica. Estas discrepancias podrían deberse a diferencias metodológicas, como la duración de la terapia, el momento de su aplicación (antes de la inducción de sepsis o en shock establecido) y la ausencia de terapia antimicrobiana en uno de los modelos.
Los estudios observacionales en shock séptico han sugerido que el uso de CPFA se asocia con mejoría en variables clínicas como la presión arterial media (PAM) y el uso de vasopresores, así como mejoría del índice cardíaco y la PaO2/FiO2. Sin embargo, estos beneficios tienden a revertir entre sesiones, lo que subraya la necesidad de confirmar estos hallazgos con ensayos clínicos rigurosos.
Ensayos clínicos aleatorizados, como el COMPACT y el COMPACT-2, diseñados para evaluar la mortalidad en pacientes con shock séptico tratados con CPFA frente al tratamiento estándar, fueron detenidos prematuramente por futilidad o por observar un incremento de la mortalidad precoz en el grupo de intervención. Problemas técnicos, como la coagulación del circuito, fueron factores contribuyentes. El ensayo español ROMPA, también detenido prematuramente por causas externas, no encontró diferencias significativas en mortalidad.
La evidencia actual no ha logrado demostrar de manera concluyente que la aplicación de CPFA, bajo las condiciones de los protocolos estudiados, sea capaz de reducir la mortalidad en un 20%. Se postula que la mayor efectividad de la CPFA se logra cuando la dosis de plasma a tratar es elevada, meta que puede ser difícil de alcanzar debido a factores como la coagulación del circuito extracorpóreo, la disfunción del acceso vascular y las alteraciones hemodinámicas.
Para asegurar la efectividad de la CPFA, se considera fundamental la anticoagulación para garantizar la duración del circuito extracorpóreo. La anticoagulación sistémica con heparina se reserva para pacientes con indicaciones específicas, como aquellos en ECMO, requiriendo monitorización estrecha. La anticoagulación regional con citrato, ajustada automáticamente por la máquina, se presenta como una alternativa.
Existen dudas razonables sobre las indicaciones específicas de CPFA y cómo mejorar sus resultados, principalmente por la falta de precisión sobre el momento óptimo de inicio de la terapia y la ausencia de un biomarcador confiable que prediga el beneficio adicional sobre otras terapias depurativas. La hemofiltración de alto volumen en sepsis, si bien ha demostrado efectos sobre el componente hemodinámico, no ha logrado sustancialmente resultados positivos en mortalidad en metaanálisis.
La aplicación de CPFA en pacientes con shock séptico y disfunción renal y hepática severa es relevante, ya que permite la remoción de bilirrubina y ácidos grasos tóxicos, que pueden generar nefrotoxicidad. Incluso, tras la reanimación inicial, la CPFA podría disminuir el riesgo de lesión renal aguda (LRA).
Principios Físicos de las Terapias Extracorpóreas en UCI - Dr. Omar Julian Plazas
Consideraciones sobre la Depuración Extracorpórea en Pediatría
La mayoría de las máquinas de depuración extrarrenal continua (TDR) están diseñadas para adultos, aunque pueden adaptarse para uso pediátrico. Sin embargo, no están oficialmente aprobadas para neonatos y lactantes pequeños. Para su uso en niños, deben permitir la programación de bajos volúmenes de flujo de sangre y reposición, así como disponer de mediciones fiables con volúmenes bajos.
La instauración de la TDR implica la elección del filtro apropiado, la monitorización de presiones (presión de "caída" del filtro y presión transmembrana) y la vigilancia activa del personal. La fracción de filtración, que representa la cantidad de suero ultrafiltrado del total de plasma que pasa por el filtro, es otro parámetro a considerar. El principal inconveniente de la TDR es la trombosis del filtro y/o circuito, lo que hace que el tratamiento anticoagulante sea crucial.
El Rol de los Sorbentes y Materiales Filtrantes
Los medios filtrantes, ya sean granulados o en polvo, son esenciales para retener material particulado en el tratamiento de aguas. El carbón activado, un ejemplo de medio filtrante, es un sólido utilizado para eliminar sustancias solubles del agua. Estos sistemas son ideales para tratamientos terciarios y la reutilización de aguas, siendo fáciles de implantar y mantener, incluso en sistemas convencionales de depuración. La calidad excepcional y el precio competitivo de estos medios filtrantes, como el carbón activado proveniente de la cáscara de coco, son factores importantes a considerar.
La adsorción es un proceso fundamental en la depuración, donde un sólido (el adsorbente) retiene una sustancia soluble del fluido. El carbón activo es ampliamente empleado en este tipo de aplicaciones.
Principios de la Depuración Renal y Técnicas Asociadas
La terapia de depuración renal (TDR) se refiere a la purificación extracorpórea de la sangre del paciente, reemplazando temporalmente la función renal mediante una máquina que hace pasar la sangre a través de un filtro. Los principios fundamentales de la TDR incluyen:
Convección o Ultrafiltración: Movimiento de disolvente y solutos disueltos a través de una membrana semipermeable en respuesta a un gradiente de presión.
- Hemofiltración Veno-Veno Continua (CVVH): Técnica convectiva donde un gradiente de presión generado por una bomba de sangre fuerza el paso de la sangre a través del filtro, eliminando agua y electrolitos. Genera un gran volumen de ultrafiltrado, requiriendo líquido de sustitución.
- Hemofiltración Veno-Veno Continua de Alto Volumen (HVCVVH): Variante de la CVVH con volúmenes de extracción superiores, administrados durante 24 horas.
Hemodiálisis Veno-Veno Continua (CVVHD): Modalidad que utiliza la difusión de partículas entre la sangre y el líquido dializante como principal mecanismo de mejora del fluido tratado. Un flujo lento de dializante a contracorriente del flujo sanguíneo facilita la difusión de moléculas de pequeño tamaño hasta igualar concentraciones.
Hemodiafiltración Veno-Veno Continua (CVVHDF): Combina los beneficios de la hemodiálisis y la hemofiltración, empleando tanto la convección como la difusión. Permite la eliminación de partículas por diferencia de concentración y altos volúmenes de líquido por presión. Requiere el uso de solución de diálisis y líquido de sustitución.
La aplicación de estas técnicas, especialmente en pacientes pediátricos, requiere equipos especializados y personal altamente capacitado para monitorizar y gestionar los posibles inconvenientes, como la coagulación del circuito.
Las terapias adsortivas, al dirigirse a la eliminación de mediadores inflamatorios y toxinas específicas, representan una evolución significativa en el manejo del paciente crítico. La continua investigación en nuevos materiales y el perfeccionamiento de las técnicas existentes prometen optimizar aún más el soporte vital y mejorar los resultados clínicos en pacientes con patologías complejas.
tags: #cartucho #sustancia #adsorbente #tecnica #depuracion