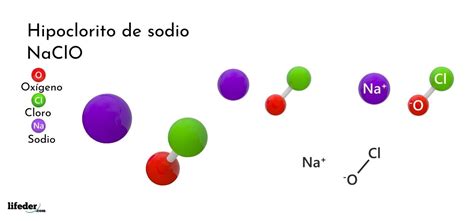
El hipoclorito de sodio, cuya fórmula química se representa comúnmente como NaClO o, de forma más precisa electrónicamente, como NaOCl, es una sal de hipoclorito de gran relevancia y uso extendido. Su característica principal es su fácil solubilidad en agua, lo que facilita su aplicación en diversas industrias y en el hogar. La potencia oxidante del hipoclorito de sodio, especialmente en medios ácidos, lo convierte en un componente esencial en la formulación de productos de limpieza, actuando como blanqueador y desinfectante. Un ejemplo paradigmático es el "Disinfectante 84", cuyo principal ingrediente activo es el hipoclorito de sodio. Más allá de su uso doméstico, su aplicación se extiende al tratamiento de aguas residuales, donde cumple una función purificadora crucial, y a la desinfección en diversos procesos industriales, incluyendo la industria textil.

A pesar de su utilidad, el hipoclorito de sodio es intrínsecamente inestable. La luz y el calor son factores que propician su rápida descomposición. Por esta razón, tanto en el ámbito cotidiano como en la producción industrial, se maneja predominantemente en forma de solución acuosa. Si bien teóricamente es posible obtenerlo en estado sólido, esta forma es menos común y se reserva principalmente para entornos de laboratorio. Los métodos de producción industrial más empleados para obtener hipoclorito de sodio son la electrólisis de soluciones salinas y la cloración de sosa cáustica. Es importante destacar que, en 2017, la Agencia Internacional para la Investigación del Cáncer de la Organización Mundial de la Salud clasificó a los hipocloritos dentro del Grupo 3 de carcinógenos, lo que indica una falta de evidencia concluyente sobre su carcinogenicidad en humanos.
Propiedades Físico-Químicas y Reactividad
El hipoclorito de sodio puro se presenta como un sólido de color blanco, mientras que sus soluciones acuosas suelen exhibir un tono amarillo pálido y despiden un olor característico e irritante. Esta dualidad en su apariencia subraya la importancia de la concentración y el estado físico en la caracterización del compuesto.
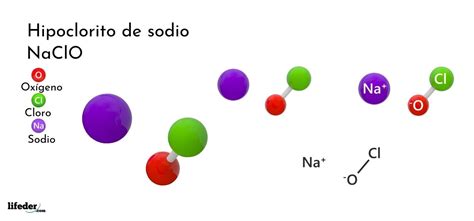
Entre sus propiedades físico-químicas, se destaca su naturaleza como sal derivada de la reacción entre una base fuerte, el hidróxido de sodio (NaOH), y un ácido débil, el ácido hipocloroso (HClO). Esta combinación es fundamental para comprender su comportamiento en solución acuosa.
Debil Basicidad y Reacción de Hidrólisis
Debido a su origen a partir de un ácido débil y una base fuerte, el hipoclorito de sodio experimenta una reacción de hidrólisis en agua. Este proceso confiere a las soluciones acuosas de NaClO un carácter ligeramente alcalino. La reacción de hidrólisis se describe de la siguiente manera:
NaClO + H₂O ⇌ HClO + NaOH
La constante de equilibrio de esta reacción de hidrólisis (Kh) a 25 °C se puede calcular a partir de la constante de disociación del ácido hipocloroso (Ka) a la misma temperatura, que es de aproximadamente 2.9×10⁻⁸. La relación entre estas constantes es:
Kh = Kw / Ka
Donde Kw es la constante del producto iónico del agua (1.0×10⁻¹⁴ a 25 °C). Por lo tanto, la constante de hidrólisis del NaClO es:
Kh = 1.0×10⁻¹⁴ / 2.9×10⁻⁸ ≈ 3.45×10⁻⁷
Este valor de Kh, significativamente menor que 1, indica que la hidrólisis es un proceso limitado, pero suficiente para impartir una basicidad medible a la solución.
Reacciones con Ácidos: Peligros y Consideraciones
La naturaleza básica del hipoclorito de sodio lo hace susceptible a reaccionar con ácidos en reacciones de neutralización. Estas reacciones pueden ser particularmente peligrosas si no se manejan adecuadamente.
Con Ácido Clorhídrico Diluido:NaClO + HCl(diluido) → NaCl + HClOEn esta reacción, se forma ácido hipocloroso, que a su vez es inestable.
Con Ácido Clorhídrico Concentrado:NaClO + 2HCl(conc.) → NaCl + Cl₂↑ + H₂OLa reacción con ácido clorhídrico concentrado es de particular importancia debido a la liberación de cloro molecular (Cl₂). El cloro es un gas tóxico, de color verde amarillento, que puede ser extremadamente dañino si se inhala. Este es el motivo por el cual productos como el "Disinfectante 84" (a base de hipoclorito de sodio) y limpiadores de inodoros (que a menudo contienen ácidos como el clorhídrico) nunca deben mezclarse. La inhalación de cloro puede causar daños severos en el tracto respiratorio y los pulmones.
Con Dióxido de Carbono (Ácido Carbónico):CO₂ + H₂O + 2NaClO → Na₂CO₃ + 2HClOEsta reacción es relevante para entender el efecto blanqueador del hipoclorito de sodio. Cuando la tela empapada en lejía se expone al aire, reacciona con el dióxido de carbono atmosférico (que forma ácido carbónico en solución acuosa) para generar ácido hipocloroso (HClO). La generación in situ de este ácido, que es un oxidante más fuerte que el ion hipoclorito, potencia la acción blanqueadora. La constante de disociación primaria del ácido carbónico (H₂CO₃) es de 4.5×10⁻⁷.
La advertencia de seguridad S50A, "No mezclar con ácidos", y la frase de peligro R31, "El contacto con ácidos libera gas tóxico", resaltan la criticidad de evitar la combinación de hipoclorito de sodio con sustancias ácidas.
Inestabilidad y Descomposición
El hipoclorito de sodio, si bien es relativamente estable a bajas temperaturas (entre 15~25 °C), es sensible a la luz y al calor. La exposición a la luz solar, especialmente a la radiación ultravioleta, y a temperaturas elevadas acelera su descomposición. La descomposición se vuelve más violenta a medida que aumenta la temperatura, alcanzando un punto crítico alrededor de los 70 °C, donde puede ocurrir una descomposición explosiva debido a la generación de especies reactivas de oxígeno.
Las principales vías de descomposición incluyen:
- Descomposición a cloruro de sodio y oxígeno:2NaClO → 2NaCl + O₂↑
- Reacción con oxígeno para formar cloratos:NaClO + O₂ → NaClO₃
- Generación de oxígeno atómico:NaClO → NaCl + [O]
Esta inestabilidad dicta las condiciones de almacenamiento y transporte. Se recomienda almacenar el hipoclorito de sodio en ambientes fríos y protegidos de la luz, utilizando recipientes opacos como frascos de color ámbar en el laboratorio.
HIPOCLORITO de Sodio 5 Preguntas & 5 Respuestas [QUÍMICA Oculta]
Métodos de Producción Industrial
La diversidad de aplicaciones del hipoclorito de sodio ha impulsado el desarrollo de varios métodos para su producción a escala industrial. La elección del método a menudo depende de factores económicos, la disponibilidad de materias primas y las consideraciones ambientales.
Método de Electrólisis de Solución Salina
Este método utiliza una solución acuosa de cloruro de sodio (sal común) como materia prima. El proceso de electrólisis genera hidróxido de sodio en el cátodo y cloro en el ánodo. Estos productos reaccionan internamente para formar hipoclorito de sodio y cloruro de sodio. Las reacciones clave son:
- Electrólisis del agua salada:2NaCl + 2H₂O → 2NaOH + Cl₂↑ + H₂↑
- Reacción del cloro con hidróxido de sodio:Cl₂ + 2NaOH → NaCl + NaClO + H₂O
Una desventaja significativa de esta ruta es su alto consumo de energía eléctrica. Además, el contenido de cloro activo en la solución resultante suele ser relativamente bajo, alrededor del 5%, lo que limita su eficiencia económica. Por estas razones, no es el método de producción principal en la actualidad.
Método de Cloración de Carbonato de Sodio
En este método, el cloro gaseoso se burbujea a través de una solución de carbonato de sodio (Na₂CO₃). Las reacciones involucradas son:
- Disolución del cloro en agua:Cl₂ + H₂O → HClO + HCl
- Reacción del carbonato de sodio con los ácidos formados:Na₂CO₃ + HClO + HCl → NaCl + NaClO + H₂O + CO₂↑Alternativamente, la reacción directa puede ser representada como:Cl₂ + Na₂CO₃ → NaCl + NaClO + CO₂
Esta ruta permite obtener soluciones de hipoclorito de sodio con un contenido de cloro activo de hasta el 10%. Sin embargo, uno de sus principales inconvenientes es la generación de una cantidad considerable de dióxido de carbono (CO₂), lo que plantea desafíos en términos de control de emisiones de carbono y puede complicar el proceso de purificación del producto.
Método de Cloración de Sosa Cáustica
Este es actualmente uno de los métodos más utilizados y eficientes para la producción de hipoclorito de sodio. La materia prima principal es el hidróxido de sodio (NaOH), comúnmente conocido como sosa cáustica. El proceso implica hacer reaccionar cloro gaseoso con una solución concentrada de sosa cáustica:
Cl₂ + 2NaOH → NaCl + NaClO + H₂O
Este método es ventajoso porque puede producir soluciones de hipoclorito de sodio con un contenido de cloro activo de hasta el 13%, y es generalmente más económico y eficiente energéticamente que la electrólisis.
Investigaciones recientes han explorado el uso de reactores de microcanales para la producción continua de hipoclorito de sodio. Estos dispositivos prometen mejoras significativas en términos de ahorro de energía y protección ambiental, al permitir un control más preciso de las condiciones de reacción y una mejor transferencia de calor y masa.
Usos y Aplicaciones Diversas
La combinación de su poder oxidante, su naturaleza desinfectante, su bajo costo y su facilidad de producción ha cimentado la amplia gama de aplicaciones del hipoclorito de sodio en múltiples sectores.
- Blanqueador y Desinfectante Doméstico: Es el componente principal de productos de limpieza como la lejía, la lavandina y el "Disinfectante 84", utilizados para eliminar manchas, desinfectar superficies y eliminar olores.
- Tratamiento de Aguas: Juega un papel vital en la potabilización del agua y el tratamiento de aguas residuales, eliminando bacterias, virus y otros microorganismos patógenos.
- Industria Textil: Se emplea para el blanqueo de fibras textiles, como el algodón, para eliminar impurezas y prepararlas para el teñido.
- Industria del Papel: Utilizado en el proceso de blanqueo de la pulpa de madera para obtener papel de alta blancura.
- Industria Farmacéutica y Química Fina: Interviene en la síntesis de diversos compuestos orgánicos e inorgánicos y como agente desinfectante en instalaciones de producción.
- Desinfección Sanitaria: Ampliamente utilizado para desinfectar hospitales, clínicas y otros entornos donde la higiene es primordial.
- Piscinas: Se usa para desinfectar el agua de las piscinas, ya sea directamente en forma líquida, en pastillas o polvo, o mediante sistemas de electrólisis salina que generan hipoclorito in situ.
Es importante señalar que el hipoclorito de sodio tiene ciertas incompatibilidades. Por ejemplo, no debe utilizarse en procesos de producción de alimentos que empleen sésamo como materia prima.
Especificaciones y Formulaciones
Las especificaciones de los productos de hipoclorito de sodio varían según su forma y el contenido de "cloro activo", que es la medida de su poder desinfectante y blanqueador. Las concentraciones y formulaciones se adaptan a las necesidades específicas de cada aplicación.
Almacenamiento, Transporte y Seguridad
Dada su reactividad e inestabilidad bajo ciertas condiciones, el almacenamiento y transporte del hipoclorito de sodio requieren precauciones rigurosas.
Requerimientos de Almacenamiento y Transporte
- Embalaje: Los recipientes deben estar completos y asegurar la estanqueidad para evitar fugas. Durante el transporte, se debe garantizar que no se vuelquen, caigan o dañen.
- Incompatibilidades: Está estrictamente prohibido transportarlo mezclado con ácidos, productos químicos alimentarios u otras sustancias incompatibles.
- Condiciones Ambientales: Los vehículos de transporte deben protegerse de la exposición al sol, la lluvia y las altas temperaturas. En el caso de derrames accidentales, los vehículos deben estar equipados con material de respuesta a emergencias.
- Rutas de Transporte: Se deben seguir rutas establecidas, evitando áreas residenciales o densamente pobladas.
Medidas de Primeros Auxilios y Respuesta a Emergencias
Las frases de seguridad S26, S28A, S36/37/39 y S45 proporcionan directrices esenciales en caso de contacto accidental:
- Contacto con la Piel (S28A): Quitarse la ropa contaminada y lavar la piel afectada con abundante agua corriente.
- Contacto con los Ojos (S26): Levantar los párpados y lavar los ojos inmediatamente con abundante agua corriente o solución salina fisiológica. Buscar atención médica de inmediato.
- Inhalación: Trasladar a la persona afectada a un lugar con aire fresco. Mantener las vías respiratorias despejadas. Si hay dificultad para respirar, administrar oxígeno. Si la respiración se detiene, iniciar respiración artificial. Buscar atención médica de inmediato.
- Ingestión: Beber una cantidad suficiente de agua tibia. No inducir el vómito. Buscar atención médica a tiempo.
Características de Peligro y Métodos de Extinción
El hipoclorito de sodio es corrosivo y puede generar humos tóxicos y corrosivos al descomponerse a altas temperaturas. Los productos de combustión nocivos incluyen cloruros. En caso de incendio, se recomienda utilizar agua en forma de rocío, dióxido de carbono o arena seca para extinguir las llamas.
Manejo de Derrames
En caso de derrame, se deben seguir los siguientes pasos:
- Evacuación: Evacuar al personal del área contaminada hacia una zona segura y aislar el perímetro.
- Protección del Personal de Respuesta: El personal de emergencia debe utilizar equipo de protección adecuado, incluyendo respiradores autónomos y trajes resistentes a ácidos y álcalis.
- Control de la Fuga: Si es posible, cortar la fuente de la fuga.
- Contención y Absorción: Para derrames de pequeña cantidad, absorber con materiales inertes como arena o vermiculita. Para derrames de gran cantidad, construir diques de contención o cavar fosos para confinar el material. Cubrir con espuma para reducir la emanación de vapores.
- Recuperación y Tratamiento: Transferir el material mediante bombeo a contenedores especializados para su recuperación o envío a una instalación de tratamiento de residuos.
Control de Ingeniería y Equipo de Protección Personal
Para minimizar la exposición y garantizar la seguridad en entornos de producción y manipulación:
- Control de Ingeniería: Los procesos de producción deben realizarse en sistemas cerrados con ventilación general adecuada. Se deben instalar duchas de seguridad y estaciones lavaojos.
- Protección Respiratoria: En ambientes con alta concentración de vapores, se debe usar una máscara antigás con filtro adecuado.
- Protección Ocular: Gafas de seguridad química son imprescindibles.
- Protección Corporal: Ropa de trabajo resistente a la corrosión.
- Protección de Manos: Guantes de goma o materiales resistentes a químicos.
- Higiene Personal: Está prohibido fumar, comer o beber en el área de trabajo. Se debe practicar una buena higiene personal, incluyendo ducharse y cambiarse de ropa al finalizar la jornada laboral.
La frase de peligro R34 ("Provoca quemaduras") y R36/37/38 ("Irritante para los ojos, las vías respiratorias y la piel") refuerzan la necesidad de un manejo cuidadoso y el uso de equipo de protección adecuado.
Consideraciones Adicionales
La constante de acidez (Ka) del ácido hipocloroso es un parámetro fundamental para entender la química del hipoclorito de sodio. Un valor de Ka de 2.9×10⁻⁸ indica que el ácido hipocloroso es un ácido débil. Esta debilidad es la razón por la cual su sal, el hipoclorito de sodio, produce soluciones básicas debido a la hidrólisis. La comprensión de estas constantes de acidez y basicidad es crucial para predecir el comportamiento del hipoclorito de sodio en diversas condiciones químicas y para optimizar su uso en aplicaciones específicas.
El hipoclorito de sodio es un compuesto químico de gran versatilidad, cuya utilidad se extiende a numerosos campos. Sin embargo, su manejo seguro y responsable es primordial debido a su reactividad y potencial para generar sustancias peligrosas. La información detallada sobre sus propiedades, métodos de producción, aplicaciones y medidas de seguridad es esencial para garantizar su uso efectivo y minimizar los riesgos asociados.