La comprensión de los diagramas de fases es fundamental para el diseño y la operación eficiente de cualquier proceso que involucre la manipulación de sustancias, incluidas las plantas potabilizadoras de agua. Un diagrama de fases es una representación gráfica que muestra las condiciones de presión y temperatura bajo las cuales una sustancia puede existir en diferentes estados físicos, o fases. Estas fases son porciones de un sistema con composición y estructura definidas, separadas de otras fases vecinas por una interfase.
Componentes y Fases: Una Distinción Clave
Es crucial distinguir entre un "componente" y una "fase". Un componente se refiere a una sustancia química concreta. Por ejemplo, en un vaso que contiene agua líquida y un cubito de hielo, hay dos fases distintas: el agua en estado sólido (hielo) y el agua en estado líquido. Sin embargo, solo existe un componente: el agua (H₂O). Esta distinción es esencial al analizar la complejidad de los sistemas.
El Diagrama de Fases: Un Mapa de Estados
Los diagramas de fases, particularmente aquellos que representan sistemas con un solo componente y la posibilidad de existir en tres fases (sólida, líquida y gaseosa), se representan típicamente en un gráfico de presión (P) versus temperatura (T). Este gráfico permite visualizar las diferentes zonas donde cada fase es estable, así como las líneas que delimitan las condiciones en las que coexisten dos fases en equilibrio.
En términos generales, la región de alta presión y baja temperatura en un diagrama de fases corresponde al estado sólido. Por el contrario, la zona de baja presión y alta temperatura es característica del estado gaseoso. Las líneas que cruzan el diagrama representan las condiciones específicas de presión y temperatura en las que dos fases pueden coexistir en equilibrio termodinámico.
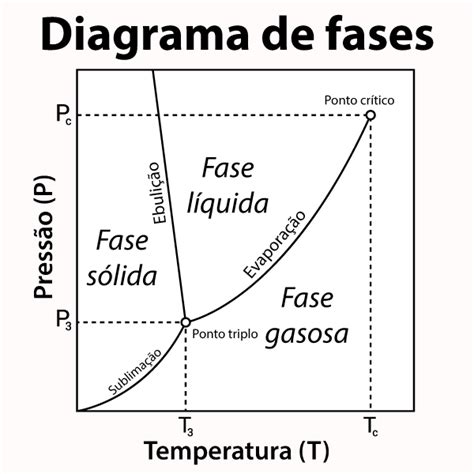
Puntos Singulares: El Punto Triple y el Punto Crítico
Dentro de un diagrama de fases, existen puntos de particular interés, conocidos como puntos singulares. Uno de ellos es el punto triple, donde las tres fases (sólida, líquida y gaseosa) coexisten en equilibrio. En este punto, el sistema tiene cero grados de libertad, lo que significa que tanto la presión como la temperatura están fijadas y no pueden variar independientemente. Para el agua, el punto triple se encuentra a una temperatura de 0,01 °C y una presión de 0,00604 atm. Este punto es significativo porque representa la presión más baja a la que el agua puede existir en estado líquido. Por debajo de esta presión, el hielo en equilibrio con el vapor no funde al aumentar la temperatura, sino que se sublima directamente a gas.
El otro punto singular es el punto crítico. En este punto, la distinción entre las fases líquida y gaseosa desaparece. Superando el punto crítico, la sustancia entra en el estado de fluido supercrítico, una fase con propiedades intermedias entre las de un líquido y un gas, poseyendo alta densidad y baja viscosidad.
La Ecuación de Clapeyron y la Pendiente de las Curvas
La pendiente de las líneas en un diagrama de fases P-T está gobernada por la ecuación de Clapeyron. Esta ecuación relaciona el cambio de presión con el cambio de temperatura en el equilibrio entre dos fases, y su signo está directamente asociado con el cambio en el volumen molar durante la transición de fase. Dado que la entalpía de cambio de estado y la temperatura son siempre positivas, el signo de la pendiente de las curvas P-T está determinado principalmente por el signo del cambio de volumen.
En la mayoría de las sustancias, la densidad del gas es significativamente menor que la del líquido, y la del líquido menor que la del sólido. Por lo tanto, el volumen molar aumenta al pasar de sólido a líquido y de líquido a gas. Esto generalmente resulta en una pendiente positiva para las líneas de equilibrio, indicando que un aumento en la presión requiere un aumento en la temperatura para mantener el equilibrio entre fases.
El Caso Particular del Agua: Una Anomalía Fascinante
El diagrama de fases del agua presenta características únicas que lo diferencian de la mayoría de las sustancias. A una presión atmosférica estándar de 1 atm, el agua cambia de estado sólido a líquido a 0 °C (punto de fusión) y de líquido a gas a 100 °C (punto de ebullición). Sin embargo, si la presión disminuye, como ocurre en altitudes elevadas, el punto de fusión del hielo se eleva ligeramente y el punto de ebullición del agua desciende por debajo de los 100 °C. En estas condiciones de menor presión, el intervalo de temperaturas en el que el agua existe en estado líquido se estrecha.
Una de las anomalías más notables del diagrama de fases del agua es la inclinación de la línea sólido-líquido. En lugar de inclinarse hacia la derecha (pendiente positiva), como es común en la mayoría de las sustancias, esta línea se inclina hacia la izquierda (pendiente negativa). Esto implica que, a medida que aumenta la presión, la temperatura de fusión del hielo disminuye. Por ejemplo, a una presión de 200 atm, el hielo funde a -1,6 °C.
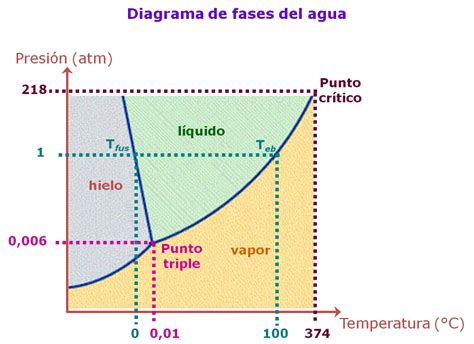
Esta propiedad se debe a que el hielo es menos denso que el agua líquida. En sustancias como el antimonio o el bismuto, que también presentan un sólido menos denso que el líquido, se observa un comportamiento similar.
Implicaciones en Entornos Extraterrestres y Procesos Industriales
Las características del diagrama de fases del agua tienen importantes implicaciones, incluso fuera de la Tierra. La presión en la superficie de la Luna es considerablemente inferior a la del punto triple del agua. Por lo tanto, en la Luna no puede existir agua en estado líquido. Sin embargo, se ha detectado hielo de agua en los cráteres lunares que permanecen en oscuridad permanente, especialmente en los polos. Dada la ausencia de atmósfera y la presión casi nula en la superficie lunar, cualquier hielo expuesto a la luz solar directa o a fluctuaciones de temperatura experimentaría sublimación, pasando directamente del estado sólido al gaseoso.
Otro ejemplo relevante es el dióxido de carbono (CO₂). A presiones inferiores a 5,11 atm, el CO₂ no puede existir en estado líquido. En condiciones normales de presión y temperatura (aproximadamente 1 atm y 25 °C), el CO₂ sublima directamente de sólido a gas, lo que se conoce comúnmente como "hielo seco".
DIAGRAMA DE FASES
Aplicaciones en Plantas Potabilizadoras
Aunque los diagramas de fases se centran en las transiciones de estado de una sustancia pura, los principios subyacentes son relevantes para las plantas potabilizadoras. La gestión de la temperatura y la presión son cruciales en diversos procesos de tratamiento de agua. Por ejemplo:
- Congelación y Descongelación: En climas fríos, la prevención de la congelación de tuberías y equipos es vital. Comprender el punto de congelación del agua a diferentes presiones ayuda a diseñar sistemas de calefacción o aislamiento adecuados. La inclinación negativa de la línea sólido-líquido del agua significa que la presión puede usarse para influir en la temperatura de congelación, aunque esto no es una práctica común en la potabilización.
- Evaporación y Condensación: En procesos que involucran la eliminación de impurezas volátiles o la desalinización por evaporación, el conocimiento preciso de los puntos de ebullición y condensación a diferentes presiones es esencial para optimizar el consumo de energía y la eficiencia del proceso.
- Tratamiento Térmico: Algunos métodos de desinfección o tratamiento pueden implicar la aplicación de calor. La comprensión de cómo la presión afecta la temperatura de ebullición permite controlar la esterilización o la inactivación de patógenos de manera efectiva.
- Gestión de Aguas Subterráneas: La presión del agua subterránea puede variar, y si bien no se trata de cambios de fase en el sentido estricto, la presión es un factor determinante en la extracción y el flujo del agua.
- Formación de Escarcha y Hielo en Equipos: En instalaciones al aire libre, la formación de escarcha o hielo en superficies expuestas puede afectar el rendimiento de los equipos. La comprensión de las condiciones de presión y temperatura que favorecen la transición de vapor a hielo (deposición) es relevante para el mantenimiento preventivo.
En resumen, aunque los diagramas de fases de sustancias puras pueden parecer un concepto de la química fundamental, los principios que rigen las transiciones de estado y las relaciones presión-temperatura son de gran utilidad para el diseño, la operación y la resolución de problemas en una amplia gama de aplicaciones de ingeniería, incluidas las plantas potabilizadoras de agua. La capacidad de predecir y controlar el comportamiento de la materia bajo diversas condiciones es clave para garantizar el suministro de agua potable segura y eficiente.