El "salting out", o expulsión salina, es un fenómeno fisicoquímico fascinante que demuestra la compleja interacción entre solutos, solventes y la presencia de sales. En esencia, se refiere a la reducción de la solubilidad de ciertas moléculas en soluciones acuosas cuando la concentración de sal es significativamente alta. Este efecto, aunque a primera vista pueda parecer contraintuitivo, es de gran importancia en diversos campos, desde la purificación de biomoléculas hasta la comprensión fundamental de los equilibrios de fases líquido-líquido.
Definición y Mecanismo Fundamental
La expulsión salina se manifiesta cuando la adición de una sal a una mezcla de disolventes miscibles provoca la separación de esta en dos o más fases líquidas inmiscibles. Un ejemplo clásico y visualmente impactante es la mezcla de agua y propan-2-ol. Estos dos componentes son completamente miscibles en condiciones normales, capaces de formar enlaces por puentes de hidrógeno que favorecen su mezcla. Sin embargo, al añadir una cantidad suficiente de cloruro de sodio (NaCl), la mezcla se vuelve inestable y se separa en dos fases líquidas. Una fase será predominantemente acuosa y rica en sal, mientras que la otra será orgánica y concentrada en propan-2-ol, aunque ambas contendrán trazas de los otros componentes.
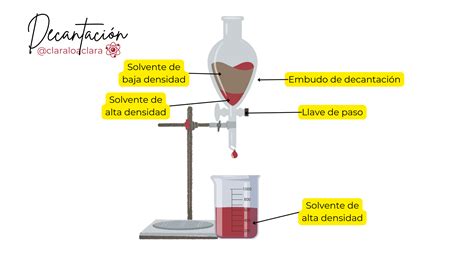
El mecanismo subyacente se relaciona con la competencia por las moléculas de agua. En una solución acuosa, las moléculas de agua forman capas de hidratación alrededor de los iones de la sal debido a las intensas interacciones atractivas ion-dipolo. Estas moléculas de agua "ocupadas" por los iones ya no están tan disponibles para interactuar y solvatar a otras moléculas, como el propan-2-ol. Cuando la concentración de sal es alta, la "demanda" de agua por parte de los iones es tan elevada que se reduce drásticamente la capacidad del agua para mantener disueltas las moléculas orgánicas, forzándolas a agruparse y separarse en una fase distinta. En términos termodinámicos, la minimización de la energía libre del sistema se logra a través de la formación de dos fases líquidas cuando no hay suficiente agua para solvatar eficientemente tanto los iones como las moléculas de propan-2-ol.
Este fenómeno es conocido como "salting out" porque la sal parece "expulsar" al soluto orgánico (en este caso, el propan-2-ol) de la fase acuosa. La inestabilidad de la mezcla se intensifica cuando la fracción de agua no es muy grande, ya que se requiere una cantidad significativa de agua para solvatar tanto los iones como las moléculas de alcohol. Si se aumenta la cantidad de agua, la miscibilidad puede restablecerse, formando una única fase homogénea.
Aplicaciones en la Purificación
La propiedad fundamental del "salting out" de reducir la solubilidad de ciertas moléculas en soluciones acuosas de alta fuerza iónica lo convierte en una herramienta valiosa para la purificación. Se emplea comúnmente en el laboratorio y en la industria para aislar y concentrar biomoléculas, especialmente proteínas.
Purificación de Proteínas:
Las proteínas, al ser macromoléculas complejas con regiones hidrofóbicas e hidrofílicas, interactúan de manera específica con el agua y las sales. En soluciones acuosas con alta fuerza iónica, las sales compiten por las moléculas de agua, lo que disminuye la hidratación de las proteínas. Esto aumenta las interacciones hidrofóbicas entre las propias moléculas de proteína, promoviendo su agregación y precipitación.
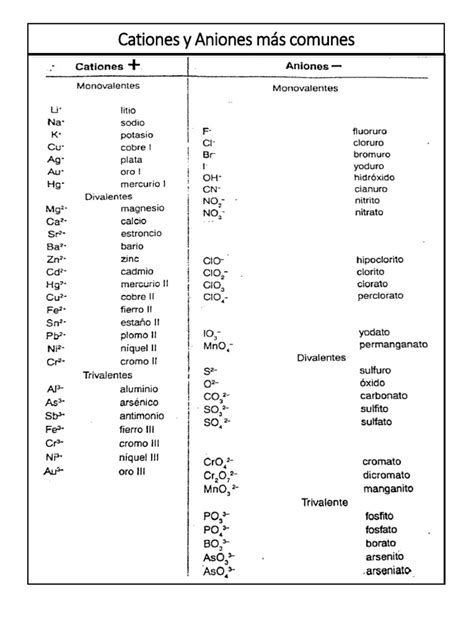
La elección de la sal y su concentración es crucial para la precipitación selectiva. Diferentes sales tienen distintas capacidades para inducir la precipitación, un concepto encapsulado en la Serie de Hoffmeister. Esta serie ordena aniones y cationes según su capacidad para afectar la solubilidad de las proteínas. Por ejemplo, el sulfato de amonio ((NH₄)₂SO₄) es una sal frecuentemente utilizada debido a la alta posición de sus iones en la Serie de Hoffmeister, lo que la hace muy eficaz para precipitar proteínas.
Es importante destacar que, si bien el "salting out" es un método eficaz para una purificación inicial y para concentrar soluciones de proteínas, puede carecer de la precisión necesaria para aislar una proteína específica de una mezcla compleja. La concentración de sal requerida para precipitar una proteína particular varía según su tamaño, carga y superficie, pero la separación no siempre es completamente selectiva.
Otras Aplicaciones:
Más allá de las proteínas, el "salting out" se utiliza para la purificación de otras biomoléculas grandes como el ADN. También se ha empleado en la preparación de partículas proteicas, como las basadas en proteínas de seda de gusano, y en la encapsulación de moléculas pequeñas mediante la precipitación salina de polímeros.
El principio también se observa en procesos cotidianos. Por ejemplo, se cree que la sal común y el vinagre ayudan en el proceso de cocción de los huevos, en parte, a través de mecanismos relacionados con la expulsión salina que promueven la coagulación de las proteínas del huevo.
Visualización y Demostraciones Educativas
La demostración del fenómeno de "salting out" puede ser muy efectiva en entornos educativos, especialmente porque a menudo presenta un efecto inesperado o contra-intuitivo, lo que capta la atención del alumnado. Una demostración común implica una botella agitada que contiene una mezcla de agua y propan-2-ol junto con cuentas de plástico de colores, por ejemplo, azules y blancas. Al dejar reposar la botella, los estudiantes esperan que las cuentas simplemente se asienten. Sin embargo, la sucesión de eventos es más compleja. Inicialmente, las cuentas pueden separarse, pero luego, de manera lenta, tienden a agruparse en el centro de la botella, manteniendo las blancas en la parte superior y las azules en la inferior. Esta observación les obliga a razonar sobre las fuerzas y las interacciones que están ocurriendo en el líquido.
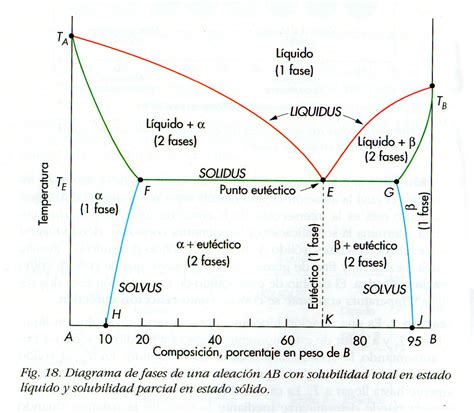
El estudio de la región de miscibilidad líquido-líquido en sistemas ternarios (como agua-NaCl-propan-2-ol) es fundamental para comprender el equilibrio de fases y los fenómenos críticos asociados. Los diagramas de fases, como el del sistema agua+NaCl+propan-2-ol a 1 bar y 25 ºC, ilustran claramente la región de inmiscibilidad líquido-líquido. En estos diagramas, se puede observar cómo una composición media específica, como la de 10.0 % NaCl, 52.0 % agua y 38.0 % propan-2-ol (en masa), cae dentro de esta región, indicando la formación de dos fases líquidas.
El "Salting Out" en el Contexto de Equilibrios de Fases
El fenómeno de "salting out" es una manifestación de los equilibrios de fases en sistemas multicomponentes. La adición de un tercer componente (la sal) a una mezcla binaria miscible puede alterar drásticamente las interacciones intermoleculares y la estabilidad termodinámica del sistema.
Consideremos el sistema agua-fenol, que presenta una región de inmiscibilidad con una temperatura crítica superior de 68 ºC. Al añadir una pequeña cantidad de NaCl (aproximadamente un 2 % en masa), esta región de inmiscibilidad se ensancha, lo que significa que las solubilidades del agua en fenol y del fenol en agua se reducen aún más. Esto indica que la sal está promoviendo la separación de las fases.
La capacidad de tener múltiples fases líquidas coexistiendo en un recipiente es un concepto que puede sorprender a muchos. De hecho, en sistemas complejos, se pueden observar hasta diez fases líquidas inmiscibles simultáneamente, un hecho ilustrado en obras clásicas de la termodinámica de soluciones.
Consideraciones Adicionales y Términos Relacionados
Es importante distinguir el "salting out" del fenómeno opuesto, el "salting in". Mientras que el "salting out" ocurre en soluciones acuosas de alta fuerza iónica y reduce la solubilidad de ciertas moléculas, el "salting in" puede ocurrir a concentraciones de sal más bajas y, en algunos casos, puede aumentar la solubilidad de ciertas proteínas.
El término "salting out" también se conoce por otras denominaciones, como precipitación inducida por sal, fraccionamiento de la sal, cristalización antisolvente o ahogamiento. En el contexto de la purificación de proteínas, se utiliza para precipitar selectivamente macromoléculas. La eficacia de la precipitación depende de la naturaleza del soluto, la sal empleada y su concentración.
La intensa interacción entre iones y agua, formando capas de hidratación, es un factor clave. Cuando esta interacción es muy fuerte, como en el caso de sales con iones que se encuentran altos en la Serie de Hoffmeister, la capacidad del agua para disolver otros solutos se ve comprometida.
Conclusión
El fenómeno de "salting out" es un principio fundamental en química física con profundas implicaciones prácticas. Demuestra cómo las interacciones intermoleculares y la competencia por el solvente pueden alterar radicalmente la miscibilidad y la solubilidad. Desde la purificación de biomoléculas hasta la enseñanza de conceptos termodinámicos complejos, la expulsión salina ofrece una ventana fascinante al comportamiento de las soluciones y al control de los equilibrios de fases. Su naturaleza a menudo contra-intuitiva lo convierte en una herramienta pedagógica poderosa, capaz de estimular el razonamiento crítico y la curiosidad científica.
tags: #salting #out #purificacion #definicion