La conductimetría es una técnica analítica fundamental en química que se basa en la medición de la conductividad eléctrica de las disoluciones iónicas. Esta propiedad inherente de las disoluciones se debe a la presencia de iones libres, tanto cationes como aniones, capaces de moverse y transportar carga eléctrica entre dos electrodos sumergidos en la disolución. La conductimetría encuentra aplicación en el seguimiento y control de reacciones iónicas, especialmente en medios como el agua, y como método para determinar el punto final en valoraciones volumétricas donde intervienen iones con distintas conductividades específicas.
Principios Fundamentales de la Conductividad en Disoluciones
Las disoluciones electrolíticas poseen la capacidad de conducir la corriente eléctrica cuando se les aplica una diferencia de potencial entre dos electrodos. La relación entre la diferencia de potencial (V), la resistencia (R) y la intensidad de la corriente (I) se describe por la Ley de Ohm (V = I * R). A diferencia de los conductores metálicos, donde el transporte de carga lo realizan electrones, en las disoluciones electrolíticas, son los iones en movimiento los responsables de la conducción eléctrica.
La resistencia que ofrecen los iones al paso de la corriente está directamente relacionada con la resistividad específica (ρ), un coeficiente de proporcionalidad que depende de la longitud y el área del conductor. La resistividad específica es una propiedad característica de cada disolución y está influenciada por la concentración total de iones, la temperatura y la carga de dichos iones.
En la práctica, se suele utilizar la conductividad total de la disolución, en lugar de la conductividad específica de cada ion individual. La unidad de medida de la conductancia en el Sistema Internacional (SI) es el siemens (S), que es la inversa del ohmio (S = 1/Ω). La conductividad específica se expresa comúnmente en siemens por metro (S·m⁻¹).
Un ejemplo ilustrativo es una disolución de cloruro de potasio (KCl) 0.01 M (0.745 g en un litro de agua pura), que presenta una conductividad de 0.1408 S·m⁻¹ a 25 °C. Debido a que este valor es relativamente pequeño, es habitual expresar las mediciones en mili siemens por centímetro (mS·cm⁻¹) o micro siemens por centímetro (µS·cm⁻¹).
Conductividad Específica vs. Conductividad Equivalente
La conductividad específica (κ) mide la conductividad de un volumen unitario de disolución y, aunque útil, no es la medida más práctica para comparar disoluciones de diferentes solutos o concentraciones. Esto se debe a que una mayor concentración de electrolito generalmente resulta en una mayor conductividad, y electrolitos diferentes, incluso a la misma concentración, pueden exhibir conductividades distintas debido a la naturaleza intrínseca de sus iones (carga, tamaño, movilidad).
Para realizar comparaciones significativas, se recurre a la conductividad equivalente (Λ), que relaciona la conductividad con la concentración del electrolito:
Λ = κ / c
donde 'c' es la concentración del electrolito expresada en equivalentes gramos por mililitro (g-eq/mL) o centímetro cúbico (cm³). En consecuencia, las unidades de la conductividad equivalente son siemens por centímetro cuadrado por equivalente (S·cm²/eq⁻¹).
Tradicionalmente, la normalidad (N), que representa el número de equivalentes gramo por litro de disolución, se utilizaba para expresar la concentración. Sin embargo, el uso de la normalidad está en declive en química, prefiriéndose cada vez más la molaridad.
Instrumentación y Metodología en Conductimetría
Para la medición de la conductividad eléctrica en disoluciones, se emplea un instrumento denominado conductímetro o conductivímetro. Este aparato consta de un medidor y una célula de conductividad, la cual se introduce en la disolución a analizar. El principio de funcionamiento del medidor se basa en circuitos de puente de Wheatstone, similares a los utilizados en ohmímetros.
La célula de medida típicamente contiene dos electrodos, a menudo de platino. Teóricamente, estos electrodos deberían ser láminas planas de 1 cm² separadas por 1 cm, pero por razones prácticas, suelen ser cilíndricos y concéntricos. La calibración previa del conductímetro hace que la geometría exacta de los electrodos no sea crítica, siempre que se mantenga la consistencia en las mediciones.
conductimetria
El proceso de medición implica sumergir la sonda en la disolución y aplicar un campo eléctrico entre los electrodos para medir la resistencia. Para prevenir reacciones de electrólisis o la formación de capas sobre los electrodos que puedan alterar la medición, se suelen emplear corrientes alternas de baja frecuencia.
Aplicaciones de la Conductimetría
La conductimetría es una técnica versátil con diversas aplicaciones en química analítica y control de calidad:
Conductimetría Directa
Este método consiste en medir directamente la conductividad de una disolución para obtener información cuantitativa sobre la concentración de iones. Aunque la conductividad no es específica de un ion particular, se pueden realizar análisis y aproximaciones valiosas.
Un uso destacado es la verificación de la pureza del agua destilada o desionizada. El agua pura tiene una conductividad extremadamente baja, cercana a 0.05 µS·cm⁻¹. Las mediciones conductimétricas permiten evaluar la calidad del agua producida por equipos desionizadores, tanto a nivel de laboratorio como industrial, y son cruciales para el mantenimiento de calderas de vapor, donde incluso trazas de impurezas iónicas pueden tener consecuencias significativas.
La conductimetría también se emplea para estimar el contenido salino en aguas naturales, particularmente en aguas continentales.
Valoraciones Conductimétricas
En las valoraciones conductimétricas, la medición de la conductividad se utiliza para identificar el punto final de una titulación. Dado que la conductividad de una disolución depende de los iones presentes y su concentración, el seguimiento de este parámetro durante la adición del valorante permite detectar el punto de equivalencia.
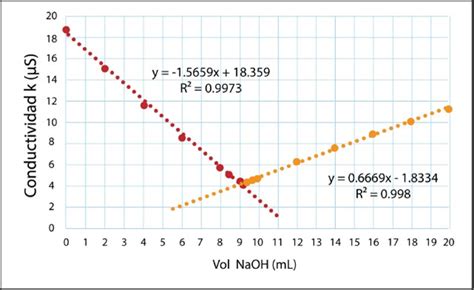
El procedimiento implica trazar una curva de conductividad versus el volumen de valorante añadido. La gráfica resultante mostrará un cambio de tendencia discernible en el punto de equivalencia, facilitando su determinación.
Valoración de Ácido Fuerte con Base Fuerte (Ejemplo: HCl con NaOH)
Al inicio de la valoración de un ácido fuerte como el HCl con una base fuerte como el NaOH, la disolución presenta una alta conductividad debido a la presencia de iones H⁺ y Cl⁻. Los iones H⁺, al poseer una movilidad excepcional (transportando protones o brechas de protones a través de enlaces de hidrógeno), contribuyen significativamente a la conductividad total.
A medida que se añade NaOH, los iones H⁺ son neutralizados y reemplazados por iones Na⁺, que tienen una menor movilidad. Esto provoca una disminución gradual de la conductividad. La concentración de iones Cl⁻ permanece constante durante toda la valoración.
En el punto de equivalencia, donde todo el HCl ha reaccionado con el NaOH, la conductividad alcanza su valor mínimo. Tras sobrepasar el punto de equivalencia, la adición de más NaOH introduce iones Na⁺ y OH⁻ en la disolución, incrementando bruscamente la conductividad.
Valoración de Ácido Fuerte con Base Débil (Ejemplo: HCl con NH₃)
En la titulación de un ácido fuerte con una base débil, como HCl con amoníaco (NH₃), la conductividad inicial es alta debido a la disociación completa del HCl. Al añadir la base débil, se forma el ion amonio (NH₄⁺) como producto de la reacción. La conductividad disminuye a medida que los iones H⁺ son reemplazados por iones NH₄⁺, que tienen menor movilidad. El punto de equivalencia se alcanza cuando todo el H⁺ ha reaccionado.
Valoración de Ácido Débil con Base Fuerte (Ejemplo: CH₃COOH con NaOH)
Al inicio de la valoración de un ácido débil como el ácido acético (CH₃COOH) con una base fuerte como el NaOH, la conductividad de la disolución es baja, ya que el ácido débil no se disocia completamente. Al añadir NaOH, se produce la reacción de neutralización formando agua. A medida que se añade NaOH, se forman iones acetato (CH₃COO⁻) y iones Na⁺, lo que provoca un aumento de la conductividad. El punto de equivalencia se alcanza cuando todo el ácido acético ha reaccionado con el hidróxido de sodio.
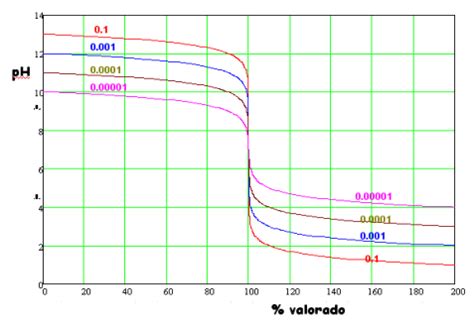
La ventaja principal de la valoración conductimétrica es que no requiere indicadores visuales, lo que permite el análisis de muestras coloreadas o turbias. Además, un único sensor de conductividad puede ser utilizado para diversas valoraciones.
La Importancia del Agua Destilada y su Conductividad
El agua destilada es un reactivo esencial en muchos laboratorios e industrias, y su pureza es un factor crítico. La etiqueta del agua destilada que se adquiere comercialmente suele indicar una conductividad específica, a menudo superior a 10 µS·cm⁻¹.
Existen mitos comunes sobre la obtención de agua destilada. Por ejemplo, el agua condensada de aparatos de aire acondicionado, aunque en parte destilada, puede contaminarse con residuos del equipo, haciéndola inadecuada para aplicaciones sensibles como autoclaves. De manera similar, el agua de sistemas de ósmosis inversa, si bien filtra impurezas, no produce agua destilada en su sentido más puro, ya que no elimina todos los sólidos disueltos ni desinfecta por completo.
Para verificar la calidad del agua destilada, se emplean pequeños dispositivos medidores de conductividad portátiles (tipo bolígrafo). Estos aparatos, económicos y duraderos, permiten confirmar si el agua adquirida cumple con las especificaciones de pureza, evitando así problemas y averías en equipos sensibles.
La conductividad del agua destilada es un indicador directo de su pureza. El agua pura tiene una conductividad teóricamente cercana a cero, ya que carece de iones disueltos. Cualquier valor medible de conductividad en agua destilada se debe a la presencia residual de impurezas iónicas.
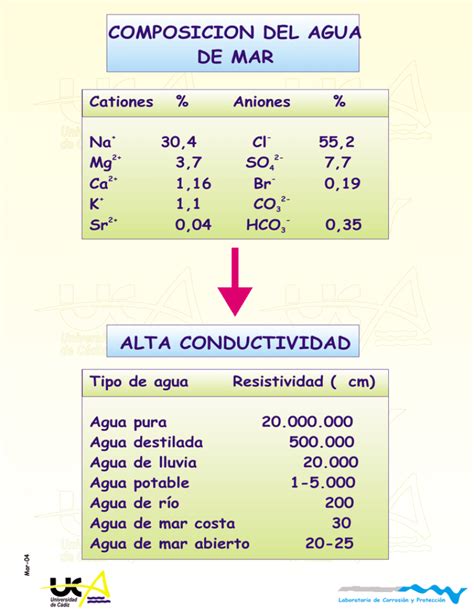
Comparativa: Agua Potable vs. Agua Destilada
El agua potable contiene minerales y sales disueltos que le otorgan una conductividad típica de entre 50 y 500 µS·cm⁻¹. En contraste, el agua destilada, tras el proceso de evaporación y condensación, se purifica de la mayoría de estos iones, resultando en una conductividad significativamente menor, idealmente por debajo de 1 µS·cm⁻¹.
Agua Destilada vs. Agua Desionizada
Aunque ambos tipos de agua se utilizan para purificar, difieren en su proceso de obtención y pureza:
Agua Destilada: Se obtiene por ebullición y posterior condensación del vapor. Este proceso elimina no solo iones, sino también otros compuestos volátiles y microorganismos, resultando en una pureza general muy alta. Es preferida en la industria farmacéutica para formulaciones de medicamentos, inyectables y limpieza de equipos críticos, garantizando la ausencia de contaminantes. En la industria cosmética, se usa como base para asegurar la pureza de cremas y lociones.
Agua Desionizada: Se produce mediante un proceso de intercambio iónico, donde resinas especiales eliminan los iones disueltos. Es ideal para aplicaciones donde la presencia de minerales puede interferir, como en la fabricación de pastillas y jarabes en la industria farmacéutica, o en laboratorios para la preparación de reactivos. En la industria cosmética, se emplea en champús y geles donde los minerales podrían afectar la consistencia o espuma.
Si bien el agua destilada tiende a ser más pura en general, el agua desionizada es efectiva para eliminar sales y minerales específicos.
Consideraciones sobre Sensores y Software en Valoraciones Conductimétricas
La selección del sensor adecuado es crucial para la precisión de las valoraciones conductimétricas. Sensores con tiempos de respuesta rápidos, como las celdas de medición de conductividad de 4 hilos o de 5 anillos, son altamente recomendables. Estos sensores, a menudo fabricados con materiales duraderos y de fácil limpieza, no requieren preacondicionamiento ni mantenimiento especial.
El software moderno, como el OMNIS, ofrece herramientas avanzadas para la evaluación de curvas conductimétricas. Funciones como la adición de tangentes óptimas, suavizado de datos, definición de rangos lineales y evaluación flexible de puntos finales, otorgan al usuario un control preciso sobre el análisis, garantizando resultados confiables y exactos en las valoraciones conductimétricas.
La valoración conductimétrica, como método analítico, representa una herramienta valiosa para la determinación de la concentración de compuestos iónicos en disoluciones, ofreciendo ventajas significativas sobre métodos clásicos, especialmente en el análisis de muestras complejas.
tags: #valoraciones #conductimetricas #agua #destilada