Introducción a la Naturaleza de los Gases y la Pureza del Agua
En diversas aplicaciones científicas y técnicas, desde la ingeniería química hasta el buceo recreativo, la comprensión precisa de las propiedades de los gases y la pureza del agua es fundamental. A menudo, simplificamos estos conceptos asumiendo comportamientos ideales, pero la realidad del mundo físico presenta matices que, ignorados, pueden llevar a errores significativos en cálculos y predicciones. Este artículo se adentra en dos áreas aparentemente dispares: el factor de compresibilidad (Z) de los gases reales, particularmente el aire, y las propiedades y usos del agua destilada, destacando la importancia de considerar las desviaciones de la idealidad y la pureza en nuestros entornos.
Comprendiendo el Factor de Compresibilidad (Z) en Gases Reales
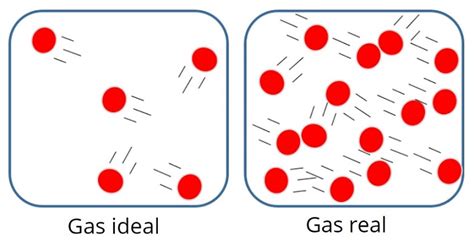
La teoría cinética de los gases, cuando se aplica al buceo y a otros campos, a menudo se basa en la suposición de que los gases se comportan como "gases ideales". Esta idealización se fundamenta en la relación lineal simple PV = nRT, donde P es la presión, V el volumen, n la cantidad de sustancia, R la constante de los gases ideales y T la temperatura. La premisa de un gas ideal es que ni el volumen ocupado por las propias moléculas del gas ni las interacciones electroestáticas entre ellas son consideradas.
Sin embargo, en condiciones de presiones y temperaturas no extremas, los gases reales se desvían de este comportamiento ideal. Las moléculas de gas, aunque pequeñas, ocupan un volumen finito, y entre ellas existen fuerzas de atracción y repulsión. Estas realidades influyen en la relación entre presión, volumen y temperatura. Para corregir el error inherente a la suposición de un gas ideal, se utiliza la ecuación de Van der Waals: (p + (a/V²))(V - b) = nRT. En esta ecuación, "a" representa un término asociado a las fuerzas de interacción intermolecular, y "b" es un término relacionado con el volumen molecular.
El factor de compresibilidad (Z) es una medida cuantitativa de esta desviación. Se define como la relación entre el volumen molar de un gas real y el volumen molar de un gas ideal a la misma temperatura y presión: Z = (Volumen molar real) / (Volumen molar ideal). Para un gas ideal, Z es siempre igual a 1. Para gases reales, Z puede ser mayor o menor que 1, dependiendo de las condiciones de presión y temperatura.
La ley de Henry, que describe la solubilidad de los gases en líquidos, también se ve influenciada por estas consideraciones. Cuando las presiones son relativamente mayores, las moléculas de gas se encuentran más próximas, aumentando la probabilidad de interacciones. De manera similar, un incremento en la temperatura aumenta la energía cinética de las moléculas, lo que puede llevar a colisiones más frecuentes y a un comportamiento que se desvía de la linealidad ideal.
La aplicación práctica de este factor es crucial. Por ejemplo, en el cálculo de la cantidad de aire en una botella de buceo, asumir un comportamiento ideal puede generar imprecisiones. Si consideramos una botella de 15 litros a 200 bares, y calculamos el volumen teórico como si fuera un gas ideal, podríamos obtener aproximadamente 3000 litros de aire. Sin embargo, al aplicar un factor de compresibilidad (Z) de 1.29, el volumen real se reduce a aproximadamente 200 bares x 15 L / 1.033 (presión atmosférica) / 1.29 (factor Z) ≈ 2904 litros. Esta diferencia, aunque parezca pequeña en términos absolutos, puede ser significativa en cálculos de consumo y autonomía, especialmente en inmersiones prolongadas o en situaciones donde la precisión es vital.
Es importante señalar que el valor de Z no es constante y varía con la presión y la temperatura. La suposición de que Z es 1.033 (un valor cercano a 1) es una simplificación que puede ser válida a presiones relativamente bajas, pero se vuelve menos precisa a medida que la presión aumenta. La discrepancia entre un valor de Z de 1.29 y uno cercano a 1.033 subraya la importancia de utilizar datos de compresibilidad precisos para el gas en cuestión y las condiciones operativas.
Cálculo y aplicación del factor de compresibilidad 2
El Agua Destilada: Pureza y Aplicaciones
El agua, en su estado más puro, es H₂O. Sin embargo, en su ciclo natural y en su distribución, el agua adquiere diversas impurezas, desde sólidos suspendidos hasta microorganismos y sales disueltas. Para muchas aplicaciones, especialmente en laboratorios y en medicina, es esencial eliminar estas impurezas para evitar interferencias, reacciones secundarias no deseadas y sesgos en los resultados.
Existen diferentes grados de tratamiento del agua, cada uno con propiedades y usos específicos:
- Agua Purificada: Ha pasado por algún tipo de tratamiento para eliminar sólidos suspendidos y patógenos. Un ejemplo común es el agua filtrada en hogares mediante filtros de celulosa y carbón activado.
- Agua Desmineralizada: Se obtiene mediante sistemas más complejos que eliminan iones disueltos y otras impurezas. Procesos como la ósmosis inversa y el tratamiento con resinas de intercambio iónico son característicos de este tipo de agua.
- Agua Destilada: Se produce mediante la ebullición del agua y la posterior condensación del vapor resultante. Las impurezas con puntos de ebullición superiores al del agua permanecen en el recipiente original, mientras que el vapor, al condensarse, forma un líquido de alta pureza.
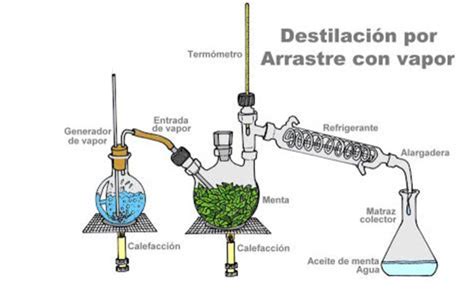
El proceso de destilación sencilla implica calentar el agua hasta que hierva, recogiendo el vapor y enfriándolo en un condensador para que vuelva a su estado líquido. El condensador, típicamente un tubo de vidrio con un flujo de refrigerante (agua fría) circulando por un espacio exterior, facilita la rápida condensación del vapor. La calidad del agua destilada producida depende de la eficiencia del proceso y de la pureza inicial del agua.
El almacenamiento del agua destilada es crucial para mantener su pureza. Se utilizan recipientes específicos, a menudo de plástico, que se limpian rigurosamente de forma periódica.
La característica más distintiva del agua destilada es su baja conductividad eléctrica. Al carecer de iones disueltos, que son los portadores de carga en el agua, su capacidad para conducir electricidad es casi nula. Esta propiedad sirve como un excelente indicador de su pureza.
La norma NC-ISO 3696:2004 establece diferentes grados de calidad para el agua destilada, adaptados a las necesidades de diversos trabajos:
- Grado 1 (Ultrapura): Libre de contaminantes, iones disueltos, coloides y materia orgánica. Es el agua más pura, utilizada en análisis de alta resolución como la cromatografía líquida. Se puede obtener mediante destilación adicional (bidestilada) o por desionización seguida de ultramicrofiltración. Su conductividad eléctrica máxima es de 0.1 μS/cm.
- Grado 2: Puede contener mínimas cantidades de contaminantes inorgánicos. Adecuada para análisis exigentes como la espectrometría de absorción atómica. Se obtiene por destilación múltiple o desionización seguida de destilación. Su conductividad eléctrica máxima es de 1 μS/cm.
- Grado 3: La más común en laboratorios para la preparación de soluciones y limpieza de material. Puede contener bajas concentraciones de contaminantes orgánicos e inorgánicos. Se obtiene por destilación simple o desionización.
El agua destilada es un reactivo de consumo masivo en laboratorios químicos y biológicos, esencial para la preparación de soluciones, la dilución de compuestos y, de manera crítica, para el enjuagado final del material de vidrio. Un último enjuague con agua destilada asegura que no queden trazas de contaminantes que puedan interferir en experimentos posteriores.
Más allá del laboratorio, el agua destilada encuentra aplicaciones en la medicina, como en máquinas de ventilación para humidificar el aire, y en el mantenimiento de vehículos, para rellenar las baterías y prolongar su vida útil. En términos de seguridad, el agua destilada no se considera tóxica ni perjudicial para el medio ambiente. No requiere equipo de protección especial para su manejo, ya que no presenta riesgos significativos para la salud en contacto con la piel, mucosas o por ingestión.
Sin embargo, algunas publicaciones sugieren que el agua destilada, al carecer de minerales esenciales, podría favorecer la lixiviación de minerales del organismo humano. Si bien esta es una consideración a tener en cuenta en el consumo humano prolongado, sus beneficios en aplicaciones técnicas y de laboratorio, donde la pureza es primordial, son indiscutibles. La ciencia detrás de la pureza del agua y la física de los gases reales nos recuerdan que, para obtener resultados precisos y fiables, debemos ir más allá de las simplificaciones y abrazar la complejidad del mundo que nos rodea.