La conductividad del agua es un concepto fundamental que resuena en los dominios de la química y la física, encontrando aplicaciones cruciales en diversos procesos industriales y de investigación científica. Comprender los mecanismos subyacentes a las propiedades de conductividad del agua destilada, particularmente cuando se le añade azúcar, arroja luz sobre la pureza del agua y la naturaleza de la conducción eléctrica. La conductividad, en su esencia, se refiere a la aptitud del agua para permitir el flujo de corriente eléctrica. Este fenómeno está intrínsecamente ligado a la presencia de iones disueltos, como sales, minerales y otras partículas cargadas. La medida de esta capacidad se expresa comúnmente en microsiemens por centímetro (µS/cm), sirviendo como un parámetro vital para evaluar la calidad del agua en una miríada de contextos.
El agua destilada, un producto de un proceso de purificación riguroso, se distingue por su excepcional baja conductividad. Durante la destilación, las impurezas y los iones son meticulosamente eliminados, resultando en un líquido que, en condiciones ideales, presenta una conductividad inferior a 1 µS/cm. De hecho, la conductividad del agua destilada funciona como un indicador sensible de la eficacia del propio proceso de destilación. Es imperativo comprender que el agua en sí misma es un conductor eléctrico deficiente. La conducción de la electricidad a través del agua es, en realidad, facilitada por los iones disueltos en ella.
Para contextualizar, comparemos la conductividad del agua destilada con la del agua potable. El agua potable, enriquecida con minerales y sales disueltas, exhibe una conductividad considerablemente mayor, típicamente en el rango de 50 a 500 µS/cm. Esta diferencia subraya la importancia de la pureza del agua en aplicaciones industriales, donde la conductividad es un barómetro clave de la calidad. Incluso el agua de mar, con su alta concentración de sales, presenta una conductividad significativamente superior a la del agua dulce.
Desde las civilizaciones antiguas, la humanidad ha sentido una profunda fascinación por los fenómenos eléctricos. Vestigios del antiguo Egipto, que datan del 2750 a.C., describen sensaciones de adormecimiento al entrar en contacto con peces eléctricos, junto con la observación de los imponentes rayos durante las tormentas. Estos relatos tempranos sentaron las bases para una exploración científica que se extendería a lo largo de milenios.
Hace más de dos milenios, los filósofos griegos se embarcaron en un viaje introspectivo hacia la naturaleza de la materia. Su indagación culminó en la conceptualización del átomo como la unidad fundamental e indivisible de la materia. Postularon que el átomo estaba compuesto por electrones, partículas cargadas negativamente que formaban la corteza atómica, y un núcleo central. Este núcleo, a su vez, albergaba protones, partículas cargadas positivamente, y neutrones, partículas eléctricamente neutras. En un átomo eléctricamente neutro, el número de electrones es igual al de protones, asegurando un equilibrio de cargas. La diversidad de sustancias en el universo se atribuye a la existencia de un número ilimitado de átomos diferentes, cada uno con una estructura y propiedades únicas. Así, se estableció que la electricidad, en su forma más básica, es un flujo de electrones que se desplazan de manera direccional, saltando de un átomo a otro.
La conciencia de las descargas eléctricas naturales y las generadas por ciertos organismos acuáticos se remonta a tiempos inmemoriales. Textos del Antiguo Egipto ya hacían referencia a los "tronadores del Nilo", peces capaces de emitir potentes descargas eléctricas. Autores de la antigüedad, como Plinio el Viejo y Escribonio Largo, documentaron el efecto paralizante de estas descargas, observando incluso que podían transmitirse a través de materiales conductores.
La electricidad y el magnetismo, aunque fenómenos interrelacionados, fueron estudiados inicialmente como entidades separadas. La generación masiva de electricidad, tal como la conocemos hoy, experimentó un impulso significativo a finales del siglo XIX con la proliferación de la iluminación eléctrica en calles y hogares.
Los filósofos griegos, en su afán por desentrañar la composición de la materia, propusieron diversas teorías. Algunos sostenían que la materia estaba compuesta por cuatro elementos primordiales: tierra, aire, fuego y agua, basándose en la observación de la combustión y la presencia de jugos en los cuerpos. Otros, sin embargo, conjeturaban que la división continua de un cuerpo conduciría eventualmente a partículas sólidas e idénticas, indivisibles. La teoría de los cuatro elementos dominó el pensamiento científico durante más de trescientos años.
Un hito crucial en la comprensión de la estructura atómica llegó en 1895 con el descubrimiento del electrón por Sir Joseph J. Thomson, quien identificó esta partícula elemental con carga negativa. Posteriormente, en 1911, se descubrió el protón, portador de carga positiva, y en 1932, el neutrón, eléctricamente neutro.
El modelo actual postula que un alambre conductor está compuesto por miles de millones de átomos. Cada átomo posee sus protones, neutrones y electrones. Mientras que los protones y neutrones permanecen firmemente anclados en el núcleo atómico, los electrones, particularmente los de las capas externas, tienen una mayor libertad de movimiento. La adición de un electrón a un átomo en un extremo de un alambre puede inducir un efecto dominó, empujando un electrón del átomo vecino y así sucesivamente. Este movimiento secuencial de electrones a través de los átomos es lo que conocemos como corriente eléctrica. La experiencia de una descarga eléctrica al tocar un cable conductor expuesto se debe precisamente a este flujo de electrones a través del cuerpo humano, que actúa como un conductor. Las descargas eléctricas, si son lo suficientemente intensas, pueden ser fatales o causar quemaduras graves.
experimento / proyecto de Electricidad, agua y sal @henrrydc
El físico inglés Stephen Gray (1666-1736) realizó investigaciones pioneras sobre la conductividad eléctrica. En 1729, demostró por primera vez la transmisión de electricidad a través de un conductor, enfatizando la importancia del aislamiento del conductor respecto a tierra para facilitar el flujo de la "virtud eléctrica", como él la denominaba. Sus estudios posteriores exploraron diversas modalidades de transmisión eléctrica.
La noción de "ion" emergió en el campo de la química para describir una molécula o átomo que ha adquirido una carga eléctrica, ya sea positiva o negativa, a través de un proceso conocido como ionización. La ionización ocurre cuando un átomo gana o pierde electrones, alterando su balance de carga eléctrica. Un ion con carga positiva se denomina catión, mientras que uno con carga negativa se llama anión.
En 1884, el científico Svante Arrhenius formuló una teoría revolucionaria que explicaba la disociación de compuestos iónicos en agua. Según Arrhenius, cuando una sustancia como el cloruro de sodio (NaCl) se disuelve en agua, se descompone en sus iones constituyentes: el ion sodio (Na+) con carga positiva y el ion cloruro (Cl-) con carga negativa. Estos iones, cargados eléctricamente, son impulsados en direcciones opuestas por fuerzas eléctricas, y su movimiento a través del agua constituye la corriente eléctrica.
Un material se considera un buen conductor si permite el paso de electrones con facilidad. Los metales son ejemplos paradigmáticos de buenos conductores, al igual que el cuerpo humano, debido a la presencia de numerosas sustancias que existen en forma de iones en nuestros fluidos corporales, como sodio, potasio, calcio, cloruro y bicarbonato. El agua, por sí misma, no es un buen conductor. Su capacidad para conducir electricidad reside en los iones que tiene disueltos. Por lo tanto, el agua pura, como el agua destilada, es un conductor deficiente de la electricidad.
Para que una sustancia sea conductora de electricidad en estado líquido, debe poseer la naturaleza de un electrolito, es decir, debe ser capaz de descomponerse en iones móviles. El agua destilada, al ser purificada mediante destilación para eliminar virtualmente todas las impurezas iónicas, no conduce la electricidad de manera significativa.
Experimentos sencillos ilustran este principio. Al introducir electrodos en agua con sal disuelta, agua con bicarbonato de sodio o jugo de limón, y aplicar una corriente eléctrica, se observa el encendido de una bombilla, indicando la conducción eléctrica. La presencia de sales y otras sustancias disueltas en estos líquidos proporciona los iones necesarios para el transporte de carga.
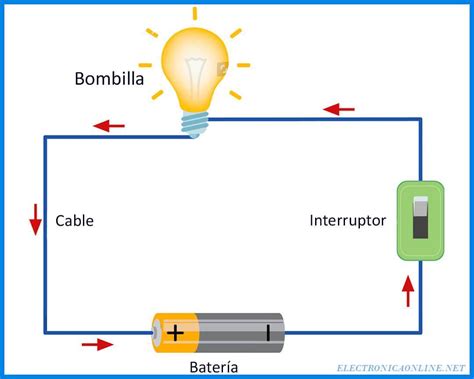
En el ámbito de la experimentación, se pueden utilizar dos puntas conductoras (electrodos) sumergidas en diferentes sustancias líquidas para medir su conductividad. Sustancias como el agua con bicarbonato de sodio, el jugo de limón, el vinagre, la leche con cacao, champú, limpiador antibacteriano, jabón en polvo con agua, agua de fuente, refrescos, tónica, café, agua con sal, bebidas gaseosas y agua de río, todas ellas, al ser sometidas a un campo eléctrico, facilitan el paso de la corriente debido a la presencia de iones disueltos. La intensidad de la conducción puede variar, permitiendo observar diferencias en la conductividad.
La conductividad en medios líquidos está directamente relacionada con la presencia de sales en solución. La disociación de estas sales genera iones positivos y negativos que son capaces de transportar energía eléctrica cuando se aplica un campo eléctrico. En el proceso de electrólisis del agua, si el agua no es destilada, no solo se separan el oxígeno y el hidrógeno, sino que también se ven afectados los demás componentes disueltos, como sales y metales.
La pregunta sobre por qué el agua destilada con azúcar no conduce la electricidad ha cobrado notoriedad, incluso en contextos mediáticos. La sal común, cloruro de sodio (NaCl), es un compuesto iónico. En estado sólido, sus iones (Na+ y Cl-) están fijos en una estructura cristalina y no pueden moverse libremente. Sin embargo, al disolver la sal en agua, la estructura se desmorona, y los iones adquieren una movilidad considerable dentro del volumen del agua. Al aplicar una corriente eléctrica, estos iones se mueven hacia los polos opuestos (Na+ hacia el polo negativo y Cl- hacia el polo positivo), facilitando la conducción eléctrica.
El azúcar, por el contrario, es un compuesto covalente. Sus moléculas no poseen cargas eléctricas que puedan ser liberadas o que se muevan libremente al aplicarse una corriente eléctrica, ni en estado sólido ni cuando se disuelve en agua. Las moléculas de azúcar permanecen intactas y sin carga neta, impidiendo así el transporte de carga eléctrica.
Es una creencia popular errónea que el agua, en general, es un buen conductor de la electricidad. La realidad es que el agua pura es un mal conductor. El agua que encontramos en nuestra vida cotidiana (agua del grifo, agua mineral, agua de ríos) siempre contiene sales minerales disueltas. Son estas sales las que confieren al agua su conductividad eléctrica, al proporcionar los iones necesarios para el flujo de electrones. Por lo tanto, la ausencia de iones disueltos en el agua destilada, combinada con la naturaleza no iónica del azúcar, explica por qué una solución de agua destilada y azúcar no conduce la electricidad.